Das Regenerationsvermögen des Axolotls
Transcrição
Das Regenerationsvermögen des Axolotls
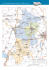
Besondere Lernleistung im Fach Biologie Das Regenerationsvermögen des Axolotls von Claudia Renneberg Klasse 12 Betreuer: Herr Weissert, Frau Wilhelm Riesa, 03.03.2008 2 Gliederung Inhalt Seite 1 Relevanz der Untersuchungen der Regeneration am Axolotl 3 2 Forschungsobjekt Axolotl 4 2.1 Herkunft und natürlicher Lebensraum 5 2.2 Morphologie 5 2.3 Neotenie 5 2.4 Metamorphose 6 3 Ziele der Tanaka Forschungsgruppe 7 4 Meine experimentellen Untersuchungen 8 4.1 Negativkontrolle und Verbindung des „empty vektor“ mit Noggin 8 4.2 Übertragung der Plasmide in die Zellen des Axolotls 9 4.2.1 Injektionsgemische 9 4.2.2 Injektion 12 4.2.2.1 Herstellung der Injektionsnadeln 12 4.2.2.2 Intramuskuläre Injektion 13 4.2.2.3 Intrathekale Injektion 14 4.2.3 Elektroporation 14 4.3 Überprüfung der Elektroporation am Fluoreszenzmikroskop 15 4.4 Amputation des Axolotlschwanzes 16 5 Ergebnisse meiner experimentellen Untersuchungen 17 5.1 Exemplare mit intrathekal injiziertem pSuper-M2 Plasmid 18 5.2 Exemplare mit intramuskulär injiziertem pSuper-M2 Plasmid 18 5.3 Exemplare mit intrathekal injiziertem pSuper-Noggin-M2 Plasmid 18 5.4 Exemplare mit intramuskulär injiziertem pSuper-Noggin-M2 Plasmid19 5.5 Zusammengefasste Erkenntnisse 20 6 Danksagung 21 7 Quellenverzeichnis 22 8 Literaturverzeichnis 23 9 Selbstständigkeitserklärung 24 10 Anlagenverzeichnis 25 11 Bildnachweis 49 6 7 8 10 13 16 48 3 1 Relevanz der Untersuchungen der Regeneration am Axolotl Laut der Deutschen Stiftung Organtransplantation (DSO) in Berlin herrscht noch immer ein Mangel an Spenderorganen in Deutschland. „Rund 12.000 schwer kranke Menschen warteten vergeblich auf ein lebensrettendes Herz, eine Lunge, eine Leber oder eine Bauchspeicheldrüse...“ 1, dies ließ die DSO am Tag der Organspende am 2.6.2007 verlauten.2 „Täglich stürben in der Bundesrepublik drei Menschen, weil sie nicht rechtzeitig ein Organ erhielten.“ Alarmierend ist auch die Wartezeit beispielsweise für eine Niere. Diese beträgt durchschnittlich sechs Jahre, laut Aussagen der Deutschen Stiftung Organtransplantation.1 Im Hinblick auf diese Missstände gewinnt das Thema Regeneration in der Forschung immer mehr an Bedeutung. Wären wir Menschen in der Lage, unsere verletzten oder verloren gegangenen Organe selbstständig neu zu bilden, ohne dabei Verluste in Funktion und Formung dieser defekten Körperteile zu erleiden, könnte vielen Patienten eine langwierige, physisch und psychisch schwere Behandlung erspart bleiben und ihr Leben verlängert werden. Doch leider wurde diese Fähigkeit in solch einem organumfassenden Maße uns Menschen der Gegenwart nicht zuteil. Sie ist unter anderem dem mexikanischen Axolotl gegeben. Um dennoch Vorteile aus dem Themengebiet Regeneration für die medizinische Betreuung von Patienten zu gewinnen, ist es wichtig zu erfahren, welche Vorgänge im sich regenerierenden Axolotlkörper ablaufen. Denn nur, wenn der komplette Regenerationsprozess im Axoltol in seine einzelnen Abläufe aufgelöst und verstanden wird, können die daraus gewonnenen Erkenntnisse auf sich nicht in diesem großen Maße neubildenden Organismen - wie den Menschen - übertragen werden. In diesem Bereich der Grundlagenforschung war ich vom 2.7.2007 bis zum 11.7.2007 im Max-Planck-Institut für molekulare Zellbiologie und Genetik in Dresden a tätig. Meine konkrete Aufgabe im Bereich der Aufschlüsselung des Regenerationsprozesses bestand darin, zu untersuchen, ob ein bestimmtes Protein an der Neubildung des Axolotlschwanzes beteiligt ist. 4 2 Forschungsobjekt Axolotl Der Name Axolotl b,c leitet sich aus dem Náhuatl, der Sprache der Azteken, 3 ab und ergibt sich aus den Worten Atl, der Bezeichnung für Wasser, und dem Namen einer Gottheit, Xolotl. 4 Der Name des Gottes heißt übersetzt Zwilling und ist der Gott des Blitzes, der Wächter der Unterwelt, welcher die Sonne täglich in die Erde hinab und wieder empor geleitet. 5 Aus diesem Zusammenhang lässt sich die Herkunft der Übersetzung des Namens Axolotl mit „Wassermonster“, „Wasserspiel“ oder „Wasserpuppe“ begründen. Trotz dieser göttlichen Verbindung landeten diese Tiere oft im Kochtopf und wurden als Grundstoff verschiedener Heilmittel genutzt, da ihnen heilende Kräfte zugesprochen wurden. 1805 wurden erstmals durch Alexander von Humboldt zwei Exemplare dieser Querzahnmolche nach Europa gebracht, doch erst 1863 führten französische Forscher eine größere Gruppe der hier besprochenen Salamanderart ein. 4 Seither hatte Ambystoma mexicanum einen großen Anklang in der Forschung. Dies beruht zum einen darauf, dass der Axolotl die Metamorphose in seinem natürlichem Biotop nicht durchführen kann, aber dies im Labor möglich ist, und zum anderen wird der Grund für das narbenlose Regenerationsvermögen von kompletten Körperteilen und verletzten Organen untersucht, um daraus in der Zukunft einen Nutzen für den Menschen zu erschließen. 6 Abgesehen von diesen Fähigkeiten sprechen noch andere Eigenschaften dieser Schwanzlurche für einen Einsatz in der Forschung. Sie haben eine massive Individuenanzahl, die pro Laich 100-300 Eier umfasst. Auch ist die Zeit, die bis zum Schlupf der Jungtiere vergeht, mit drei Tagen relativ kurz. 3 Es besteht auch die Möglichkeit, die Tiere während ihres Ei-Stadiums auf bestimmte Eigenschaften zu untersuchen, denn die Größe der Eier liegt bei rund drei Millimetern und sie sind damit gut zu handhaben. Ebenfalls erleichtert das Auftreten von Teilalbinos den Einsatz und das Erkennen von in den Körper injizierten Farbstoffen mit dem bloßen Auge. Die Tiere stellen auch keine besonderen Ansprüche an ihre Unterbringung. Die kleineren, für meine Untersuchungen geeigneten, Exemplare (bis zirka zwei Zentimeter) bewohnen Trinkbecher, welche 0,2 l Fassungsvermögen haben d und die größeren Axolotl verweilen zwischen den jeweiligen Untersuchungen in 0,5 l - Kunststoffbecken. Lediglich die Besetzung der adulten, bis 30 cm großen, Zuchttiere muss im 50 l - Becken mit genügend Sauerstoffzufuhr stattfinden und nimmt somit recht viel Platz ein. 5 2.1 Herkunft und natürlicher Lebensraum „Axolotl als endemische Art sind wild lebend ausschließlich noch im südöstlich unweit von Mexiko City auf vergleichbarer Höhe über dem Meer gelegenen Xochimilcosee zu finden (FREYTAG 1970; ZUCCHI & GONSCHOREK 1983).“ 7,e „Dieses Gewässer, welches noch von den Azteken als „Mondsee“ bezeichnet wurde, besteht heute aus einer Vielzahl von sumpfigen Bereichen und Kanälen, die 20 Meter Breite nicht überschreiten und Tiefen von einem bis zu zehn Metern aufweisen“ 8 „Das ursprüngliche Seensystem dieser Hochebene ist zwischenzeitlich durch anthropogene, vom Menschen verursachte, Einflüsse in seiner Ausdehnung stark reduziert. f Lediglich ein Gebiet von etwa 35 Quadratkilometern ist noch dem unmittelbaren Einzugsgebiet des auch durch Quellwasser gespeisten, reines Süßwasser enthaltenen Sees zuzuordnen (BRANDON 1989, ZUCCHI & GONSCHOREK 1983); der Rest des ehemals umliegenden Gewässers ist bereits trockengefallen und gleicht nach der beginnenden Verkarstung zunehmend der semiariden Umgebung.“ 7 2.2 Morphologie „Die Larven und die neotenen geschlechtsreifen Tiere wirken vom Körperbau her gedrungen, zeigen breite, relativ stumpf erscheinende Köpfe, kräftige Extremitäten und deutlich ausgeprägte Rippenfurchen.“ 9 Am hinteren Teil des Kopfes tragen sie beidseitig drei kräftige Kiemenäste und der seitlich abgeflachte Ruderschwanz ist mit einem, die Wirbelsäule entlang laufenden, Hautsaum versehen. 9 Die im Vergleich zum Kopf winzig wirkenden, im Wildtyp gelben Augen, sind am Schädel oben, weit auseinanderstehend, angesetzt. Das Maul ist sehr breit, leicht unterständig und insgesamt leicht abgerundet.10 2.3 Neotenie „Die umfassendste heute als gültig angesehene und seit langem gebräuchliche Definition des Begriffs der Neotenie im Bereich der Wirbeltiere sieht Tiere dann als neoten an, wenn diese in der Lage sind oder in der Lage zu sein scheinen, sich zu reproduzieren während sie noch larvale Merkmale zeigen (JUST et al. 1981).“ 11 Speziell auf die Axolotl bezogen bedeutet dies eine induzierbar-obligatorische Neotenie. „Solche Schwanzlurche kommen in natürlicher 6 Umgebung ihr Leben lang nie zur Metamorphose, haben aber die Sensitivität für das zur Metamorphose notwendige Schilddrüsenhormon, Thyroxin, nicht grundsätzlich verloren“. 12 Vielmehr ist dieses Dauerlarvenstadium von einer Schilddrüsenunterfunktion abzuleiten, bei welcher zu wenig Thyroxin gebildet wird, um den Hormonreiz, der zum Auslösen der Umwandlung nötig ist, im Laufe der Ontogenese (=Individualentwicklung) zu erreichen. 12 2.4 Metamorphose „Eine exakte allgemeine Begriffsdefinition für diesen Prozess existiert trotz jahrzehntelanger Forschung bisher nicht.“ 13 Gut brauchbar sind die von JUST et al. 1981 aufgestellten Kriterien zur Feststellung dieses Umwandlungsvorgangs. 13 „Damit diese vorliegt, müssen Tiere über ein definierbares Larvenstadium verfügen, welches klar von dem des Embryos und dem des geschlechtsreifen Tieres abgrenzbar ist.“ 13 Die Veränderung muss sich in dem Zeitraum zwischen Schlupf und Geschlechtsreife vollziehen und „Strukturen umfassen, die nicht mit der Fortpflanzung im Zusammenhang stehen. Prozesse, die mit der sexuellen Reifung, der Alterung oder der Embryonalentwicklung verbunden sind, müssen vom Metamorphosegeschehen trennbar sein.“ 13 Als Auslöser für eine Metamorphose treten externe Faktoren, wie zum Beispiel die Änderung von Umweltbedingungen, oder interne Faktoren, wie die Veränderung des Hormonstatus, welche jedoch der Beeinflussung durch Ersteres unterliegen kann, auf. 13 Insgesamt ist die Metamorphose als eine Umwandlung zu sehen, die mit dem Wechsel des Lebensraumes einhergeht. Aus den aquatischen, über Kiemen und Haut atmenden Larven werden lungenatmende, terrestrische Adulttiere. 12 Ein Paradebeispiel für die Verwirklichung dieser Kriterien ist die klassische Froschentwicklung. „Aus dem sich im Ei früh entwickelnden Embryo entsteht eine Kaulquappe, die typische larvale Strukturen, wie etwa das Raspelmaul und den Ruderschwanz, aufweist.“ 13 Die Larven sind an das Wasser gebunden. Den für die Atmung benötigten Sauerstoff entnehmen sie über Kiemen dem Wasser und die Ernährung erfolgt vegetarisch, woraus ein relativ langer Darm resultiert. Die adulten Frösche hingegen nehmen über die Lungen atmosphärischen Sauerstoff auf und verbringen den größeren Teil der Zeit 7 an Land. Sie haben einen relativ kurzen Darm auf Grund ihrer tierischen Kost. Der Schwanz wird zum Fortbewegen nicht mehr benötigt und fehlt vollkommen. 13 „Strukturell ist das Larvenstadium eindeutig von Embryo und geschlechtsreifem Tier getrennt, bestimmte Systeme sind nur larval vorhanden. Kaulquappe und Frosch nutzen unterschiedliche Lebensräume und unterschiedliche Ressourcen“. 14 Bei Betrachtung der oben genannten Kriterien findet man diese bei der Froschentwicklung alle erfüllt. Verglichen damit sind die Verhältnisse beim Axolotl weit weniger deutlich. Sowohl die Larven als auch die geschlechtsreifen Tiere beanspruchen das Wasser als Lebensraum für sich, ihre Nahrung ist vergleichbar, sie verändert sich nur relativ zum Wachstum. Ebenso bei der Grundgestalt beider Entwicklungsstadien, denn „viele Organsysteme und Verhaltensweisen verändern sich nur wachstumsbedingt, echte Larvalorgane scheinen zu fehlen“.10 Als einziger auffälliger Unterschied ist die strukturelle Veränderung durch die Geschlechtstreife adulter Tiere, welche aber als „Kriterium für eine Metamorphose nicht zugelassen“ ist. 14 So gesehen ist eine vollständige Metamorphose beim frei lebenden Axolotl nicht anzutreffen. Doch besteht die Möglichkeit, von außen experimentell dem Tier unter anderem das Schilddrüsenhormon Thyroxin zu verabreichen und den Querzahnmolch somit zur vollständigen Umwandlung zu einem terrestrischen Axolotl zu bringen. 14 Aus diesen Sachverhalten geht hervor, dass Ambystoma mexicanum „ganz offensichtlich auf natürlichem Weg nicht zur vollständigen Metamorphose gelangen, obwohl sie sich ebenso eindeutig fortpflanzen können. Dieser Zusammenhang zeigt deutlich, dass zumindest die reproduzierenden Organsysteme ( ..., Kloakaldrüsen, Kloakenregion) den Vorgängen unterliegen müssen, die in den metamorphosierenden Formen erst mit oder nach dem Landgang stattfinden; ein wichtiger Hinweis auf das als Teilmetamorphose beschriebene Geschehen“. 15 8 3 Ziele der Tanaka Forschungsgruppe Die Forschungsgruppe unter der Leitung Elly Tanakas führt Untersuchungen am Axolotl durch, um Fragen über das Regenerationsvermögen großer Teile des Zentralen Nervensystems und kompletter Extremitäten dieser Tiere zu klären. Ein Schwerpunkt ihrer Forschung ist der mit der Regeneration verbundene Wiedereintritt ausdifferenzierter Zellen in den Zellzyklus und die Fähigkeit der ausdifferenzierten Zellen des Axolotls, sich bei der Regeneration zu vermehren. Das Gesamtziel dieser Forschungen ist es, den Mechanismus, der den ganzen Regenerationsprozess steuert, mit seiner Flexibilität und seinen nahezu unbegrenzten Erneuerungen zu verstehen. 4 Meine experimentellen Untersuchungen In meinen im Folgendem beschriebenen Experimenten untersuchte ich den Einfluss des Signalproteins BMP4 auf das Regenerationsvermögen des Axolotls. Das BMP4 gehört zu den Bone Morphogenetic proteins - morphogenetische Knochenproteine - die grundlegende Ereignisse in der frühen embryonalen Entwicklung und in der Organogenese kontrollieren. Die BMP-Proteine sind eine Gruppe einander ähnlicher Signalproteine, die in den Zellen produziert werden und von diesen dann ausgeschleust werden, um benachbarte Zellen zu beeinflussen. 16 Die von den signalgebenden Zellen ausgeschütteten BMPs gelangen über Diffusion zu den benachbarten Zellen und binden sich dort an die Membranrezeptoren, welche dieses Signal durch die Zellmembran hindurch in das Zellinnere weiterleiten. In einer Signalkaskade, bei der die Signale über Enzyme und sekundäre Botenstoffe über eine oder mehrere Ebenen bis hin in den Zellkern weitergeleitet werden, werden sie verstärkt. 17 Im Zellkern angelangt, kann dieses Signal eine Veränderung der Genaktivität hervorrufen, „was letztendlich dazu führt, dass die Empfängerzelle ihre Proteinzusammensetzung und damit ihre Eigenschaften verändert“.16 Doch reagiert je nach Zustand der Zelle, je nach Dauer und Stärke des Signals die Empfängerzelle unterschiedlich auf das Signal. Auch spielt der Typ des BMPs dabei eine entscheidende Rolle. Doch können diese Signalproteine auch durch andere Proteine abgefangen und unwirksam gemacht werden. Solch ein Inhibitor, der sich an das BMP4 heftet und somit dessen 9 räumliche Struktur so verändert, dass es von der Empfängerzelle nicht mehr erkannt wird, ist zum Beispiel das Noggin. 16 Mit Hilfe dieses Hemmstoffes konnte ich sehen, ob die Regeneration des von mir amputierten Axolotlschwanzes vom BMP4 abhängig ist. Beim Einsatz des Noggins müsste, wenn man davon ausgeht, dass das BMP4 für die Regeneration eine wichtige Rolle spielt, der Schwanz sich nicht neu ausbilden beziehungsweise in irgendeiner Form nicht komplett regeneriert sein. 4.1 Negativkontrolle und die Verbindung des „empty vektor“ mit Noggin Eine Negativkontrolle wurde in diesen Experimenten mit eingebracht, um zu sicher zu gehen, dass die Elektroporation oder die Injektion an sich keine Wirkung auf die Regeneration hat. Somit habe ich in diesen Experimenten bei der Hälfte der mir zur Verfügung stehenden Axolotlexemplaren anstelle der DNA des pSuper-Noggin-M2, die pSuper-M2 DNA injiziert. Dieses pSuper-M2 ist ein sogenannter „empty vektor“, das heißt, dieses Protein hat keinerlei Funktionen im Axolotlorganismus. Diese Gegebenheit, um einen „stummen“ Noggin-DNA-Träger zu finden, ausnutzend, „schnitten“ die Forscher das präparierte Plasmid - ein aus Bakterien gewonnener ringförmiger Träger von genetischen Informationen, welches das pSuper-M2 Protein synthetisiert - auf und klonten die für die Noggin-Synthese zuständigen Basensequenzen hinein. Somit kann der Inhibitor Noggin über das nun entstandene pSuper-Noggin-M2 Plasmid in den Zellen des Axolotls in Verbindung mit dem BMP4 seine hemmende Wirkung auf die Regeneration freisetzen. Sowohl der Inhibitor pSuper-Noggin-M2, als auch die Negativkontrolle pSuper-M2 wird von den Zellen selbst gebildet, doch dazu muss, wie im vorhergegangenen Text schon einmal angesprochen, die genetische Information für diese Proteine in den Zellen des Axolotls vorhanden sein. Dazu bedient man sich mit von Bakterien stammenden Plasmiden, denen - wie oben beschrieben - der einen Hälfte die genetische Information des Noggins hinzugefügt wird. 10 4.2 Übertragung der Plasmide in die Zellen des Axolotls Um die DNA dieser beiden Proteine in die Zellen des Axolotls zu übertragen, bedarf es dreier wichtiger Schritte: Die Vorbereitung des „Impfstoffes“, die Injektion und die Elektroporation. 4.2.1 Injektionsgemische Für die Axolotl bereitete ich zwei verschiedene Injektionsstoffe vor. Die Grundsubstanz der einen Mixtur bestand aus dem pSuper-Noggin-M2 Plasmid und die andere bekam das pSuper-M2 Plasmid als Ausgangspunkt. Beiden fügte ich den Farbstoff „fast green“ hinzu, der die Injektionsstelle mit einem für das bloße Auge blau erscheinende Farbe markiert. Auch mischte ich jeweils einen fluoreszierenden Farbstoff den zu injizierenden Stoffen unter. Dieses GFP-T2A-Cherry Reporterplasmid geht bei der Elektroporation mit dem pSuper-Noggin-M2 beziehungsweise mit dem pSuper-M2 Plasmid in die Zellen über und markiert somit bei der Belichtung im red- beziehungsweise green-Channel, am Fluoreszenzmikroskop, die Zellen, welche die Plasmide beinhalten. Unter Vorgaben einzuhaltender Maßstäbe für die einzelnen Bestandteile dieser Gemische, fügte ich alle Einzelteile im Mikroliterbereich zusammen. Für das erste Stoffgemisch erhielt ich folgende Richtlinien: Es sollte in 20μl (= 0,02ml) eine Konzentration der Stoffe pSuper-Noggin-M2 und GFP-T2A-Cherry von jeweils 0,5 mg*ml-1 vorhanden sein und des weiteren sollte sich 1μl des Farbstoffes „fast green“ in diesem Injektionsstoff befinden. Aus diesen Angaben ergibt sich, dass von jedem Einzelbestandteil 0,01mg dem Ganzen hinzugefügt werden muss, denn: ρ = m/V m= ρ*V = 0,5 mg*ml-1 * 0,02ml = 0,01mg . Von dem im Labor bereitgestellten Einzelbestandteilen waren 1,9mg*ml-1 vom pSuper-Noggin-M2 vorhanden und davon müssen ≈5,26 μl in das Endgemisch zugeführt werden. Dies ergibt sich aus folgender Berechnung: ρ = m/V V = m/ρ = 0,01mg / 1,9mg*ml-1 ≈ 0,00526 ml ≈ 5,26 μl . Von dem zweiten Bestandteil der p-Super-Noggin-M2 Plasmid-Mixtur, dem Reporterplasmid 11 GFP-T2A-Cherry, waren im Labor 0,78mg*ml-1 vorhanden. Aus dieser Menge mussten, um die Konzentration von 0,5mg*ml-1 in dem Endgemisch zweier Bestandteile zu erhalten, diesem ≈12,82 μl vom GFP-T2A-Cherry Plasmid zugesetzt werden. Dieses Ergebnis erhielt ich, als ich die gegebenen Faktoren in die nachstehende Gleichung einsetzte: ρ = m/V V = m/ρ = 0,01mg / 0,78mg*ml-1 ≈ 0,01282 ml ≈ 12,82 μl Mit Hilfe der errechneten Maße konnte ich die Menge des PBS’s, einem Salz-Wasser-Gemisch, bestimmen, welches als Füllstoff dient. Das PBS wird der Summe der Einzelbestandteile des Injektionsstoffes beigefügt, sodass das Gesamtvolumen des Injektionsstoffes 20 μl betrug. Im Fall der pSuper-Noggin-M2 Plasmid-Mixtur musste dieser Mischung 0,92 μl des PBS-Füllstoffes untergemischt werden, damit sich, wie oben erwähnt, das Gesamtvolumen auf 20 μl belief. VPBS = 20 μl – ( V pSuper-Noggin-M2 Plasmid + V GFP-T2A-Cherry Plasmid + 1 μl fastgreen ) = 20 μl – ( 5,26 μl + 12,82 μl + 1 μl ) = 0,92 μl Bei der Herstellung des zweiten Injektionsstoffes, mit dem pSuper-M2 Plasmid als Basis, wurde mir wieder die Anweisung gegeben, sowohl eine Konzentration der Einzelbestandteile pSuper-M2 und GFP-T2A-Cherry von 0,5 mg*ml-1 in einem Gesamtvolumen des Injektionsstoffes von 20 μl zu erreichen, als auch einen μl des Farbstoffes „fast green“ in das Gemisch einzubinden. Wie schon im vorausgegangenen Mischungsplan angegeben, musste von jedem Einzelbestandteil, sprich von dem pSuper-M2 und dem GFP-T2A-Cherry Plasmiden, jeweils 0,01mg dem Injektionsstoff beigemischt werden, damit die Konzentration der beiden Plasmide bei 0,5 mg*ml-1 lag. Der mir zur Verfügung stehende Vorrat an pSuper-M2 Plasmiden betrug 2,35 mg*ml-1. Aus der Rechnung: ρ = m/V V = m/ρ = 0,01mg / 2,35 mg*ml-1 ≈ 0,004255 ml ≈ 4,26 μl ließ sich die benötigte Menge an pSuper-M2 Plasmiden herleiten, um das erforderliche Gewicht von 0,01 mg und damit die Konzentration von 0,5 mg*ml-1 in dem Injektionsgemisch zu erreichen. Der nächste Bestandteil der pSuper-M2-Mixtur ist das GFP-T2A-Cherry Reporterplasmid. Von diesem wurden wie in der oben bereits beschriebenen Anfertigung des pSuper-Noggin-M2-Injektionsgemisches ≈12,82 μl benötigt, um die erwünschte 0,5mg*ml-1-Konzentration in dem Endgemisch zu erlangen. 12 Bedenkt man wieder die 20 μl, welche des fertige Injektionsgemisch bilden musste, erkennt man, dass wieder ein bestimmter Wert an Salzwasser, dem PBS, dem Gemisch hinzugefügt werden musste. Um diesen Wert zu erhalten, addierte ich erneut alle Volumen der Einzelbestandteile mit Einbezug des „fast green“ mit seinem einen Mikroliter (μl) und subtrahierte den erhaltenen Betrag von dem Gesamtvolumen, den 20 μl, und erhielt somit die Menge des PBS, mit dem ich den Injektionsstoff auffüllte und ihn damit für die Injektion in die Axolotl fertig stellte. VPBS = 20 μl – ( V pSuper-M2 Plasmid + V GFP-T2A-Cherry Plasmid + 1 μl fastgreen ) = 20 μl – ( 4,26 μl + 12,82 μl + 1 μl ) = 1,92 μl Alle die zu vermischenden Einzelbestandteile des Injektionsstoffes im Mikroliterbereich maß ich mit einer Mikroliterpipette ab. Mit dieser Kolbenhubpipette konnte ich auf zwei Dezimalstellen hinter dem Komma genau das benötigte Volumen in die Pipette aufnehmen, um eine exakte Dosierung vorzunehmen. Damit eine Verunreinigung beziehungsweise eine Vermischung der Injektionsbestandteile untereinander nicht stattfinden konnte, verwendete ich bei jeder neuen Flüssigkeitsaufnahme mit der Pipette eine neue Kunststoffpipettenspitze. j 4.2.2 Injektion Unter einer Injektion versteht man „... das Einspritzen von (sterilen) Flüssigkeiten mit einer Injektionsspritze und einer Injektionsnadel (Kanüle) in den Körper.“ 18 Speziell auf meine Experimente bezogen heißt dies, dass ich fünf Exemplaren meiner insgesamt 20 Axolotl das Impfstoffgemisch mit dem pSuper-M2 Plasmid als Grundlage in die Schwanzmuskeln injizierte und weiteren fünf Tieren den selben Injektionsstoff in das Rückenmark, in Höhe der Mitte des Schwanzes. Auch der andere Injektionsstoff, welcher auf dem pSuper-Noggin-M2 Plasmid basiert, wurde in zehn Exemplare gegeben. Wieder wurde die Injektion an zwei verschiedenen Stellen verabreicht: fünf Exemplare bekamen die pSuper-Noggin-M2 Plasmide in die Muskelfasern der Schwanzregion geimpft und die restlichen fünf Axolotl bekamen die Injektionsmischung in das Rückenmark. 13 4.2.2.1 Herstellung der Injektionsnadeln Bevor ich dies mit Hilfe eines Injektionsmikroskops g durchführen konnte, musste ich die Injektionsnadeln herstellen. Dafür standen mir ca. 12 Zentimeter lange Glasröhrchen zur Verfügung, die einen ungefähren Durchmesser von einem Millimeter hatten. Diese spannte ich einzeln an beiden Enden in eine Apparatur ein, welche die Mitte des Glasröhrchen erhitzte und die Enden des Glasstückes auseinander zog. Der durch die starke punktuelle Erwärmung verflüssigte mittlere Abschnitt verjüngte sich durch die gleichmäßig von beiden Seiten angreifende Zugkraft soweit, dass sich das eine Glasröhrchen in zwei sehr dünne, geschlossene Spitzen teilte. Um aus diesen gläsernen Nadeln durchgängige Kanülen herzustellen, musste ich die Glasröhrchen in eine Halterung am Injektionsmikroskop bringen. h Unter einer 11-fachen Vergrößerung der Nadelspitze entfernte ich mit Hilfe einer Pinzette den vorderen Teil der Glasröhrchen, sodass einsetzbare Injektionsnadeln entstanden. In jeweils eine dieser Kanülen füllte ich die vorbereiteten Injektionsgemische mit einer manuellen Mikroliterpipette. j 4.2.2.2 Intramuskuläre Injektion Bei zehn Axolotl führte ich eine intramuskuläre Injektion durch. Dieses Einbringen der Injektionsstoffe in die Muskelzellen des Schwanzes führte ich an einem Injektionsmikroskop aus, nachdem ich kurz vor der eigentlichen Injektion den jeweiligen Axolotl aus seinem Becher in ein Bad mit Narkosemittel ließ. Immer wenn sich der schlafende Axolotl auch nach einer Berührung nicht mehr sichtlich bewegte, verlagerte ich das Tier auf eine Platte und steckte es mit Nadeln an der Unterlage fest. Da die Tiere austrocknen konnten, mussten sie in einer kleinen Wasserlache auf der Platte liegen. Diese Platte schob ich daraufhin unter das Objektiv des Mikroskops und vergrößerte den Abschnitt 11-fach, den ich für die geeignetste Injektionsstelle ausgewählt hatte. Die Position der bereits mit einem Injektionsstoff präparierten und in eine Halterung am Mikroskop angebrachten Injektionsnadel konnte ich nun mit Hilfe von Stellrädern so verändern, dass die Nadelspitze im Ausschnitt der Injektionsstelle zu sehen war. Nun konnte ich die Injektionsnadelspitze in den Axolotlkörper, genauer gesagt in den Bereich der Muskelzellen, eindringen lassen. War die Kanüle genau platziert, betätigte ich ein Fußpedal, welches das Einschießen des in der Nadel befindlichen Gemisches bewirkte. Auch 14 bei jedem weiteren Bedienen des Pedals wurde eine kleine Menge des Injektionsstoffes über Druckluft in den Axolotlkörper freigelassen. Durch den für das bloße Auge blau wirkenden Farbstoff „fast green“ war es mir möglich die Injektionsstelle und den genauen Ort der injizierten Plasmide auch mehrere Stunden nach vollendeter Injektion für weitere Untersuchungen wiederzufinden. Auffallend dabei war die kleine kreisförmige bläuliche Färbung um die Einspritzstelle, welche die Größe des Ausbreitungsbereiches des eingespritzten Stoffes markierte. Nach erfolgter Injektion befreite ich die Molche von ihrer Unterlage, indem ich die Nadeln aus ihrem Flossensaum herauszog und ging mit den noch schlafenden Tieren zur Elektroporation über. 4.2.2.3 Intrathekale Injektion Das Einspritzen von Impfstoffen in das Rückenmark oder in das Gehirn wird als intrathekale Injektion bezeichnet und verläuft exakt wie die intramuskuläre Injektion ab. 19 Nur mit dem Unterschied, dass als ideale Injektionsstelle ein Abschnitt des durch den ganzen Axolotlkörper laufendes Rückenmarks ausgesucht wird. Auch ist die farbliche Markierung durch das „fast green“ nicht auf einen Hof um die Einspritzstelle beschränkt, sondern das gesamte Rückenmark erhält eine bläuliche Färbung, wobei die leichte beim Einstechen entstandene Verletzung eine intensivere Färbung für mehrere Stunden beibehält. 4.2.3 Elektroporation Mit der Elektroporation wird der Transfer der sich im Zellzwischenraum befindlichen injizierten Plasmide in die Zellen beabsichtigt. Durch diese Methode werden die Zellmembranen über ein elektrisches Feld für wenige Millisekunden permeabel gemacht, sodass die großen Plasmide in die Zellen eingeschleust und zum Zellkern transportiert werden können. 20 Für den Elektroporator, i dem Gerät, welches das elektrische Feld erzeugt, bekam ich bestimmte Anweisungen, auf welche Parameter ich dieses Gerät einzustellen habe. k Mit einer Gleichspannung von 15 V brachte ich zwei Elektrodenplatten ober- und unterhalb der Injektionsstelle am Axolotl in Position. Dabei war es wichtig, darauf zu achten, dass die 15 zwei Elektroden über das Wasser, welches den noch schlafenden Axolotl umgab, miteinander verbunden waren. Doch durften die Elektrodenplatten den Körper des Axolotls nicht berühren. Wurden dann die 15 V Spannung angelegt, bildeten sich um und zwischen den Elektroden Blasen, und der Axolotl begann zu zucken, da durch die elektrischen Impulse die Muskeln zum Kontrahieren und Erschlaffen gebracht wurden. Nach einer Wartezeit von 19 Stunden überprüfte ich am Fluoreszenzmikroskop, l ob die Elekrtoporation erfolgreich war. 4.3 Überprüfung der Elektroporation am Fluoreszenzmikroskop Das in dem Injektionsgemisch enthaltene GFP-T2A-Cherry Reporterplasmid diente als fluoreszierender Farbstoff, welcher mit den anderen Plasmiden bei der Elektroporation in die Zellen überging. Die nach den genetischen Informationen des Plasmids synthetisierten Proteine markierten bei Belichtung im red- beziehungsweise green-Channel des Fluoreszenzmikroskops somit die Zellen, welche die pSuper-M2 beziehungsweise die pSuperNoggin-M2 Plasmide enthalten. Bei diesem Vorgang werden die Zellen um die Elektroporationsstelle eine bestimmte Zeit mit einem Laserlicht bestrahlt. m Dieses Licht umfasst im red-Channel eine Wellenlänge von 490 bis 575 nm, und erscheint somit grün. Im green-Channel beträgt die Wellenlänge des Laserlichtes 420 bis 490 nm und ist somit als blaues Licht für uns sichtbar. 21 Während der kurzzeitigen Belichtung wird das „Farbprotein“ angeregt und emittiert in einer höheren Wellenlänge. Dies führt dazu, dass im red-Channel das abgestrahlte Licht im Fluoreszenzmikroskop rot erscheint und eine Wellenlänge von 650 bis 750 nm besitzt. Im green-Channel dagegen fluoresziert das „Farbprotein“ grün und weist eine Wellenlänge von 490 bis 575 nm vor. 21 Bei der Belichtung meiner 20 Axolotlexemplare in dem Fluoreszenzmikroskop, 19 Stunden nach der Elektroporation, war das GFP-T2A-Cherry Reporterplasmid in keiner Zelle im red- beziehungsweise green-Channel zu sehen. Folglich wurden auch die pSuper-Noggin-M2 und die pSuper-M2 Plasmide nicht in die Zellen elektroporiert. Nur bei zwei Axolotl war ein geringes Leuchten sichtbar. Dies ließ mich zu dem Schluss kommen, dass die Elektroporation vielleicht auf Grund einer zu niedrigen Spannung misslungen war und ich nun mit 20 neuen Exemplaren die Injektion, 16 Elektroporation und die Überprüfung der Plasmidübertragung am Fluoreszenzmikroskop in gleicher Weise wiederholte. Für die intrathekale und intramuskuläre Injektion nahm ich die von mir schon einmal vorbereiteten Injektionsgemische mit dem pSuper-M2 und dem pSuper-Noggin-M2 Plasmiden als Grundlage, denen ich jeweils einen weiteren Mikroliter des Farbstoffes „fastgreen“ hinzufügte, um die Gesamtmenge der Injektionsstoffe zu erhöhen, damit ich die weiteren 20 Exemplare mit genügend Impfstoff versorgen konnte. Für eine erfolgreichere Elektroporation erhöhte ich die Spannung am Elektroporator auf 30 V, was dementsprechend stärkere Zuckungen der Schwanzmuskeln und eine vermehrte Bläschenbildung hervorrief. n Bei der darauffolgenden Überprüfung der Elektroporation am Fluoreszenzmikroskop im redbeziehungsweise green-Channel waren bei elf Exemplaren rote beziehungsweise grüne Farben zu erkennen, was daraus schließen ließ, dass die Elektroporation erfolgreich war und das GFP-T2A-Cherry Reporterplasmid zusammen mit den pSuper-M2 beziehungsweise dem pSuper-Noggin-M2 Plasmid in den Zellen der Axolotlkörper vorhanden war. 4.4 Amputation des Axolotlschwanzes Die Amputation führte ich an einem Fluoreszenzmikroskop durch, unter welches ich die in Anästhetikum gebadeten Axolotl legte und die Zellen mit dem fluoreszierenden „Farbprotein“ suchte. Hatte ich die erwähnten Zellen ausfindig gemacht, schnitt ich mit einem Skalpell den dahinter befindlichen Teil des Schwanzes ab. Dabei versuchte ich die plasmidhaltigen Zellen geringfügig zu verletzen, um sicher zu gehen, dass diese speziellen Zellen an der Regeneration des Schwanzteiles beteiligt sind. 17 5 Ergebnisse meiner experimentellen Untersuchungen In denen von mir zusammengesetzten Einzelbildern aus dem Fluoreszenzmikroskop konnte ich die in den letzten acht Tagen nach der Amputation abgelaufene Regeneration des Axolotlschwanzes bildlich festhalten. Zu diesem Zweck arbeitete ich mit dem Fluoreszenzmikroskop verbundenen Computerprogramm MetaVue, wodurch ich simultane Bilder des narkotisierten Axolotls auf dem Computerbildschirm erhielt und diese als momentane Einzelbilder abspeichern konnte. o Somit war es mir möglich, Aussagen über die Wirkung des BMP4 Proteins auf die Regeneration im Axolotlorganismus zu treffen. Hierbei verglich ich die fotografischen Aufnahmen der Exemplare, welche mit dem BMP4 hemmenden Plasmidbestandteil pSuper-Noggin-M2 geimpft wurden, mit denen, welche den bloßen „empty vektor“, das pSuper-M2 Plasmid, in den Zellen trugen. Zur Unterscheidung der einzelnen Tiere trug eine Beschriftung der Becher, in denen sich die Axolotl befanden, bei. Dabei nahm ich drei verschiedene, mit Bindestrichen abgetrennte Ziffernkombinationen zu Hilfe. Die erste Gruppe stand für den Injektionsort. Hierbei gab es zwei Unterteilungen: „SC“ als Abkürzung des englischen Begriffs „spinal cord“ markierte die Becher, in welchen sich die Axolotl mit einer erhaltenen intrathekalen Injektion befanden. „M“ hingegen - eine Kurzbezeichnung für den englischen Begriff „muscle“ - bezeichnete die Becher der Axolotl, welche den Impfstoff in die Muskeln gespritzt bekamen. Die damit entstandene Zweiteilung der Axolotlzahl wurde durch die nächste Bezifferung weiter spezialisiert. Die Abkürzel „N“ beziehungsweise „M2“ richteten sich nach der Art des Injektionsgemisches, welches die Tiere erhielten. „N“ markierte hierbei die Becher, in welchen sich Exemplare mit dem pSuper-Noggin-M2 Plasmid in ihren Zellen befanden, die Tiere in den „M2“-Behältern enthielten die pSuper-M2 Plasmide in ihren Zellen. Römische Ziffern von I bis V gaben die Nummer des einzelnen Axolotls an und gewährleisteten mit den anderen beiden Abkürzungen eine eindeutige Kombination (z.B. SCN-III), um einer Verwechslung der 20 Exemplare vorzubeugen. 18 5.1 Exemplare mit intrathekal injiziertem pSuper-M2 Plasmid Sowohl nach fünf als auch nach acht Tagen entsprach der regenerierte Abschnitt des Schwanzes dem geradlinigen Verlauf des restlichen Körpers. Bei beiden Exemplaren p betrug die Länge des gesamten regenerierten Bereiches nach acht Tagen durchschnittlich 3200 μm, wobei das Rückenmark des Exemplars SC-M2-ΙV zirka 250 μm kürzer war als vom Exemplar SC-M2-V. q Dies ist darauf zurückzuführen, dass ich bei der Amputation keine einheitlichen Maße eingehalten hatte, jede Amputation verschieden schwere Wunden hinterlassen hatte und die Regeneration von Tier zu Tier unterschiedlich schnell ablief. Auffallend ist zudem, dass die fluoreszierenden Proteine aus den präparierten Rückenmarkszellen vereinzelt im Rückenmark des neugeschaffenen Schwanzabschnittes wiederzufinden waren. 5. 2 Exemplare mit intramuskulär injiziertem pSuper-M2 Plasmid Auch bei diesen zwei Axolotl wies der regenerierte Teil des Rückenmarks ein gerades Wachstum auf, was einen regenerierten Schwanzbereich von durchschnittlich 2900 μm umfasste. q Doch nur bei einem Exemplar, bei M-M2-IV, waren fluoreszierende Farben in Teilen vom neugebildeten Rückenmark und nebenliegende Muskelzellen zu finden. Dass diese Fluoreszenz nicht in den neugebildeten Zellen des Exemplars M-M2-V zu sehen war, liegt wahrscheinlich daran, dass ich die plasmidhaltigen Zellen bei der Amputation des Schwanzstückes nicht verletzt hatte und damit eine Beteiligung dieser Zelle an der Wiederherstellung des entfernten Körperteils unwahrscheinlich geworden war. r 5.3 Exemplare mit intrathekal injiziertem pSuper-Noggin-M2 Plasmid Jedes der fünf Axolotl aus dieser Versuchsreihe wies eine erfolgreiche Elektroporation auf. s Außerdem war zu erkennen, dass drei dieser Molche ein nach oben gekrümmtes etwa 2000 μm langes Rückenmark regenerierten. q Überdies zeigten diese Exemplare eine Deformation der Schwanzspitze. 19 Zum einen schloss diese Missbildung eine Überlappung des Flossensaums ein (SC-N-II und SC-N-V) ein, zum anderen wurde ein Stück Flossensaum ringförmig abgeschnürt, wie es bei dem Axolotl SC-N-I der Fall war. Der gesamte neugebildete Schwanzteil der fünf Axolotl hatte eine durchschnittliche Länge von 2500 μm und war mit fluoreszierenden Proteinen, q die aus dem injiziertem und in die Zellen hinein elektroporierten GFP-T2A-Cherry Plasmid synthetisiert worden, durchsetzt. Die zwei übrigen Tiere (SC-N-III und SC-N-IV) hatten dagegen ein ungefähr ebenso langes Rückenmark mit leichten Krümmungen aufgebaut, was jedoch zum größtem Teil dem geraden Verlauf des „alten“ Rückenmarks entsprach. 5.4 Exemplare mit intramuskulär injiziertem pSuper-Noggin-M2 Plasmid Bei diesen beiden Exemplaren betrug die durchschnittliche Länge des gesamten regenerierten Schwanzstückes 2800 μm. q Ebenso war bei einem Axolotl eine Abschnürung des Flossensaums in einer Ringform zu sehen. t Auf Grund der schlechten Qualität der Bilder war es schwierig, weitere exakte Aussagen über die abgelaufene Regeneration zu treffen. Die unscharfen Abschnitte - vor allem bei dem Axolotl M-N-II - ließen nicht erkennen, ob die sichtbaren Farben auf fluoreszierende, auf Grundlage des GFP-T2A-Cherry Plasmid synthetisierte Proteine basierten oder durch mir unbekannte Fremdpartikel hervorgerufen wurden. Es wäre sogar zu bedenken, ob aus den Bildern dieser beiden Exemplare deutliche Aussagen über die Regeneration des Axolotlschwanzes getroffen werden können. Das Fehlen von fluoreszierenden „Farbproteinen“ im nicht amputierten Bereich lässt sich darauf zurückführen, dass ich bei der Amputation die Zellen, welche die injizierten Plasmide beinhalteten, mit dem restlichen Schwanzteil unbeabsichtigt entfernt hatte. Somit waren diese Zellen nicht an der Wiederherstellung des Schwanzes beteiligt und es konnten keine Informationen für die Synthese von den fluoreszierenden „Frabproteinen“ bei der für die Regeneration notwendige Teilung weitergegeben werden. 20 5.5 Zusammengefasste Erkenntnisse Aus dem Ergebnis der Untersuchungen der Bilder lassen sich Aussagen über den vorhandenen Einfluss des BMP4 Proteins auf das Regenerationsvermögen des Axoltols im Bereich des Schwanzes ableiten. Dieses Protein trägt zum Wiederaufbau von verlorenen Schwanzstücken bei, da aus den Mikroskopaufnahmen hervorgeht, dass bei einer Hemmung des BMP4 Proteins durch den Inhibitor Noggin die Schwanzregeneration negativ beeinflusst wird. Diese unvorteilhafte Beeinflussung lässt sich im Vergleich zu der abgelaufenen Regeneration der vier Exemplare erklären, welche den „empty vektor“ - der keinerlei Einfluss auf den Axolotlorganismus hat - in die Zellen injiziert bekamen. So war der neugebildete Schwanzabschnitt der mit dem Noggin Plasmid injizierten Exemplare durchschnittlich um 300 μm kürzer und wies bei vier von sieben Exemplaren eine Hautwucherung beziehungsweise eine Missbildung des Flossensaums auf, was bei den BMP4-ungehemmten Axolotl nicht vorkam. Die Hemmung des BMP4 Proteins rief ein von dem geradlinigen Rückenmarksverlauf abweichendes Wachstum des regenerierten Rückenmarks bei sämtlichen sieben Exemplaren hervor. Doch können aus den Aufnahmen nicht nur die Erkenntnis des positiven Einflusses des BMP4 auf die Schwanzregeneration beim Axolotl abgeleitet werden, sondern sie lassen auch weitere Vermutungen über den Wiedereinstieg ausdifferenzierter Zellen in den Zellzyklus aufkommen. u Aus den Bildern lässt sich entnehmen, dass ausdifferenzierte Zellen, also Dauergewebszellen wie Muskel- und Nervenzellen, die sich zum Beispiel in unserem menschlichen Körper nicht mehr teilen können, sich im Axolotlorganismus vermehren und somit zur Regeneration beitragen. Einen Beleg für diesen Gedanken liefern die fluoreszierenden Farbproteine, welche sich sowohl in den Zellen befinden, in welche sie elektroporiert wurden, als auch in den neugebildeten Zellen des Schwanzes. Die genetische Information des GFP-T2A-Cherry Reporterplasmid muss bei der Zellteilung der ausdifferenzierten Zellen in die Zellen des regenerierten Abschnittes weitergegeben worden sein, denn in der Betrachtung am Fluoreszenzmikroskop sind an beiden Stellen, den „alten“ und den neu gebildeten Zellen, synthetisierte fluoreszierende „Farbproteine“ zu finden. 21 6 Danksagung Die zu meinen Untersuchungen notwendigen Experimente überwachte während meines Aufenthaltes am Max-Planck-Institut für molekulare Zellbiologie und Genetik Herr Philipp Weissert, ein angehender Doktor der Biologie. Mit sehr viel Ausdauer und Verständnis wies er mich in den Umgang mit den Geräten ein und stand mir bei jeder Frage und bei jedem Problem zur Seite. An dieser Stelle spreche ich ihm einen besonderen Dank aus, da er für mich sehr viel Zeit und Geduld aufbrachte und durch seine Arbeit meine Begeisterung für die Biologie intensivierte und das Studium der Biologie mein erstrebenswertes Hauptziel wurde. Dank auch meiner Biologielehrerin, Frau Wilhelm. Sie half mir auftretende Fragen zu klären, stellte mir Fachliteratur für meine Recherchen zur Verfügung und überwachte meine schriftlichen Ausführungen. Ebenfalls Dank Herrn Pamsch, der das gesamte Praktikum organisierte und Frau Elly Tanaka und ihrem Team. Sie ermöglichten mir einen Einblick in ihre Forschungen und integrierten mich vollständig in ihr angenehmes Arbeitsklima. 22 7 Quellenverzeichnis 1 http://www.dradio.de/aktuell/631390/ 2 http://www.organspende-und-transplantation.de/tag_der_organspende.htm 3 www.wikipedia.org/wiki/Azteken 4 http://www.axolotl-online.de/body_index.html 5 http://de.wikipedia.org/wiki/G%C3%B6tter_der_Azteken 6 Wistuba, Joachim: Axoltol. Natur und Tier – Verlag 2000, S. 58 7 ebd. S. 47 8 ebd. S. 48 9 ebd. S. 49 10 ebd. S. 50 11 ebd. S. 56 12 ebd. S. 58 13 ebd. S. 59 14 ebd. S. 60 15 ebd. S. 63 16 www.wikipedia.org/wiki/Bone_morphogenetic_protein 17 www.wikipedia.org/wiki/signalkaskade 18 Weiß, Dr. Joachim: Meyers Taschenlexikon Band 1. B.I.-Taschenbuchverlag 1999, S. 1594 19 http://de.wikipedia.org/wiki/Intrathekal 20 http://de.wikipedia.org/wiki/Elektroporation 21 http://de.wikipedia.org/wiki/Licht#Physiologie 23 8 Literaturverzeichnis Bayrhuber, Horst/ Kull, Ulrich: Linder Biologie. Hannover: Schroedel Verlag GmbH 21 1998 Brehme, Siegfried/ Meincke, Irmtraut: Wissensspeicher Biologie. Berlin: Volk-und-Wissen-Verlag 1 2005 Hafner, Lutz/ Hoff, Peter: Genetik. Hannover: Schroedel Schulbuchverlag 2000 Libbert, Eike: Allgemeine Biologie. Jena: VEB Gustav Fischer Verlag 5 1986 Probst, Wilfried/ Schuchardt, Petra: Abiturwissen Biologie. Mannheim: Dudenverlag 2004 Weber, Wilhelm/Sieve, Bernhard: Entwicklungsbiologie. Hannover: Schroedel Verlag 2002 Weber, Wilhelm/ Scharf, Karl-Heinz: Fortpflanzung und Entwicklung. Hannover: Schroedel Schulbuchverlag 1993 Weiß, Joachim: Meyers Taschenlexikon in 10 Bänden. Augsburg: Weltbild-Verlag 1999 Wistuba, Joachim: Axolotl. Münster: Natur-und-Tiere-Verlag 1 2000 Wolpert, Lewis: Principles of Development. New York: Oxford University 2 2002 24 9 Selbstständigkeitserklärung Hiermit erkläre ich, dass ich die vorliegende Arbeit selbstständig und ohne fremde Hilfe verfasst und keine anderen Hilfsmittel als angegeben verwendet habe. Insbesondere versichere ich, dass ich alle wörtlichen und sinngemäßen Übernahmen aus anderen Werken als solche kenntlich gemacht habe. Riesa, 03.03.2008 25 10 Anlagenverzeichnis a Max-Planck-Institut für molekulare Zellbiologie und Genetik Dresden, S. 3 b Axolotl wildfarben, S. 4 c Axolotl leukistisch, S. 4 26 d Eines meiner untersuchten Axolotl in seinem Trinkbecher, mit Futter, S. 4 e Lage des Xochimilcosees in Mexico, S. 5 27 f Rückgang des Xochimilcosees und Expansion der Stadt Mexico City, S. 5 28 29 g Injektionsmikroskop, S. 13 mit h Injektionsnadelhalterung am Injektionsmikroskop, S. 13 i Elektroporator, S. 14 i h j manuelle Mikroliterpipette mit aufgesetzter Kunststoff Pipettenspitze, S. 12 f. 30 k Daten zur Elektroporation, S. 14 Set up Voltage Pulse Length Pulses Interval Polarity l Fluoreszenzmikroskop, S. 15 15 V 50 ms 5 100 ms unipolar 31 m Dauer der Belichtung plasmidhaltigen Zellen, S. 15 4.7.2007, am Tag der Elektroporation Anregung der Fluoreszenz in ms: Exemplar: RFP GFP 32 SC-N-Ι 1000 2000 SC-N-ΙΙ 1000 4000 SC-N-ΙΙΙ 700 10000 SC-N-ΙV 2000 3000 SC-N-V 4000 4000 SC-M2-Ι / / SC-M2-ΙΙ / / SC-M2-ΙΙΙ / / SC-M2-ΙV 3000 8000 SC-M2-V 250 2000 M-N-Ι 2000 8000 M-N-ΙΙ 3000 10000 M-N-ΙΙΙ / / M-N-ΙV / / M-N-V / / M-M2-Ι / / M-M2-ΙΙ / / M-M2-ΙΙΙ / / M-M2-ΙV 800 3000 M-M2-V 2000 1500 /… Exemplare, bei welchen ich keine Fluoreszenz im red- beziehungsweise green-Channel feststellen konnte und damit für die weiteren Untersuchungen ausschieden 5.7.2007, ein Tag nach der Elektroporation Anregung der Fluoreszenz in ms: RFP GFP 1000 2000 Exemplar: SC-N-Ι 33 SC-N-ΙΙ 1000 4000 SC-N-ΙΙΙ 2500 10000 SC-N-ΙV 550 2500 SC-N-V 2000 10000 SC-M2-Ι / / SC-M2-ΙΙ / / SC-M2-ΙΙΙ / / SC-M2-ΙV 1000 3000 SC-M2-V 450 3000 M-N-Ι 1000 3000 M-N-ΙΙ 1000 5000 M-N-ΙΙΙ / / M-N-ΙV / / M-N-V / / M-M2-Ι / / M-M2-ΙΙ / / M-M2-ΙΙΙ / / M-M2-ΙV 500 1500 M-M2-V 700 3000 /… Exemplare, bei welchen ich keine Fluoreszenz im red- beziehungsweise green-Channel feststellen konnte und damit für die weiteren Untersuchungen ausschieden 6.7.2007, zwei Tage nach der Elektroporation Anregung der Fluoreszenz in ms: RFP GFP 1000 6000 Exemplar: SC-N-Ι 34 SC-N-ΙΙ 1000 5000 SC-N-ΙΙΙ 900 5000 SC-N-ΙV 400 2000 SC-N-V 2000 8000 SC-M2-Ι / / SC-M2-ΙΙ / / SC-M2-ΙΙΙ / / SC-M2-ΙV 300 6000 SC-M2-V 150 2000 M-N-Ι 250 1500 M-N-ΙΙ 2500 8000 M-N-ΙΙΙ / / M-N-ΙV / / M-N-V / / M-M2-Ι / / M-M2-ΙΙ / / M-M2-ΙΙΙ / / M-M2-ΙV 250 1000 M-M2-V 1000 5000 /… Exemplare, bei welchen ich keine Fluoreszenz im red- beziehungsweise green-Channel feststellen konnte und damit für die weiteren Untersuchungen ausschieden 9.7.2007, fünf Tage nach der Elektroporation Anregung der Fluoreszenz in ms: RFP GFP Exemplar: a, b, c, d, a, b, c, d, 35 SC-N-Ι 300 500 1000 1000 2000 5000 SC-N-ΙΙ 1000 1000 900 SC-N-ΙΙΙ 200 2000 2000 1000 8000 6000 SC-N-ΙV 800 1250 300 2000 4000 8000 SC-N-V 2000 2000 2000 900 3000 5000 4000 4000 5000 4000 6000 SC-M2-Ι / / SC-M2-ΙΙ / / SC-M2-ΙΙΙ / / SC-M2-ΙV 250 200 300 SC-M2-V 100 1500 1500 1000 250 M-N-Ι 100 2000 1000 5000 M-N-ΙΙ 2000 1000 5000 4000 M-N-ΙΙΙ / / M-N-ΙV / / M-N-V 2000 1500 1000 4000 5000 8000 / / M-M2-Ι / / M-M2-ΙΙ / / M-M2-ΙΙΙ / / M-M2-ΙV 200 500 150 M-M2-V 1000 4000 4000 800 600 300 4000 5000 8000 /… Exemplare, bei welchen ich keine Fluoreszenz im red- beziehungsweise green-Channel feststellen konnte und damit für die weiteren Untersuchungen ausschieden 11.7.2007, sieben Tage nach der Elektroporation Anregung der Fluoreszenz in ms: RFP GFP Exemplar: a, b, c, d, a, b, c, d, 36 SC-N-Ι 400 400 500 1300 1300 2000 SC-N-ΙΙ 600 900 1000 2500 3000 3000 4000 8000 SC-N-ΙΙΙ 600 2500 4000 2500 SC-N-ΙV 1000 2000 2200 500 5000 6000 6000 1500 SC-N-V 2000 1000 1500 800 500 8000 10000 12000 6000 6200 SC-M2-Ι / / SC-M2-ΙΙ / / SC-M2-ΙΙΙ / / SC-M2-ΙV 300 300 800 500 2000 2000 1000 1000 SC-M2-V 250 1000 2000 1000 3000 5500 M-N-Ι 100 800 2000 1000 3500 6000 M-N-ΙΙ 1800 3000 1000 8000 10000 8000 M-N-ΙΙΙ / / M-N-ΙV / / M-N-V / / M-M2-Ι / / M-M2-ΙΙ / / M-M2-ΙΙΙ / / M-M2-ΙV 500 800 800 M-M2-V 1000 2000 3500 800 1500 1500 6000 8000 12000 /… Exemplare, bei welchen ich keine Fluoreszenz im red- beziehungsweise green-Channel feststellen konnte und damit für die weiteren Untersuchungen ausschieden n Daten zur zweiten Elektroporation, S. 16 Set up Voltage 30 V Pulse Length 50 ms Pulses 5 Interval 100 ms Polarity unipolar 37 o Einstellungen am Fluoreszenzmikroskop für das Programm MetaVue, S. 17 Oberes DIC = 0 Unteres DIC = 30 p Exemplare mit intrathekal injiziertem pSuper-M2 Plasmid, S. 18 Exemplar SC-M2-IV, regenerierter Schwanzteil fünf Tage nach der Amputation 38 amputation plane Exemplar SC-M2-IV, regenerierter Schwanzteil acht Tage nach der Amputation a.p. 39 Exemplar SC-M2-V, regenerierter Schwanzteil fünf Tage nach der Amputation a.p. Exemplar SC-M2-V, regenerierter Schwanzteil acht Tage nach der Amputation a.p. 40 q Länge der regenerierten Bereiche, S. 18 ff. gerundete Länge des regenerierten Schwanzteils in μm: nach 5 Tagen nach 8 Tagen Exemplar: SC-N-Ι SC-N-ΙΙ SC-N-ΙΙΙ SC-N-ΙV SC-N-V SC-M2-Ι SC-M2-ΙΙ SC-M2-ΙΙΙ SC-M2-ΙV SC-M2-V M-N-Ι M-N-ΙΙ M-N-ΙΙΙ M-N-ΙV M-N-V M-M2-Ι M-M2-ΙΙ M-M2-ΙΙΙ M-M2-ΙV M-M2-V Rückenmark Schwanz Rückenmark Schwanz 1167 1167 1250 1667 1300 2000 2000 2125 2000 1500 1667 2083 1833 1917 2200 / / / 2400 2750 2875 2500 2250 / / / 1875 1250 3000 2000 2250 2500 3250 3125 1143 1000 1786 1571 1800 2500 2200 3500 / / / / / / / / / 1143 800 / / / 1714 2000 /... aus der Untersuchung entfallene Exemplare 1700 2750 2300 3500 41 r Exemplare mit intramuskulär injiziertem pSuper-M2 Plasmid, S. 18 Exemplar M-M2-IV, regenerierter Schwanzteil fünf Tage nach der Amputation a.p. Exemplar M-M2-IV, regenerierter Schwanzteil acht Tage nach der Amputation a.p. 42 Exemplar M-M2-V, regenerierter Schwanzteil fünf Tage nach der Amputation a.p. Exemplar M-M2-V, regenerierter Schwanzteil acht Tage nach der Amputation a.p. 43 s Exemplare mit intrathekal injiziertem pSuper-Noggin-M2 Plasmid, S. 18 Exemplar SC-N-I, regenerierter Schwanzteil fünf Tage nach der Amputation a.p. Exemplar SC-N-I, regenerierter Schwanzteil acht Tage nach der Amputation 44 a.p. Exemplar SC-N-II, regenerierter Schwanzteil fünf Tage nach der Amputation a.p. 45 Exemplar SC-N-II, regenerierter Schwanzteil acht Tage nach der Amputation a.p. Exemplar SC-N-III, regenerierter Schwanzteil fünf Tage nach der Amputation 46 a.p. Exemplar SC-N-III, regenerierter Schwanzteil acht Tage nach der Amputation a.p. Exemplar SC-N-IV, regenerierter Schwanzteil fünf Tage nach der Amputation 47 a.p. Exemplar SC-N-IV, regenerierter Schwanzteil acht Tage nach der Amputation a.p. 48 Exemplar SC-N-V, regenerierter Schwanzteil fünf Tage nach der Amputation a.p. Exemplar SC-N-V, regenerierter Schwanzteil acht Tage nach der Amputation a.p. 49 t Exemplare mit intramuskulär injiziertem pSuper-Noggin-M2 Plasmid, S. 19 Exemplar M-N-I, regenerierter Schwanzteil fünf Tage nach der Amputation a.p. M-N-I, regenerierter Schwanzteil acht Tage nach der Amputation 50 a.p. Exemplar M-N-II, regenerierter Schwanzteil fünf Tage nach der Amputation a.p. 51 M-N-II, regenerierter Schwanzteil acht Tage nach der Amputation a.p. u Vereinfachte Darstellung des Zellzyklus, S. 20 52 53 11 Bildnachweis a http://www.mpi-cbg.de/research/building.html b http://www.ambystoma.de/index.html c http://de.wikipedia.org/wiki/Axolotl d Foto: Renneberg, Claudia e Wistuba, Joachim: Axoltol. Natur und Tier – Verlag 2000, S. 7 f ebd. S. 6 g Foto: Renneberg, Claudia h ebd. i ebd. j http://de.wikipedia.org/wiki/Pipette p Foto: Renneberg, Claudia. Fluoreszenzmikroskop, Programm: MetaVue r ebd. s ebd. t ebd. u Modell: Renneberg, Claudia