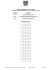Critérios para revisão de lâminas de extensão
Transcrição
Critérios para revisão de lâminas de extensão
Critérios para revisão de lâminas de extensão do sangue Publicações Comentadas Com os avanços da automação em hematologia e a possibilidade da realização da contagem diferencial leucocitária pelos equipamentos hematológicos, uma questão sempre presente refere-se à necessidade ou não da revisão microscópica das lâminas de extensão sanguínea. Ou, mais especificamente, quais os critérios que o laboratório deve adotar como indicativos da necessidade dessa revisão? O texto aqui apresentado, de autoria de Gen Gulati, Jinming Song, Alina Dulau Florea e Jerald Gong, publicado no Annals of Laboratory Medicine, aborda o assunto de maneira bastante prática e sugere diferentes maneiras de analisar o sangue à microscopia, dependendo das alterações reportadas pelo equipamento hematológico. As considerações dos autores não refletem necessariamente o parecer do tradutor ou da Sysmex, mas são bastante interessantes e merecem uma avaliação crítica do leitor, podendo ser valiosas para a aplicação na sua rotina laboratorial. Ann Lab Med. 2013 Jan;33(1):1-7. English. Published online 2012 December 17 . http://dx.doi.org/10.3343/alm.2013.33.1.1 Purpose and Criteria for Blood Smear Scan, Blood Smear Examination, and Blood Smear Review Gene Gulati, Ph.D., Jinming Song, M.D. , Alina Dulau Florea, M.D. and Jerald Gong, M.D. Department of Pathology, Anatomy, and Cell Biology, Jefferson Medical College and Thomas Jefferson University Hospital, Philadelphia, USA. “Propósitos e critérios para escanear, examinar e revisar as lâminas de extensão do sangue”. A despeito da capacidade da maioria dos equipamentos hematológicos realizarem de maneira eficiente e precisa as contagens global e diferencial de células, a análise microscópica do sangue por um profissional habilitado ainda é necessária em várias circunstâncias e por diversas razões. O presente artigo é dedicado à definição e delineamento das razões e critérios para 3 tipos de análise do esfregaço ou extensão sanguínea: uma que se limita a um escaneamento da lâmina, a segunda que compreende a análise completa do sangue com contagem diferencial manual e a terceira que seria uma revisão da lâmina e dos resultados encontrados previamente por outro analisador. Os três tipos de avaliação da extensão sanguínea 1. Escaneamento da lâmina (EL) Sinônimos: escaneamento das plaquetas, estimativa plaquetária, análise da lâmina sem a contagem diferencial de leucócitos (DIFF). Quando é feita: • Para verificar a contagem automática das plaquetas: presença de alarmes ou contagem muito reduzida. • Muitos laboratórios optam por fazer essa verificação quando a contagem de plaquetas é < 100x109/L num paciente desconhecido (1ª coleta) ou quando o delta-check é ≥ 50% da contagem anterior. • Pseudo-trombocitopenia pode resultar numa contagem < 100x109/L, o que pode levar em condutas desnecessárias, como consultas com hematologista, adiamento de cirurgia ou novas coletas de sangue. • Verificação de alarmes das outras linhagens celulares, como a presença de blastos, células atípicas, granulócitos imaturos, e desvio à esquerda. • Verificar se a contagem diferencial acompanhada de alarmes requer a contagem manual. Como verificar a contagem de plaquetas: - examinar toda a extensão, incluindo as bordas da lâmina e as áreas mais finas com o aumento de 10X, procurando por grumos de plaquetas. Para grumos menores o aumento de 40X é recomendado. - observar a presença de fragmentos de hemácias, bactérias ou fungos que podem causar falsas plaquetoses, e plaquetas gigantes que podem resultar em falsas plaquetopenias. Como relatar em casos de grumos: Muitas vezes as contagens não são reportáveis e uma descrição qualitativa pode ser feita, como “aparentemente normal/alta ou baixa, com presença de grumos”. Como obter uma contagem confiável na amostra com grumos de plaquetas: - uso de vortex em alta velocidade, o que pode resolver em cerca de 50% dos casos. - colher nova amostra com citrato, que resolve cerca de 90% dos casos. Como proceder se o escaneamento da lâmina revelar a presença de células imaturas/anormais/atípicas: Em geral já está estabelecido pelos laboratórios que a contagem diferencial manual deve ser feita e os resultados devem substituir a contagem automatizada. - somente 1 célula suspeita: deve ou não ser feita a revisão de lâmina??? Na opinião dos autores se for o primeiro hemograma e se a célula for claramente identificada ou suspeita de ser um blasto, hairy-cell, ou célula de mieloma, deve ser feita a revisão manual. Na presença de outros tipos de células imaturas/atípicas ou anormais, os laboratórios podem definir a partir de quantas dessas células será indicada a contagem diferencial manual. - observar se outras alterações morfológicas estão presentes. 2. Exame da extensão sanguínea (EES) Sinônimos: diferencial manual, DIFF Inclui: diferencial de leucócitos (em geral 100 células são contadas) e avaliação da morfologia das séries vermelha, branca e plaquetária. - verificação de alarmes - estimativa da contagem de plaquetas Critérios para o DIFF manual: cada laboratório deve estabelecer seus próprios critérios de EES, baseados nos seguintes aspectos: - tipo de população atendida (maioria dos pacientes internos ou externos, grau de complexidade dos procedimentos, etc) - significado clínico das anormalidades relatadas pelo equipamento de automação tanto nas contagens globais como na contagem diferencial - capacidade do sistema utilizado em emitir alarmes confiáveis - volume de exames realizados - nível de capacitação do pessoal técnico A tabela mostrando os critérios adotados pelo “Clinical Hematology Laboratory at Thomas Jefferson University Hospital” para Escaneamento da lâmina (Blood Smear Scan – BSS) e/ou Exame da extensão sanguínea (EES) pode ser vista no link: http://dx.doi.org/10.3343/alm.2013.33.1.1 Do ponto de vista clínico o exame da extensão sanguínea tem 3 objetivos principais: 1. Servir como controle de qualidade dos resultados gerados pela automação 2. Identificar células atípicas/anormais 3. Reconhecer alterações morfológicas que o equipamento não é capaz de detectar, como: - na série vermelha: eliptócitos, células em alvo, hemácias falcizadas, acantócitos, equinócitos, cristalóides SC, estomatócitos, hemácias em gota, rouleaux, corpúsculos de Howell-Jolly, corpos de Pappenheimer, granulações basofílicas, organismos intracelulares, etc. - na série branca: bastonetes de Auer, granulações tóxicas, corpos de Döhle, granulócitos hipo ou agranulares, organismos intraleucocitários. - na série plaquetária: satelitismo plaquetário, granulação anormal, plaquetas bizarras hipo ou agranulares. Como fazer o exame de extensão sanguínea: • Exame panorâmico de toda a extensão, com objetiva de 10X: observar qualidade da coloração, presença de grumos plaquetários, hemácias e leucócitos; presença de organismos extra-celulares (como filária); crioprecipitado; formação de rouleaux e filamentos de fibrina. • Aumento de 100x: para confirmar as alterações observadas no aumento de 10X. • Grumos leucocitários: não são frequentes e geralmente estão associados com condições infecciosas (em geral grumos neutrofílicos) e/ou doenças linfoproliferativas – podem causar falsas leucopenias. Para tentar desfazer esses grumos pode-se colocar a amostra em BM a 37°C por 10 a 15 minutos ou colocar no vortex por 1-2 minutos em alta velocidade e repassar no aparelho. Pode também fazer nova coleta de sangue usando tubo de citrato (tampa azul) e multiplicar o resultado de leucócitos por 1.1. É recomendável colocar uma observação sobre a presença de grumos. • Aglutinação de hemácias: indica a presença de aglutinina a frio; causa uma falsa elevação do HCM, CHCM e VCM, e uma falsa redução na contagem de hemácias e hematócrito. O aquecimento da amostra a 37°C por 10-15 minutos pode corrigir os resultados. • Crioproteinemia: pode estar associada com contagens falsamente elevadas de leucócitos e/ou plaquetas. A pré-incubação a 37°C por 10-15 min pode produzir resultados confiáveis. • Formação de rouleaux: indica altos níveis de fibrinogênio e/ou globulinas. Associada a condições inflamatórias ou infecciosas, benignas ou malignas, como mieloma múltiplo ou macroglobulinemia. • Restos de fibrina: integridade da amostra é questionável. Deve ser solicitado novo material. • Leucócitos lesados ou degenerados, onde a membrana celular está ausente e são vistos somente os núcleos, são sugestivos de hiperlipidemia, que pode causar aumento da Hb, HCM e CHCM. Possível correção da hiperlipidemia: centrifugar a amostra e substituir o plasma por igual volume de diluente isotônico e repetir a contagem. Como fazer a contagem diferencial manual: Em geral 100 leucócitos são contados e separados por tipos celulares. Contagens inferiores ou superiores a 100 podem ser necessárias dependendo da contagem global de leucócitos. A contagem deve ser reportada em números relativos e absolutos. A contagem em números absolutos é em geral considerada mais valiosa porque reflete um aumento ou diminuição reais ou verdadeiros de cada tipo celular e não as alterações de uma série em relação às outras. Avaliação morfológica da série vermelha: não existe consenso em como e o que reportar referente as alterações morfológicas da série vermelha. Alguns exemplos de formas de relatar essas alterações: anormalidade presente ou ausente; graduação da anormalidade como leve, moderada ou grave; de 1+ a 4+. Em algumas situações a graduação pode ser importante, como: uma marcada eliptocitose, reportada como 3+ ou 4+ pode ser indicativa de eliptocitose hereditária, enquanto a “presença de eliptócitos” é um dado não-específico, que pode aparecer em diversos outros tipos de anemia. O mesmo vale para os dacriócitos ou hemácias em forma de gota. Grande quantidade dessas células está associada à fibrose da medula óssea, enquanto alguns eventos podem ocorrer na anemia ferropriva ou anemia renal, entre outras. Uma recente publicação da American Society for Clinical Pathology Press apresenta uma sistematização sobre a descrição das alterações morfológicas das séries vermelha, branca e plaquetária (Gulati G et al. Blood cell morphology grading guide.Chicago ASCP Press, 2009:1:85). Outras descrições: - presença de organismos intra/extra-celulares; - células malignas não-hematológicas - estimativa qualitativa das plaquetas: contagem normal/aumentada ou reduzida. Finalização: Após o exame da extensão sanguníea será determinado se há ou não necessidade de uma revisão (descrita a seguir) e/ou interpretação por um hematomorfologista e/ou patologista. 3. Revisão da extensão sanguínea (RES): Sinônimos: interpretação da extensão sanguínea, revisão médica da extensão sanguínea. Pode ser requisita pelo clínico ou indicada pelo pessoal do laboratório que realizou os 2 tipos anteriores de análise da lâmina. Pode ser feita com ou sem interpretação dos resultados. Indicações clínicas para a RES: a) anemia, trombocitopenia e/ou leucopenia inexplicadas b) suspeita de anemia hemolítica tombocitopênica, coagulação intravascular disseminada, etc c) hemoglobinopatia (SS, SC, CC, etc), talassemia, membranopatia (esferocitose hereditária, eliptocitose hereditária, etc) d) doença linfoproliferativa, discrasia de células plasmáticas, mielofibrose, síndrome mielodisplásica e) infecção parasitária f) mononucleose infecciosa g) doença leucocitária hereditária (Pelger huet, May-Hegglin, etc) h) doença plaquetária hereditária (síndrome da plaqueta cinza). Quem realiza a RES: Um profissional com experiência em morfologia em células sanguíneas pode estar qualificado como revisor para confirmação dos achados previamente observados. Entretanto, um hematologista, hematopatologista ou patologista clínico com treinamento e experiência em morfologia hematologia está mais capacitado para interpretar os achados da extensão sanguínea associando-os a outras informações clínicas e laboratoriais existentes. A tabela a seguir mostra os critérios adotados pelo Thomas Jefferson University Hospital indicativos da necessidade de revisão das lâminas: Tabela 2 Critérios para revisão de esfregaço do sangue no Thomas Jefferson University Hospital Adultos A. Baseados no CBC WBC (x109/L) RBC (x1012/L) Hb (g/dL) (mmol/L) PLT (x109/L) MCY (fL) B. Baseados no diferencial automático (x109/L) Linfócitos Monócitos Eosinófilos Basófilos C. Baseados no diferencial manual Blastos ou outras anomalidades/células não identificadas Promielócitos Mielócitos Metamielócitos Linfócitos atípicos NRBC (por 100 WBC) Parasitas Início* Início Início Início Início Pediátrico > 30 > 6.0 (Mulher) ou > 6.5 (Homem) ≤ 6 ou > 18 < 14 (RN) ≤ 3.7 ou > 11.2 < 50 ou > 999 < 60 ou > 110 < 85 (RN) Início Início Início Início > 7 (> 14 anos) > 10 (1-14 anos) > 3 (> 7 dias) >2 > 0.5 > 14 (< 1 ano) Início Início Início Início Início Todos ≥ 3% ≥ 5% ≥ 10% ≥ 10% maior que 2 (> 7 dias) Maior que 50 (< 7 dias) Todos D. Pedidos do médico * Início: primeiro esfregaço de um novo paciente internado ou eventual consulta ambulatorial. Abreviações: CBC: hemograma completo; WBC: glóbulos brancos; RBC: hemácias; PLT: plaquetas; MCV: volume corpuscular médio; DIFF: contagem diferencial leucocitária; NRBC: eritoblastos. As tabelas originais podem ser vistas no link: http://dx.doi.org/10.3343/alm.2013.33.1.1 Importante: a lista de critérios para a revisão de lâmina é usualmente desenvolvida pelos laboratórios e pode ser revista periodicamente. Fatores que podem determinar esses critérios: - tipo de população de pacientes atendida - algum tipo específico de paciente ou doença que seja do interesse dos clínicos - treino e experiência dos examinadores - volume de amostras processadas pelo laboratório - regras do programa de qualidade do serviço - considerações educacionais ou científicas. Publicações referentes ao assunto podem ser consultadas pelos laboratórios como ponto de partida no desenvolvimento dos critérios próprios de cada serviço. As referências abaixo relatam alguns dados da literatura: 1. Javidian P, Garshelis L, Peterson P. Pathologist review of the peripheral film. A mandatory quality assurance activity. Clin Lab Med 1993;13:853–861. 2. Peterson P, Blomberg DJ, Rabinovitch A, Cornbleet PJ. Physician review of the peripheral blood smear: when and why-an opinion. Lab Hematol 2001;7:175–179. 3. Gulati GL, Alomari M, Kochar W, Schwarting R. Critera for blood smear review. Lab Med 2002;33:374–377. 4. Sandhaus LM, Wald DN, Sauder KJ, Steele EL, Meyerson HJ. Measuring the clinical impact of pathologist reviews of blood and body fluid smears. Arch Pathol Lab Med 2007;131:468–472. A revisão da lâmina por um hematomorfologista qualificado possibilita que: - seja assegurada a qualidade das contagens global, diferencial e dos reticulócitos. - a interpretação conjunta do resultado do hemograma com outros exames laboratoriais pode definir melhor o diagnóstico e sugerir estratégias futuras com eficiência e redução de custos. - atividades de estudo, treinamento e reciclagem de estudantes, residentes e do pessoal do laboratório sejam desenvolvidas. Diferentemente dos processos de escaneamento da lâmina (EL) e exame da extensão sanguínea (EES), na revisão da lâmina (RES) a contagem diferencial de leucócitos só deve ser realizada pelo revisor quando: a) a revisão está sendo feita para um teste de controle de qualidade ou para avaliar a competência dos outros profissionais do serviço; b) se o revisor considerar a contagem feita anteriormente por outro examinador como sendo incompleta, incorreta ou contendo alguma célula não identificada relatada como “outras células”. Comentário do tradutor: gostaríamos de saber como você procede no seu laboratório quanto à liberação automática dos hemogramas pelos equipamentos de automação. Quais os critérios utilizados como indicativos da revisão microscópica da extensão sanguínea pelo seu laboratório? Envie seus comentários e/ou dúvidas para nossa assessoria científica Profa. Dra. Helena Z. W. Grotto Consultora médica Sysmex América Latina e Caribe [email protected] We Believe the Possibilities Publicado por Sysmex América Latina e Caribe Rua do Paraíso, 148 - Paraíso/SP - 04103-000, Brasil www.sysmex.com/la Tel. +55(11) 3145-4300