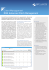
Entwicklung von Real-Time PCR Nachweissystemen
Transcrição
Entwicklung von Real-Time PCR Nachweissystemen
Entwicklung von Real-Time PCR Nachweissystemen für getränkerelevante Hefen vorgelegt von Diplom-Ingenieur Hans-Henno Dörries Angefertigt bei der Firma BIOTECON Diagnostics GmbH in Potsdam Von der Fakultät III - Prozesswissenschaften der Technischen Universität Berlin zur Erlangung des akademischen Grades Doktor der Ingenieurwissenschaften - Dr.-Ing. - genehmigte Dissertation Vorsitzender: Prof. Dr. rer. nat. L. Kroh Berichter: Prof. Dipl.-Ing. Dr. U. Stahl Berichterin: Dr.-Ing. K. Berghof-Jäger Tag der wissenschaftlichen Aussprache: 01.03.2006 Berlin 2006 D 83 Danksagung Mein besonderer Dank gilt Herrn Prof. Dipl.-Ing. Dr. Ulf Stahl für die wissenschaftliche Betreuung und Unterstützung beim Erstellen dieser Arbeit. Frau Dr. Kornelia Berghof-Jäger danke ich für die hevorragende Unterstützung und die ununterbrochene Begeisterung für alle Ergebnisse dieser Arbeit. Herrn Dr. Cordt Grönewald und Herrn Dr. Thomas Zippel möchte ich für ihre Hilfe bei der Lösung von praktischen Problemen, für wertvolle Anregungen und ihre ständige Diskussionsbereitschaft danken. Ivonne Remus danke ich für die tatkräftige Unterstützung bei einigen der durchgeführten Versuche. Ganz besonders danke ich Jana Kohlmann für die große Geduld und die Unterstützung bei der Anfertigung der schriftlichen Arbeit. Herrn Dipl. Biol. Benjamin Junge danke ich für die kritische Durchsicht dieser Arbeit. Allen Mitarbeitern der Firma BIOTECON Diagnostics GmbH danke ich für die Hilfsbereitschaft und angenehme Arbeitsatmosphäre. II Inhaltsverzeichnis Inhaltsverzeichnis Abbildungsverzeichnis .......................................................................................... VI Tabellenverzeichnis .............................................................................................. VII Abkürzungsverzeichnis ......................................................................................... IX Zusammenfassung................................................................................................ XII 1 Einleitung ..................................................................................................................1 1.1 Getränkerelevante Hefen .........................................................................................1 1.1.1 Alkoholfreie Getränke ..............................................................................................2 1.1.2 Bier ............................................................................................................................5 1.1.3 Wein...........................................................................................................................6 1.2 Nachweis und Identifizierung von getränkerelevanten Hefen .............................7 1.2.1 Kultivierungsabhängiger Nachweis........................................................................8 1.2.2 Mikroskopie, Durchflusszytometrie und Immunoassay .....................................10 1.2.3 Elektrometrische Methoden und ATP-Messung..................................................12 1.2.4 Phänotypische Identifizierung ..............................................................................13 1.2.5 Konventionelle, PCR-basierte Methoden .............................................................13 1.2.6 Real-Time PCR-Methoden .....................................................................................17 1.3 Ziele der Arbeit .......................................................................................................18 2 Material und Methoden ..........................................................................................19 2.1 Mikroorganismen ...................................................................................................19 2.2 Nährmedien.............................................................................................................22 2.3 Oligonucleotide ......................................................................................................24 2.4 Probenmatrices ......................................................................................................26 2.5 Anzucht von Mikroorganismen .............................................................................27 2.6 Extraktion von Nucleinsäuren...............................................................................27 2.6.1 Mechanisch/thermische DNA-Extraktion .............................................................27 2.6.2 Extraktion quantifizierbarer und RNA-freier DNA ...............................................27 2.6.3 Erweiterte, mechanisch/thermische DNA-Extraktion..........................................27 2.7 Konzentrationsbestimmung von DNA-Lösungen ...............................................28 2.7.1 Fluorometrische Bestimmung...............................................................................28 2.7.2 Konzentrationsbestimmung über Absorptionsspektrometrie ...........................28 2.8 Agarosegelelektrophorese ....................................................................................28 2.9 Klonierung von PCR-Fragmenten.........................................................................29 2.9.1 Erzeugung von PCR-Fragmenten für die Klonierung .........................................29 2.9.1.1 EF-3-Gen Fragmente ..............................................................................................29 2.9.1.2 Interne Amplifikationskontrolle und Positivkontrolle .........................................30 2.9.2 Reinigung von PCR-Fragmenten für die Klonierung ..........................................31 III Inhaltsverzeichnis 2.9.3 Ligation von gereinigten DNA-Fragmenten .........................................................31 2.9.4 Transformation von E. coli Zellen.........................................................................31 2.9.4.1 Herstellung kompetenter E. coli Zellen ................................................................31 2.9.4.2 Transformationsansatz ..........................................................................................31 2.9.4.3 Kontrolle der Transformation................................................................................31 2.9.5 Präparation von Plasmid-DNA ..............................................................................32 2.9.6 Restriktionsverdau von Plasmid-DNA..................................................................32 2.10 Sequenzierung........................................................................................................32 2.11 Sequenzanalyse .....................................................................................................32 2.12 Zellzahlbestimmung ...............................................................................................32 2.13 Real-Time LightCycler® PCR .................................................................................33 2.13.1 Real-Time LightCycler® PCR-Programme ............................................................33 2.13.1.1 S. cerevisiae var. diastaticus Nachweis mit Hybridisierungssonden ...............33 2.13.1.2 Hefegesamtnachweis mit Hybridisierungssonden .............................................34 2.13.1.3 Hefegesamtnachweis mit SYBR®-Green I ............................................................34 2.13.2 Real-Time PCR-Ansätze.........................................................................................35 2.13.2.1 S. cerevisiae var. diastaticus Nachweis mit Hybridisierungssonden ...............35 2.13.2.2 Hefegesamtnachweis mit Hybridisierungssonden .............................................35 2.13.2.3 Hefegesamtnachweis mit SYBR®-Green I ............................................................36 2.14 Spezifitätstestung der Real-Time LightCycler® PCR...........................................36 2.15 Sensitivitätstestung der Real-Time LightCycler® PCR .......................................36 2.15.1 Sensitivität ermittelt mit quantifizierter, RNA-freier DNA ...................................36 2.15.2 Sensitivität ermittelt mit dotierten Probenmatrices ............................................36 2.15.3 Sensitivität ermittelt bei einer hohen Begleitflora...............................................36 2.16 Praxisnahe Testung der Real-Time PCR für S. cerevisiae var. diastaticus ......37 3 Ergebnisse ..............................................................................................................38 3.1 Entwicklung einer Real-Time PCR für S. cerevisiae var. diastaticus ................38 3.1.1 Auswahl der STA1-3 Gene als Zielregionen ........................................................38 3.1.2 Anordnung der Primer und Hybridisierungssonden im STA Gen .....................39 3.1.3 Konstruktion der internen Amplifikationskontrolle und der Positivkontrolle ..40 3.1.4 Spezifität der Real-Time PCR für S. cerevisiae var. diastaticus ........................42 3.1.5 Sensitivität der Real-Time PCR für S. cerevisiae var. diastaticus .....................45 3.1.6 Kompatibilität der Real-Time PCR für S. cerevisiae var. diastaticus mit unterschiedlichen Probenmatrices.......................................................................48 3.1.7 Anwendbarkeit der Real-Time PCR für S. cerevisiae var. diastaticus in der Praxis.......................................................................................................................49 3.1.7.1 Versuchsteil 1: Robustheit ....................................................................................49 3.1.7.2 Versuchsteil 2: Spezifität .......................................................................................51 3.1.7.3 Versuchsteil 3: Sensitivität....................................................................................51 IV Inhaltsverzeichnis 3.2 Entwicklung einer Real-Time Consensus-PCR für Hefen...................................53 3.2.1 Auswahl des EF-3 Gens als Zielregion ................................................................53 3.2.2 Sequenzierung und Alignment des EF-3 Genbereichs.......................................54 3.2.3 Sequenzvergleich des EF-3 Genbereichs ............................................................55 3.2.4 Anordnung der Primer und Hybridisierungssonden im EF-3 Gen ....................57 3.2.4.1 Real-Time Consensus-PCR für Hefen mit SYBR®-Green I..................................58 3.2.4.2 Real-Time Consensus-PCR für Hefen mit Hybridisierungssonden...................58 3.2.5 Konstruktion der internen Amplifikationskontrolle und der Positivkontrolle ..59 3.2.6 Spezifität und Auswahl des Detektionssystems .................................................61 3.2.6.1 Spezifität der Real-Time Consensus-PCR für Hefen mit SYBR®-Green I ..........61 3.2.6.2 Spezifität der Real-Time Consensus-PCR für Hefen mit Hybridisierungssonden .........................................................................................63 3.2.7 Sensitivität der Real-Time Consensus-PCR für Hefen mit Hybridisierungssonden .........................................................................................64 3.2.7.1 Sensitivitätstestung mit quantifizierter, RNA-freier DNA ...................................64 3.2.7.2 Sensitivität in Kombination mit der mechanisch/thermischen DNA-Extraktion.......................................................................................................66 3.2.7.3 Sensitivität in Kombination mit der erweiterten, mechanisch/thermischen DNA-Extraktion.......................................................................................................68 3.2.7.4 Detektionszeit für unterschiedliche Hefearten ....................................................68 3.2.7.5 Sensitivität bei einer hohen Begleitflora ..............................................................71 4 Diskussion ..............................................................................................................73 4.1 Beurteilung der STA1-3 und EF-3 Gene als Targetmoleküle..............................73 4.2 Spezifität und Sensitivität der Real-Time PCR-Assays.......................................78 4.3 Anwendbarkeit der Real-Time PCR in Kombination mit der Probenaufarbeitung ...............................................................................................81 4.4 Ausblick ..................................................................................................................92 5 Literatur...................................................................................................................93 6 Anhang ..................................................................................................................110 6.1 Getestete Mikroorganismen ................................................................................110 6.2 Sequenzauswertung ............................................................................................111 6.3 Real-Time RT-PCR................................................................................................124 6.3.1 RNA-Extraktion.....................................................................................................124 6.3.2 Real-Time One-Step RT-PCR...............................................................................124 6.3.3 Real-Time One-Step RT-PCR-Programm............................................................125 6.3.4 Real-Time One-Step RT-PCR-Ansätze................................................................126 6.3.5 Ergebnisse der Real-Time One-Step RT-PCR....................................................127 V Abbildungsverzeichnis Abbildungsverzeichnis Abb. 3.1: Anordnung der identischen Sequenzabschnitte der Gene SGA1 und MUC1 in der STA Multigen-Familie................................................................38 Abb. 3.2: Anordnung der Primer und Hybridisierungssonden im STA1 Gen............39 Abb. 3.3: Sequenzvergleich der IAK mit dem STA1 Gen.............................................40 Abb. 3.4: Sequenzvergleich der PK mit dem STA1 Gen ..............................................41 Abb. 3.5: Differenzierung zwischen der PK und positiven Proben bei der Real-Time PCR für S. cerevisiae var. diastaticus.........................................42 Abb. 3.6: Amplifikation und Schmelzkurven-Analyse des STA Genfragments von S. cerevisiae. var. diastaticus Stämmen ...............................................43 Abb. 3.7: Agarosegelelektrophorese nach Real-Time PCR mit dem S. cerevisiae var. diastaticus System ..................................................................................44 Abb. 3.8: Sensitivität der Real-Time PCR für S. cerevisiae var. diastaticus..............46 Abb. 3.9: Sensitivität der Real-Time PCR für S. cerevisiae var. diastaticus bei einer hohen Begleitflora .................................................................................47 Abb. 3.10: Real-Time PCR Nachweis von S. cerevisiae var. diastaticus in Flaschenbier....................................................................................................52 Abb. 3.11: Schematische Darstellung der Aminosäuresequenz des Elongationsfaktors 3 von Hefen ....................................................................53 Abb. 3.12: Dendrographische Auswertung der EF-3 Gensequenzen...........................57 Abb. 3.13: Konstruktion der Hybridisierungssonde Yff3 für das EF-3 Genfragment....................................................................................................59 Abb. 3.14: Sequenzvergleich der IAK mit dem EF-3 Gen von S. cerevisiae var. diastaticus .......................................................................................................60 Abb. 3.15: Agarosegelelektrophorese nach Real-Time PCR mit SYBR®-Green I ........61 Abb. 3.16: Schmelzkurven-Analyse von spezifischen Amplifikaten und Primerdimeren.................................................................................................62 Abb. 3.17: Schmelzkurven-Analyse von unspezifisch amplifizierter Bakterien-DNA.................................................................................................63 Abb. 3.18: Schmelzkurven-Analyse unterschiedlicher Hefearten ................................64 Abb. 3.19: Sensitivität der Real-Time Consensus-PCR für Hefen ................................66 Abb. 3.20: Real-Time PCR Nachweis von D. bruxellensis in Orangensaft ..................69 Abb. 3.21: Sensitivität bei Anwesenheit einer hohen Begleitflora ...............................72 Abb. 6.1: Alignment der Nucleinsäuresequenzen des EF-3 Sequenzabschnitts (Position 2272-2637) mit Angabe der Primerpositionen............................111 Abb. 6.2: Real-Time One-Step RT-PCR .......................................................................127 Abb. 6.3: Agarosegelelektrophorese nach Real-Time One-Step RT-PCR................128 Abb. 6.4: Schmelzkurven-Analyse zur Kontrolle des DNA Abbaus .........................128 VI Tabellenverzeichnis Tabellenverzeichnis Tab. 2.1: Hefestämme.....................................................................................................19 Tab. 2.2: Bakterienstämme ............................................................................................21 Tab. 2.3: Schimmelpilzstämme .....................................................................................22 Tab. 2.4: YM-Medium (yeast extract-malt extract broth) .............................................22 Tab. 2.5: CASO-Bouillon ................................................................................................22 Tab. 2.6: Peptonwasser (gepuffert)...............................................................................23 Tab. 2.7: MRS-Bouillon ..................................................................................................23 Tab. 2.8: LB-Medium (Luria-Bertani-Medium) ..............................................................23 Tab. 2.9: LB-Agarplatten ................................................................................................23 Tab. 2.10: SOC-Medium ...................................................................................................23 Tab. 2.11: Primer für die DNA-Kontrolle .........................................................................24 Tab. 2.12: Primer zur Amplifikation von PCR-Fragmenten des EF-3 Gens.................24 Tab. 2.13: Primer für Real-Time PCR Nachweissysteme ..............................................24 Tab. 2.14: Mutageneseprimer zur Herstellung von internen Amplifikationskontrollen und Positivkontrollen ...................................................................25 Tab. 2.15: Hybridisierungssonden für die Real-Time PCR-Assays .............................25 Tab. 2.16: Getränkeproben ..............................................................................................26 Tab. 2.17: Nährmedien .....................................................................................................26 Tab. 2.18: Prozessproben von Brauerei A......................................................................26 Tab. 3.1: Spezifität der Real-Time PCR für S. cerevisiae var. diastaticus .................43 Tab. 3.2: Abbaubarkeit von Amplifikaten des STA Gens mit dem Enzym UNG .......45 Tab. 3.3: Sensitivität der Real-Time PCR für S. cerevisiae var. diastaticus..............46 Tab. 3.4: Sensitivität der Real-Time PCR für S. cerevisiae var. diastaticus bei einer hohen Begleitflora .................................................................................47 Tab. 3.5: Amplifikation der IAK der Real-Time PCR für S. cerevisiae var. diastaticus bei einer hohen Begleitflora .......................................................48 Tab. 3.6: Eignung der Real-Time PCR für S. cerevisiae var. diastaticus in Kombination mit der mechanisch/thermischen Aufarbeitung für unterschiedliche Probenmatrices .................................................................48 Tab. 3.7: Ergebnisse des Versuchsteils 1: Robustheit ...............................................50 Tab. 3.8: Ergebnisse des Versuchsteils 2: Spezifität ..................................................51 Tab. 3.9: Ergebnisse des Versuchsteils 3: Sensitivität...............................................52 Tab. 3.10: Sensitivitätstestung mit quantifizierter, RNA-freier DNA ............................65 Tab. 3.11: Eignung der Real-Time Consensus-PCR für Hefen in Kombination mit der mechanisch/thermischen Aufarbeitung für unterschiedliche Probenmatrices und Hefearten......................................................................67 VII Tabellenverzeichnis Tab. 3.12: Eignung des Real-Time Consensus-PCR für Hefen in Kombination mit der erweiterten, mechanisch/thermischen Aufarbeitung für unterschiedliche Probenmatrices .................................................................68 Tab. 3.13: Detektionszeit für langsam wachsende Hefen .............................................69 Tab. 3.14: Detektionszeit in Abhängigkeit von der Hefeart und der Probenaufarbeitung ........................................................................................70 Tab. 3.15: Sensitivität bei einer hohen Begleitflora.......................................................71 Tab. 6.1: Stämme für die Spezifitätstestung der Real-Time PCR für S. cerevisiae var. diastaticus..............................................................................................110 Tab. 6.2: Distanz-Matrix: Prozentuale Übereinstimmung der EF-3 Aminosäuresequenzen innerhalb der Unterabteilung der Ascomycota ......................119 Tab. 6.3: Distanz-Matrix: Prozentuale Übereinstimmung der EF-3 Aminosäuresequenzen innerhalb der Unterabteilung der Basidiomycota ..................124 VIII Abkürzungsverzeichnis Abkürzungsverzeichnis A Abb. Acc. No. AFLP ATCC ATP aw B B. BCD bp BSA Bul. C C. Ci Cl. Cr. c. CBS Cp dATP dCTP dGTP D D. Deb. DEFT DNA DNase dNTP DSM dTTP dUTP E. EDTA ELISA En. EPS et al. F. fg FRET G G. g xg GÄ H. Hy. I I. Adenin Abbildung accession number amplified fragment length polymorphism American Type Culture Collection Adenosintriphosphat Wasseraktivität Cytosin, Guanin oder Thymin Brettanomyces BIOTECON Diagnostics GmbH (Potsdam, Deutschland) Basenpaar bovine serum albumin (Rinderserumalbumin) Bullera Cytosin Candida Citeromyces Clavispora Cryptococcus cerevisiae Centraalbureau voor Schimmelcultures crossing point Desoxyadenosintriphosphat Desoxycytosintriphosphat Desoxyguanosintriphosphat Adenin, Guanin oder Thymin Dekkera Debaryomyces direct epifluorescent filter technique deoxyribonucleic acid (Desoxyribonucleinsäure) Deoxyribonuclease Desoxynucleotidtriphosphat; (dATP, dCTP, dGTP und dTTP und/oder dUTP) Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH Desoxytymidintriphosphat Desoxyuridintriphosphat Escherichia Ethylendiamintetraessigsäure enzyme linked immunosorbant assay Endomyces extrazelluläre Polysaccharide et alii (und andere) Filobasidiella Femtogramm (10-15 Gramm) fluorescence resonance energy transfer Guanin Guilliermondella Gramm Vielfaches der Erdbeschleunigung g (g = 9,81 m s-2) Genomäquivalent Hanseniaspora Hyphopichia Inosin Issatchenkia IX Abkürzungsverzeichnis IAK ITS ISO K K. Ka. Kap. KBE kbp l L. La. M M. Mbp MEA min ml mM MPN mRNA MUCL N NCYC ng nm OD P. past. PCR pg pH PK R R. RAPD rDNA RFLP RNA RNase rRNA RT S S. Sch. sp. Sp. T T. Tab. TBE TE TGYA Tr. interne Amplifikationskontrolle internal transcribed spacer International Organization for Standardization Guanin oder Thymin Kluyveromyces Kazachstania Kapitel Koloniebildende Einheiten Kilobasenpaare (103 Basenpaare) Liter Lodderomyces Lachancea Adenin oder Cytosin Metschnikowia Megabasenpaare (106 bp) Malzextrakt Agar Minuten Milliliter (10-3 Liter) millimolar (10-3 molar) most probable number messenger RNA (Boten-RNA) Stammnummer der BCCM (Belgian co-ordinated Collection of Microorganisms) Adenin, Cytosin, Guanin oder Thymin National Collection of Yeast Cultures Nanogramm (10-9 Gramm) Nanometer (10-9 Meter) optische Dichte Pichia pastorianus polymerase chain reaction (Polymerase-Kettenreaktion) Pikogramm (10-12 Gramm) negativer, dekadischer Logarithmus der Wasserstoffionenkonzentration Positivkontrolle Adenin oder Guanin Rhodotorula random amplified polymorphic DNA ribosomale DNA Restriktionsfragment-Längenpolymorphismen ribonucleic acid (Ribonucleinsäure) Ribonuclease ribosomale RNA Reverse Transkriptase Cytosin oder Guanin Saccharomyces Schizosaccharomyces species Sporidiobolus Thymin Torulaspora Tabelle Tris-Borat-EDTA-Puffer Tris-EDTA-Puffer Trypton Glucose Hefeextrakt Agar Trichosporon X Abkürzungsverzeichnis Tris var. VBNC VTT W X-Gal Y Y. YM Z. µg µl Tris(hydroxymethyl)aminomethan variety (Varietät) viable but nonculturable Valtion Teknillinen Tutkimuskeskus, Kulturstammsammlung (Finnland) Adenin oder Thymin 5-Brom-4-Chlor-3-indolyl-β-D-galactodid Cytosin oder Thymin Yarrowia yeast extract-malt extract Zygosaccharomyces Mikrogramm (10-6 Gramm) Mikroliter (10-6 Liter) XI Zusammenfassung Zusammenfassung Im Rahmen dieser Arbeit wurden zwei Real-Time PCR-Systeme zum Nachweis von getränkerelevanten Hefen auf Basis der LightCycler® Technologie mit Hybridisierungssonden entwickelt. Für beide Systeme wurden interne Amplifikationskontrollen und Positivkontrollen hergestellt und zwei DNA-Extraktionssysteme bereitgestellt. Ein hoch spezifischer und sensitiver Einzelnachweis für die wichtigste, bierschädliche Saccharomyces Fremdhefe, S. cerevisiae var. diastaticus, wurde entwickelt, indem die sequenziellen Unterschiede zwischen den Glucoamylase kodierenden Genen von S. cerevisiae var. diastaticus (STA1-3) und S. cerevisiae (SGA1) ausgenutzt wurden. Die hohe Nachweisempfindlichkeit des PCR-Systems von 5 bis 10 GÄ pro Reaktion ermöglichte in Kombination mit einer schnellen, mechanisch/thermischen Probenaufarbeitung, die sich aus einem Zellaufschluss mit Glaskügelchen, hohen Temperaturen und dem Ionenaustauscher Chelex® 100 zusammensetzte, den Nachweis von 102 bis 103 S. cerevisiae var. diastaticus Zellen/ml bei einer Hintergrundpopulation von 108 Zellen/ml S. cerevisiae. Die Robustheit des Systems wurde durch Testung von 66 unterschiedlichen Probenmatrices, von denen sich nur eine als ungeeignet für das Real-Time PCR-System herausstellte, gezeigt und die Praxistauglichkeit wurde direkt bei vier Brauereien verifiziert. Der gesamte Assay mit Probenaufarbeitung und PCR ist innerhalb von 2,5 Stunden durchführbar und damit signifikant schneller als kultivierungsabhängige Methoden. Die Sequenzierung eines Abschnitts des Gens des Elongationsfaktors 3 (EF-3) von 93 Hefestämmen lieferte die Grundlage für die Entwicklung einer Real-Time Consensus-PCR zum Nachweis von getränkerelevanten Hefen. Der Nachweis von allen 252 getesteten Hefestämmen wurde bei dem Assay durch degenerierte Primer und Hybridisierungssonden ermöglicht, ohne dass mit DNA von einer der 71 getesteten Bakterien falsch-positive Ergebnisse auftraten. Der Nachweis konnte nicht zur Identifizierung der Hefearten oder -gattungen eingesetzt werden und die Abgrenzung zu den Schimmelpilzen, die ebenfalls das EF-3 Gen enthalten, ließ sich nicht zu 100 % erreichen. Die Sensitivität des Systems lag in Abhängigkeit von der Hefeart zwischen 10 und 250 GÄ pro Reaktion und in Kombination mit einer Erweiterung der mechanisch/thermischen Probenaufarbeitung bei 103 bis 104 Zellen/ml. Bei sehr niedrig kontaminierten Getränkeproben mit 1 bis 100 Zellen/ml war ein Nachweis nach zwei bis drei Tagen Flüssiganreicherung in YM-Medium möglich. XII 1 Einleitung 1 Einleitung 1.1 Getränkerelevante Hefen Die Anwesenheit von Mikroorganismen in Getränken kann aus drei Gründen für den Menschen von Interesse sein. Das Getränk kann zum einen pathogene Mikroorganismen beherbergen, die bei Aufnahme ein Gesundheitsrisiko für den Menschen darstellen. Zum anderen können Mikroorganismen zu unerwünschten Veränderungen von Getränken führen, sodass sie nicht mehr für den Verzehr geeignet sind. Dem gegenüber übernehmen einige Arten entscheidende Prozesse bei der Produktion einer Vielzahl von Getränke, die durch Fermentation hergestellt werden (Fleet 1992). Hefen sind besonders für ihren positiven Beitrag bei der Herstellung von Getränken bekannt. Die Gefahr sich über Getränke mit pathogenen Hefearten (Candida albicans, Candida tropicalis oder Cryptococcus neoformans) zu infizieren ist dagegen von untergeordneter Bedeutung (Fleet 1992). Zu den Hefen zählen Pilze aus den Unterabteilungen der Asco- oder Basidiomycota, die einzellig oder mit Pseudohyphen vorliegen können, sich entweder vegetativ durch Sprossung oder binäre Spaltung reproduzieren oder sexuelle Stadien bilden, die nicht in Fruchtkörpern eingeschlossen sind (Boekhout und Phaff 2003). Hefen können als Verderbniserreger von Getränken eine bedeutende Rolle spielen, wobei hierzu oftmals auch Getränke wie z.B. Bier oder Wein zählen, bei deren Produktion Hefen beteiligt waren. Visuell erkennbare Beeinträchtigungen wie Trübung und Bodensatzbildung können dabei durch die gebildete Hefebiomasse hervorgerufen werden. Einige Hefearten bilden bei ihrem Wachstum Pseudohyphen oder Zellverbände, die in klaren Getränken als Partikel oder an der Oberfläche von Getränken als Filme sichtbar werden (Kato 1981, Pitt und Hocking 1997). Die Produktion von extrazellulären, pektolytischen Enzymen kann Fruchtsäfte ausklären. Sensorische Beeinträchtigungen durch Geruchs- oder Geschmacksveränderungen können durch primäre und sekundäre Stoffwechselendprodukte wie Alkohole, organische Säuren, Aldehyde und Ester entstehen (Weidenbörner 1998). Eine der extremsten, sichtbaren Auswirkungen stellt sicher das Anschwellen oder die Bombage von Produktverpackungen aufgrund einer starken CO2-Produktion dar (Fleet 1992). Die Quellen, über die Hefen in Getränke gelangen, sind vielfältig und reichen von den Ausgangssubstanzen, Staub- und Luftkontaminationen, Insekten als Vektoren (z. B. Drosophila spp.), Flaschenabfüllanlagen, Flaschenverschlüssen (Kronkorken, Korken) bis hin zu mangelhaft gereinigten Flaschen (Back 1994, Deák 1991, Fleet 1992, Mortimer und Polsinelli 1999). Nach Schätzungen sind 95 % aller Kontaminationen von alkoholfreien Getränken mit Hefen, auf ungenügende Hygiene zurückzuführen (Stratford und James 2003). In der Brauerei wird eine Unterteilung der Kontaminationen in Primärkontaminationen, die im Prozess 1 1 Einleitung vorkommen wie z. B. Kontaminationen der Anstellhefe, und Sekundärkontaminationen, die bei der Abfüllung entstehen, vorgenommen (Back 1994, Fleet 1992). Die Vermehrung von Hefen in einem Habitat hängt entscheidend von vier Parametergruppen ab. Zu den intrinsischen Parametern zählen die Wasseraktivität (aw-Wert), der pH-Wert, das Redoxpotential, das Nährstoffangebot und die Konzentration an Konservierungsmitteln. Für Hefen bestehen teilweise Wachstumsvorteile gegenüber anderen Mikroorganismen, wenn diese Parameter bestimmte Werte annehmen. Niedrige aw-Werte durch hohe Salz- oder Zuckerkonzentrationen und niedrige pH-Werte können selektiv zu Gunsten von Hefen wirken. Unter anaeroben oder semi-anaeroben Verhältnissen sind von den bekannten Hefearten ca. ein Drittel in der Lage, ihren Energiestoffwechsel aufrechtzuerhalten und von aerober Atmung auf Gärung umzustellen (Pasteur Effekt). Auch Resistenzen gegenüber Konservierungsmitteln wie z. B. Benzoesäure, Sorbinsäure oder SO2 oder die direkte Nutzung dieser Substanzen als Substrat sind bei einigen Arten möglich (Miller 1979, Steels et al. 1999a, Steels et al. 2000). Von den extrinsischen Parametern sind bei Getränken besonders die Temperatur und die Atmosphäre für Hefen von Bedeutung. Neben dem Aspekt, dass Hefen teilweise anaerobe oder semi-anaerobe Verhältnisse tolerieren, können auch Toleranzen gegenüber erhöhten CO2-Konzentrationen und niedrigen Temperaturen bestehen (Stratford und James 2003, Steels et al. 1999a). Die Art der Herstellung und Abfüllung von Getränken beeinflusst entscheidend die Anwesenheit von Hefen. Während vegetative Hefezellen in Abhängigkeit von weiteren Parametern wie pH-Wert, Ethanol-Gehalt und Konzentration an Konservierungsmitteln relativ schnell bei Temperaturen oberhalb von 65 °C abgetötet werden, werden für Ascosporen wesentlich höhere D-Werte ermittelt (Fleet 1992). Antagonismus oder Synergismus mit anderen Hefearten oder Mikroorganismen beeinflussen ebenfalls das Wachstum von Hefen durch z. B. unterschiedliche Wachstumsgeschwindigkeiten, gebildete Endprodukte oder Killertoxine (Deák 1991). 1.1.1 Alkoholfreie Getränke Die Gruppe der alkoholfreien Getränke, auch Soft-Drinks genannt, beinhaltet unterschiedliche Getränketypen wie Fruchtsäfte, Fruchtnektars, karbonisierte Getränke (Limonaden und Cola-Limonaden), stille Getränke und Mineralstoffgetränke (isotonische Getränke), die unterschiedliche Anteile an Zusätzen wie Zucker, Frucht- oder Gemüseextrakten enthalten. Getränke wie Fruchtsäfte und -nektars, die in erster Linie aus Fruchtmuttersäften oder Saft- und Aromakonzentraten hergestellt werden, bieten für ein mikrobielles Wachstum ein ideales Nährstoffangebot (Weidenbörner 1998). Ein niedriger pH-Wert zwischen 2,5 und 4,5, hervorgerufen durch Fruchtsäuren, selektiert jedoch zu Gunsten von säuretoleranten Mikroorganismen unter ihnen auch einige Hefearten (Back 1994). In Fruchtsaftkonzentraten wachsen 2 1 Einleitung nahezu ausschließlich Hefen (Weidenbörner 1998). Karbonisierte, alkoholfreie Getränke, die einen hohen Zuckeranteil, einen niedrigen pH-Wert, eine niedrige Sauerstoffkonzentration und eine hohe CO2-Konzentration haben, bieten nur einer geringen Zahl an Hefen, Schimmelpilzen und einigen säuretoleranten Bakterien (z. B. Lactobacillus und Acetobacter spp.) gute Wachstumsbedingungen. Ein hoher CO2-Gehalt hat besonders gegenüber Bakterien und Schimmelpilzen einen selektierenden Einfluss zugunsten von Hefen (Stratford und James 2003). Aufgrund ihrer physiologischen Merkmale wurden Hefearten, die in alkoholfreien Getränken vorkommen, von Davenport (1996) in Gruppen unterschiedlicher Relevanz klassifiziert. Die wichtigste Gruppe aus obligaten Schadhefen bilden osmotolerante, stark gärfähige und gegenüber Konservierungsmitteln wie z. B. Essigsäure, Sorbinsäure und Benzoesäure resistente Hefearten. Auch in sehr geringer Zahl führen Arten dieser Kategorie in jedem Fall zu einem Verderb der Produkte, wenn sie ihren Vitaminbedarf decken können (Davenport 1996). Zu den wichtigsten Vertretern dieser Gruppe gehören Arten der Gattungen Saccharomyces, Dekkera (anamorph: Brettanomyces), Zygosaccharomyces und Schizosaccharomyces. Saccharomyces cerevisiae und Saccharomyces bayanus (Synonym: S. uvarum) sind die am weitesten verbreiteten Verursacher für den Verderb von karbonisierten und stillen, alkoholfreien Getränken (Back 1999, Back und Anthes 1979). Eine größere Relevanz hat S. exiguus (anamorph: Candida holmii) in Fruchtsäften und karbonathaltigen Getränken (Stratford und James 2003). Schizosaccharomyces pombe ist nicht so weit verbreitet, zeigt aber alle Charakteristika einer Hefe mit hohem Verderbnispotential wie starke Gasproduktion durch Gärung, Resistenzen gegenüber Konservierungsstoffen und Osmotoleranz (Davenport 1996). Das Wachstum dieser Art, die sich durch binäre Spaltung vermehrt, ist mit einer Verdoppelungszeit von 4 Stunden sehr langsam und kann zu einem verzögerten Verderb führen (Stratford und James 2003). Das Wachstum von Dekkera Spezies (anamorph: Brettanomyces) kann besonders aufgrund ihrer Resistenz gegenüber hohen CO2-Konzentrationen karbonathaltige, alkoholfreie Getränke aber auch Fruchtsäfte durch Geschmacks- und Geruchsveränderungen verderben (Back und Anthes 1979, Ison und Gutteridge 1987, Sand und van Grinsven 1976, Heresztyn 1986a,b). Die wichtigsten Arten sind D. bruxellensis, D. anomala und D. naardensis (Davenport 1996). Zu der Gattung Zygosaccharomyces gehören einige Arten, die aufgrund ihrer hohen Gärfähigkeit, Osmotoleranz und Resistenz gegenüber Konservierungsmitteln in hohem Maße zum Verderb von Getränken führen können. Saure (pH 2,5 bis 5,0) Getränke und Getränke mit 3 1 Einleitung einem hohen Zuckergehalt (z. B. Fruchtsäfte, Fruchtkonzentrate, Soft-Drinks, Zuckersirup) sind ein ausgezeichnetes Habitat für diese Gattung. Die Art Z. rouxii kann bei aw-Werten von 0,62 wachsen und besitzt damit die höchste Osmotoleranz aller bekannten Hefearten (Erickson und McKenna 2000). Die Bildung von Filmen auf der Oberfläche von Getränken ist für diese Gattung beschrieben worden (Kato 1981). Die wichtigsten, verderbniserregenden Arten sind Z. bailii, Z. bisporus, Z. rouxii und Z. mellis, die auch phylogenetisch eine separate Gruppe innerhalb der Gattung Zygosaccharomyces bilden (Kurtzman und Robnett 1998). Aber auch die Arten Z. cidri, Z. fermentati, Z. florentinus und Z. microellipsoides können als Verderbniserreger auftreten, wobei Z. microellipsoides in Soft-Drink Produktionsanlagen weit verbreitet ist (James und Stratford 2003). Die 1999 neu beschriebene Art Z. lentus ist osmotolerant, resistent gegenüber Konservierungsmitteln und kann außerdem bei niedrigen Temperaturen (z. B. 4 °C) wachsen (Steels et al. 1999a,b). Opportunistische Verderbniserreger sind nach Davenport (1996) Hefearten, die nur durch Produktionsfehler wie z. B. Unterdosierung von Konservierungsmitteln, Fehler bei der Pasteurisation, Reinigungsfehler oder Sauerstoffzufuhr während der Produktion von alkoholfreien Getränken auftreten. Zu dieser Gruppe gehören Arten wie Debaryomyces hansenii, Candida parapsilosis, Lodderomyces elongisporus, Hanseniaspora uvarum (anamorph: Kloeckera apiculata), Pichia anomala (=Hansenula anomala) und Pichia membranaefaciens (anamorph: Candida valida). Die thermotolerante Art Candida magnoliae kann konzentrierten Fruchtsaft verderben (Deák und Beuchat 1993). Pichia membranaefaciens und seltener Pichia farinosa und Pichia fermentans bilden wie Issatchenkia orientalis beim Verderb Filme auf der Oberfläche der Getränke aus (Back 1987, Loureiro und Malfeito-Ferreira 2003, Parish und Higgins 1989, Pitt und Hocking 1997). Eine weitere Gruppe bilden Arten, die reine Hygiene-Indikatoren darstellen und selbst bei hohen Zellzahlen nicht schädlich für das Produkt sind, deren Anwesenheit aber die Reinigungseffizienz und allgemeine Betriebshygiene anzeigt (Back 1994). Indikatorhefen sind oft mit obligat schädlichen Hefen vergesellschaftet, sodass deren Nachweis die Rolle einer Früherkennung hat. Im Bereich der Herstellung von alkoholfreien Getränken werden oft die Hefearten Candida sake, Candida solani, Candida tropicalis, Clavispora lusitaniae, Cryptococcus albidus, Cryptococcus laurentii, Debaryomyces etchellsii, Rhodotorula glutinis, Rhodotorula mucilaginosa und Trichosporon cutaneum (=Trichosporon beigelii) nachgewiesen (Back 1999, Davenport 1996). 4 1 Einleitung 1.1.2 Bier Die hauptsächlich als Bierhefen eingesetzten Stämme gehören zu den Arten Saccharomyces pastorianus (=S. carlsbergensis, untergärige Hefen) und S. cerevisiae (obergärige Hefen), die zusammen mit S. bayanus und S. paradoxus den Saccharomyces sensu stricto Komplex bilden (Vaughan Martini und Martini 1987a, Vaughan Martini 1989). In geringerem Ausmaß werden auch Dekkera Arten z. B. in einigen belgischen Bieren und Mischkulturen mit Milchsäurebakterien (Berliner Weisse) eingesetzt (Back 1994). Die Reinheit dieser Anstellkulturen ist für jede Brauerei von entscheidender Bedeutung, da sich jede Kontamination in Veränderungen des Fermentationsverhaltens und des Biergeschmacks auswirken kann. Als Fremdhefen werden in Brauereien alle Hefestämme eingestuft, die nicht bewusst eingesetzt werden. Demnach kann auch jede Brauhefe in einem anderen Brauprozess eine Kontamination darstellen (Dufour et al. 2003). Besonders in Brauereien, die mit unterschiedlichen Hefestämmen zur Produktion von unterschiedlichen Biersorten arbeiten, besteht das Risiko, eine Brauhefe mit einer charakteristisch anderen Brauhefe zu kontaminieren (Campbell 2002). Für Primärkontaminationen der Kulturhefe und im Unfiltratbereich sind oft Arten aus dem Saccharomyces sensu stricto Komplex, Saccharomyces exiguus (anamorph: C. holmii) und Saccharomycodes ludwigii verantwortlich (Back 1994). Geschmacksfehler durch phenolische Verbindungen, die durch Primärkontaminationen hervorgerufen werden und bis ins Endprodukt gelangen, können z. B. durch Saccharomyces cerevisiae var. diastaticus Stämme verursacht werden, die über ein POF- (phenolic off flavour) Gen verfügen (Dufour et al. 2003). Wild- oder Fremdhefen der Gattungen Candida, Pichia (z. B. P. membranaefaciens), Debaryomyces, Hanseniaspora, Issatchenkia, Kluyveromyces, Torulaspora, Schizosaccharomyces, Cryptococcus, Filobasidium, Rhodotorula und Zygosaccharomyces sind ebenfalls als Kontaminationen zu finden, sie sind jedoch weniger an die Fermentationsbedingungen angepasst und sind daher für die Produktqualität weniger gefährlich (Barnett et al. 1983, Dufour et al. 2003). Eine Kontamination des Sauerguts kann besonders durch thermotolerante Arten wie Kluyveromyces marxianus (=Candida kefyr) oder Candida magnoliae erfolgen (Back 1994). Eine Reihe dieser Hefearten sind als Indikatorkeime wichtig, da sie zwar nicht direkt bierschädlich sind, ihr Nachweis aber für die Betriebskontrolle wichtige Informationen über die hygienischen Bedingungen liefert. Debaryomyces hansenii (anamorph: C. famata) kommt häufig vergesellschaftet mit Bierschädlingen vor, besitzt aber selbst keine ausgeprägte Gärfähigkeit (Back, 1994). Sekundärkontaminationen von Bier sind aufgrund der selektiven Bedingungen wie anaerobe Atmosphäre, niedriger pH-Wert, Hopfenbitterstoffe, Alkoholgehalt, Mangel an Nährstoffen und niedrige Temperaturen nur durch wenige Hefen und Bakterien möglich (Back 1994). 5 1 Einleitung Neben den eigentlichen Brauhefen können Saccharomyces Arten oder Varietäten des Saccharomyces sensu stricto Komplexes (z. B. S. bayanus, Wildtypen von S. cerevisiae, S. c. var. cratericus, S. c. var. ellipsoideus und S. c. var. chevalieri) im abgefüllten Bier in Abhängigkeit vom Restnährstoffgehalt wachsen und dadurch zur Trübung, zu Bodensatz, zur Übersättigung mit CO2, zu Geruchs- und Geschmacksveränderungen führen (Back 1994). Eine obligat bierschädliche Hefe ist S. c. var. diastaticus durch ihre Fähigkeit höhere Dextrine und Stärke, die als Restnährstoffe im Endprodukt Bier vorliegen, über eine extrazelluläre Glucoamylase zu verwerten (Dufour et al. 2003). Schon sehr geringe Zellzahlen dieser Hefe können zu einer Übervergärung des Bieres führen (Campbell 2002). Die Mehrheit der bierschädlichen Hefearten gehört zu der Gattung Saccharomyces. Nur ca. 20-30 % bilden Mitglieder einer anderen Gattung wie z. B. Candida, Dekkera, Pichia, Hanseniaspora, Debaryomyces, Torulaspora (Deák 1991). Wie in alkoholfreien Getränken können auch im Bier schwach gärfähige Arten der Gattung Dekkera (anamorph: Brettanomyces) bei ihrem Wachstum durch die Bildung von z. B. Essigestern für Geschmacks- und Geruchsveränderungen sorgen (Heresztyn 1986a,b). Arten wie Pichia anomala (=Hansenula anomala), Pichia membranaefaciens und Kluyveromyces marxianus (=Candida kefyr) führen im Bier zu Geschmacksfehlern durch die Bildung von Äthylacetat, flüchtigen Phenolen, Säuren und Estern. Sie sind jedoch wie einige Candida Arten (z. B. C. boidinii, C. sake, C. intermedia, C. vini, C. parapsilosis und C. tropicalis) auf Sauerstoff angewiesen und bilden daher beim Wachstum auf Flüssigkeitsoberflächen Filme aus (Back 1994, Fleet 1992). 1.1.3 Wein Am Anfang der Weinherstellung wird der Most von einer Mischpopulation unterschiedlicher Hefearten dominiert, die zu einer spontanen Fermentation führen und je nach Ausmaß das Endprodukt beeinflussen können. Zu diesen Arten zählen z. B. Metschnikowia pulcherrima, Zygosaccharomyces sp., Kluyveromyces lactis, Lachancea thermotolerans (=Kluyveromyces thermotolerans), Saccharomyces exiguus (anamorph: C. holmii), Debaryomyces hansenii (anamorph: C. famata) Torulaspora delbrueckii, Hanseniaspora sp. (anamorph: Kloeckera sp.), Issatchenkia orientalis, Pichia sp. (=Hansenula sp.), Cryptococcus albidus und Cryptococcus laurentii (Deák 1991, Back 1994, Dequin et al. 2003). In diesem Stadium der Fermentation ist es schwierig, vorteilhafte und schädliche Aktivitäten der beteiligten Hefen von einander abzugrenzen. Die Art Hanseniaspora uvarum (anamorph: Kloeckera apiculata) ist wie Hanseniaspora vineae (anamorph: Kloeckera africana) oft an Weintrauben und im Weinmost vorhanden und kann durch übermäßige Produktion von Acetat den Weingeschmack negativ beeinflussen (Back 1994, Weidenbörner 2000). Saccharomycodes ludwigii kann selbst in stark geschwefeltem Most hohe Konzentrationen an Acetaldehyd produzieren 6 1 Einleitung (Back 1994, Fleet 1992). Dagegen wird die Produktion von 4-Ethylphenol durch Dekkera sp. (anamorph: Brettanomyces sp.) in Rotwein erst als störend angesehen, wenn eine Konzentration von 620 µg/l überschritten wird (Chatonnet et al. 1992). Konzentrationen unterhalb von 400 µg/l wirken sich dagegen vorteilhaft auf die geschmackliche Komplexität des Weines aus (Loureiro und Malfeito-Ferreira 2003). Im weiteren Verlauf der Fermentation selektieren die Bedingungen wie z. B. die Zugabe von SO2 und die erhöhte Ethanolkonzentration zu Gunsten von S. cerevisiae oder seltener S. bayanus, die zumeist als Starterkulturen zugegeben werden und die Fermentation abschließen (Fleet et al. 1984, Heard und Fleet 1985, Naumov et al. 2000). Nach Abschluss des Fermentationsprozesses ist für die Weinqualität jede weitere Aktivität von Hefen schädlich (Deák 1991). Die Mehrheit der Hefearten, die für den Verderb von Wein, der in Fässern und Tanks gelagert wird, verantwortlich sind, gehört zu den filmbildenden, aeroben oder schwach gärfähigen Arten wie C. vini, C. zeylanoides, C. rugosa, I. orientalis, P. anomala und P. membranaefaciens (Loureiro und Malfeito-Ferreira 2003, Minárik 1981). In Fässern gealterter Rotwein ist ein klassisches Habitat für die Gattung Dekkera (anamorph: Brettanomyces), die große Mengen Acetat durch die Oxidation von Ethanol bilden kann (Back 1987). Selbst in Sherry, der mit mehr als 15 % Ethanol ein sehr ungeeignetes Habitat für die meisten Mikroorganismen darstellt, kann die Art D. bruxellensis wachsen (Ibeas et al. 1996). Neben den genannten Arten sind außerdem für den Verderb von Weinen, die nach GMP (good manufacturing practice) produziert und verpackt wurden, die ethanoltoleranten Stämme der Hefearten Z. bailii und S. cerevisiae besonders gefährlich (Fleet 1992, Loureiro und Malfeito-Ferreira 2003). 1.2 Nachweis und Identifizierung von getränkerelevanten Hefen Für die Qualitätskontrolle und die Qualitätssicherung in der Getränkeindustrie sind möglichst schnelle und zuverlässige Methoden zum Nachweis und zur Identifizierung von Hefen notwendig, um die mikrobielle Stabilität der Endprodukte sicherzustellen. Die Sensitivität dieser Methoden muss so hoch sein, dass z. B. eine Zelle in 100 ml Wein nachweisbar ist (Loureiro und Malfeito-Ferreira 2003). Je schneller die Ergebnisse für die mikrobiologischen Untersuchungen vorliegen, desto aktiver und schneller kann im Herstellungsprozess reagiert werden oder die Auslieferung der Produkte erfolgen. Eine genaue Identifizierung der detektierten Hefen bietet, neben der Möglichkeit deren Schädlichkeitspotential zu beurteilen, auch die Möglichkeit eine Kontamination bis zu ihrem Ursprung zu verfolgen und damit Verbesserungen des Produktionsablaufes einzuleiten (van der Vossen und Hofstra 1996). Eine große Anzahl an unterschiedlichen Methoden steht für diese Zwecke zur Verfügung, um Hefen auf- 7 1 Einleitung grund von phänotypischen oder genotypischen Merkmalen zu detektieren und/oder zu identifizieren. 1.2.1 Kultivierungsabhängiger Nachweis Klassische, mikrobiologische Methoden zum Nachweis von Hefen basieren auf der Kultivierung und Anreicherung von Hefen mit festen oder flüssigen Nährmedien, nachdem von der Ursprungsprobe eine geeignete Verdünnungsreihe hergestellt wurde. Zur Verdünnung, die üblicherweise dekadisch im 1:10 Verhältnis vorgenommen wird, werden Medien wie Peptonwasser (0,1 %), Salzlösungen (0,85 %), Phosphatpuffer (0,1 M, pH 7,0) oder Mischungen dieser Komponenten verwendet. Die Kultivierung erfolgt normalerweise bei Temperaturen zwischen 25 und 28 °C für 5 Tage, kann jedoch bei langsam wachsenden Arten (Z. bailii, D./B. bruxellensis) auch bis zu 14 Tage in Anspruch nehmen (Deák 1991, Millet und Lonvaud-Funel 2000, Rodrigues et al. 2001). Eine große Anzahl an unterschiedlichen, komplexen, nährstoffreichen und unselektiven Medien wird verwendet, die Zucker als Energiequelle (z. B. Glucose, Fructose, Sucrose), verdaute Proteine als Stickstoffquelle (z. B. Pepton, Trypton, Casein) und komplexe Zusätze (z. B. Hefeextrakt, Malzextrakt) enthalten (Loureiro und Malfeito-Ferreira 2003). Im Idealfall sollten die Medien den Nährstoffansprüchen möglichst aller relevanten Hefen genügen, das Wachstum von geschädigten Hefen unterstützen, Bakterienwachstum unterdrücken und ein Überwachsen von Schimmelpilzen vermeiden (Fleet 1992). Oft ist jedoch auch nur der summarische Nachweis von Hefen und Schimmelpilzen erforderlich (Anonymus 1987, Deák 2003). Einige der wichtigsten Universalmedien sind der Glucose-Hefeextrakt Agar (GYE), der Plate-Count Agar (PCA), der Trypton-Glucose-Hefeextrakt Agar (TGYA), der KartoffelDextrose Agar (PDA), der Malzextrakt Agar (MEA) der Hefeextrakt-Malzextrakt Agar (YMA oder MYGPA), der Hefeextrakt-Pepton-Glucose Agar (YPGA) und der Sabouraud-Dextrose Agar (SDA). Das Bakterienwachstum wird entweder durch den Zusatz von Antibiotika (z. B. Oxytetracyclin, Chlortetracyclin, Chloramphenicol, Gentamycin oder Streptomycin) oder durch Absenkung des pH Wertes auf 3,5 unterdrückt, wobei die Verwendung von Antibiotika bevorzugt wird, da die Wiederfindungsrate höher ist (Beuchat 1979, Cava und Hernandez 1994). Hefeextrakt-Glucose-Chloramphenicol Agar (YGCA) wird als ISO-Standardmedium empfohlen (Anonymus 1987). Falls das Wachstum von Schimmelpilzen, die eine Agarplatte komplett überwachsen können, problematisch ist, werden Zusätze wie z. B. Bengalrot, Dichloran und Natrium- oder Kaliumpropionat zu dem Medium gegeben (Henson 1981, King et al. 1979). Dichloran-Bengalrot-Chloramphenicol Agar (DRBC) ist ein oft verwendetes Medium, das sowohl Bakterien als auch Schimmelpilze inhibiert. Beim Einsatz dieser Medien ist zu be- 8 1 Einleitung rücksichtigen, dass deren Zusammensetzung auch das Wachstum von Hefen negativ beeinflussen kann (Banks und Board 1987, Chilvers et al. 1999). Neben den Universalmedien werden selektive Medien eingesetzt, die auf die Ansprüche eines Industriezweiges (z. B. Brauereien, Winzereien) oder der nachzuweisenden Hefearten (z. B. D. bruxellensis) abgestimmt sind. In Brauereien werden selektive Medien verwendet, um Fremdhefen in sämtlichen Bereichen des Produktionsprozesses nachweisen zu können. Ein Nachweis muss hier teilweise so selektiv sein, dass nicht nur Fremdhefen der Gattungen Brettanomyces, Candida, Debaryomyces, Pichia, Torulaspora oder Zygosaccharomyces, sondern auch als Fremdhefen eingeordnete S. cerevisiae Varietäten, die sich von der Brauhefe nur in wenigen Eigenschaften unterscheiden, nachzuweisen sind (Back 1987). Außerdem muss der Nachweis nicht nur selektiv, sondern auch sehr sensitiv sein, wenn sehr geringe Zellzahlen einer Fremdhefe in der Anstellhefe detektiert werden müssen. Eine Reihe von selektiven Medien wurde entwickelt, da kein einzelnes Medium für den Nachweis aller Kontaminationen geeignet ist. Die Selektivität wird dabei durch Zugabe von für S. cerevisiae inhibierenden Substanzen (Kupfersulfat, Cycloheximid, Fuchsinsulfit), von Nährstoffen, die von S. cerevisiae nicht verwertet werden (Lysin, Nitrat, Xylose, Dextrin), durch Farbstoffe (Kristallviolett, Bromkresolgrün), durch Inkubation bei 37 °C oder durch eine Kombination dieser Bedingungen erreicht. (Deák 1991, Back 1994). Für osmotolerante Hefen wie z. B. Z. rouxii werden Verdünnungslösungen und Medien mit hohen, prozentualen Anteilen an Glucose, Glycerol oder Sucrose verwendet, die eine verminderte Wasseraktivität aufweisen und die Zellen vor einem osmotischen Schock bewahren (Beuchat und Hocking 1990). Medien wie z. B. Dichloran-18 % Glycerol Agar (DG18), Malzextrakt-Hefeextrakt Agar mit 30 % Glucose (MY30G), Plate-Count Agar mit 52 % Sucrose oder Trypton-Hefeextrakt Agar mit 10 % Glucose (TY10G) können in Kombination mit Verdünnungslösungen wie z. B. 40 % Glucose oder 30 % Glycerol verwendet werden, um osmotolerante Hefen in konzentrierten Produkten (z. B. Saftkonzentrate) nachzuweisen (Andrews et al. 1997, Beuchat et al. 1998, Hocking und Pitt 1980). Ein weiterer in diesem Bereich eingesetzter Agar ist der Orangenfruchtsaftagar (Back 1999). Hefen wie z. B. Zygosaccharomyces bailii, Pichia membranaefaciens und Schizosaccharomyces pombe, die Resistenzen gegen Säuren und Konservierungsmittel aufweisen, können mit angesäuerten Universalmedien wie MEA oder TGYA selektiv nachgewiesen werden (Hocking 1996). Als Techniken kommen sowohl das Plattengussverfahren als auch das Oberflächenverfahren mit Spatel oder Spiralplater zum Einsatz. Vergleiche der beiden Techniken zeigten, dass das Oberflächenverfahren zu höheren Zellzahlen führt, da beim Plattengussverfahren höhere Temperaturen (ca. 45 °C) eingesetzt werden, die zu einem Hitzestress bei Hefen führen kön- 9 1 Einleitung nen (Deák 2003). Die Sensitivität des Oberflächenverfahrens ist dagegen durch das geringere, einsetzbare Probenvolumen von normalerweise 0,1 ml gegenüber dem beim Plattengussverfahren eingesetzten 1,0 ml vermindert. Wenn die initiale Zellzahl sehr klein ist, können demnach Hefen bei Anwendung des Oberflächenverfahrens unentdeckt bleiben (Deák 1991). Dies kann besonders bei Hefen wie z. B. Z. bailii problematisch sein, die schon bei sehr geringen Zellzahlen Produkte schädigen können. Schon das Inokulum von einer Zelle Z. bailii kann eine Dose mit karbonathaltigem Soft-Drink verderben (Pitt und Hocking 1997, Davenport 1996). Solche geringen Inokula können entweder durch Anwendung von Membranfiltern mit einem Porendurchmesser von 0,45 µm oder durch Voranreicherung in geeigneten, flüssigen Nährmedien vor dem Gebrauch von festen Nährmedien detektiert werden (Pitt und Hocking 1997). Eine weitere klassische, kultivierungsabhängige Methode ist die „most probable number“ (MPN) Technik, die in Kombination mit selektiven Medien zur Bestimmung von Hefearten eingesetzt werden kann, die nur einen geringen prozentualen Anteil an einer Gesamtpopulation haben (Rodrigues et al. 2001). Die routinemäßige Detektion und Quantifizierung von Hefen über Koloniebildende Einheiten (KBE) ist einfach, günstig und allgemein akzeptiert. Nachteile der kultivierungsabhängigen Methoden sind jedoch in dem hohen Arbeitsaufwand, der geringen Reproduzierbarkeit und der langsamen Datengenerierung, die mindestens drei bis fünf Tage Kultivierung benötigt, zu sehen. Die erhaltenen Daten sind demnach für eine Qualitäts- und Prozesskontrolle nur eingeschränkt verwendbar (Deák 1995). Mit weiterentwickelten Methoden wie dem ISO-GRID® Membranfiltrationssystem, das die Membranfiltration mit der MPN Technik verbindet, lässt sich die benötigte Zeit bis zum Ergebnis auf zwei Tage reduzieren (Entis und Lerner 1996). Auch die Anwendung von Petrifilm® YM Platten [3M Microbiology] oder SimPlate® YM Platten [Biocontrol Systems] liefert in kürzerer Zeit vergleichbare Ergebnisse wie die Verwendung konventioneller Nährmedien (Beuchat et al. 1990 und 1991, Ferrati et al. 2005, Vlaemynck 1994). 1.2.2 Mikroskopie, Durchflusszytometrie und Immunoassay Neben den kultivierungsabhängigen Methoden wird seit langem die Mikroskopie zur direkten Quantifizierung von Hefen verwendet, wobei in Kombination mit einer Anfärbung mit Methylenblau eine Differenzierung zwischen lebenden und toten Zellen möglich ist (Back 1994, Smart et al. 1999). Die Lebensfähigkeit von Hefezellen lässt sich auch sehr präzise mit Methoden der Epifluoreszenzmikroskopie, die auf der Anfärbung mit Fluoreszenzfarbstoffen wie z. B. Acridinorange beruhen, ermitteln (Back 1994, Betts et al. 1989). In Kombination mit der Membranfiltration ist diese als „direct epifluorescent filter technique“ (DEFT) bekannte Me- 10 1 Einleitung thode sehr effizient bei der Detektion von Hefen in Bier, Wein oder karbonathaltigen Getränken (Hope und Tubb 1985, Rodrigues und Kroll 1986). Ein Nachteil der mikroskopischen Techniken stellt die eingeschränkte Sensitivität dar, die bei der DEFT bei 103 Zellen/ml liegt, jedoch bei filtrierbaren Proben wie Bier und Wein durch Filtration von größeren Volumina leicht zu erreichen ist. Eine Automatisierung ist durch die Kopplung mit einem Bildauswertungssystem möglich (Pettipher et al. 1992). Die Fluoreszenz In Situ Hybridisierung, die ebenfalls auf der Detektion durch Epifluoreszenzmikroskopie beruht, wurde zum Nachweis von D. bruxellensis (anamorph: B. bruxellensis) angewendet (Stender et al. 2001). Der Test beruht auf fluorescein-markierten „peptide nucleic acid“ Sonden, die mit einem artspezifischen Sequenzbereich der 26 S rRNA hybridisieren. Die Durchflusszytometrie ist eine effektive Methode zur schnellen Zellzahlbestimmung (15 bis 30 min) von Hefen in Bier (Jespersen et al. 1993). Eine Differenzierung zwischen Hefen, Pilzen und Bakterien ist möglich und in Kombination mit Fluoreszenzsonden können Aussagen über die Lebensfähigkeit der Zellen gemacht werden (Deere et al. 1998, Millard et al. 1997). Eine weitere Möglichkeit, um z. B. Fremdhefen in obergäriger Anstellhefe zu detektieren, bietet die Immunofluoreszenzmethode, bei der fluoreszenzmarkierte Antikörper spezifisch an Antigene auf der Oberflächen von Hefen binden und mit der Epifluoreszenzmikroskopie nachweisbar sind (Campbell 2002). Eine Differenzierung zwischen lebenden und toten Zellen ist jedoch mit dieser Methode nicht möglich. Einige weitere Immunoassays zur Detektion von Hefearten sind beschrieben worden, die mit polyklonalen Antikörpern extrazelluläre Polysaccharide (EPS) oder lebende Hefezellen mit der ELISA (enzyme linked immunosorbant assay) Technik nachweisen (García et al. 2004, Marcilla et al. 1999, Middelhoven und Notermans 1988 und 1993, Yoshida et al. 1991). Der Nachweis über EPS war jedoch nicht spezifisch genug und die Produktion der EPS zu sehr von den jeweiligen Wachstumsbedingungen abhängig, um für eine Anwendung in der Lebensmittelindustrie geeignet zu sein (Middelhoven und Notermans 1988 und 1993). Mit polyklonalen Antikörpern, die gegen lebende Zellen gerichtet waren, wurden höchstens 104 bis 105 KBE/ml in Orangensaft oder Milch nachgewiesen (García et al. 2004, Yoshida et al. 1991). Die Spezifität der Systeme war immer eingeschränkt auf einige wenige, für das jeweilige Lebensmittel relevante Arten, die nicht alle gleich sensitiv nachzuweisen waren. Ein weiteres ELISA-System wurde für den Nachweis von Brettanomyces-Kontaminationen in Wein beschrieben (Kuniyuki et al. 1984). 11 1 Einleitung 1.2.3 Elektrometrische Methoden und ATP-Messung Mikroorganismen verändern durch ihr Wachstum die elektrischen Eigenschaften (Kapazität, Leitfähigkeit und Impedanz) ihrer Umgebung. Diese Veränderungen können elektronisch gemessen werden und die Detektionszeit, als die Zeit bis diese Veränderung messbar wird, ist direkt proportional zu der mikrobiellen Ausgangspopulation (Fleet 1992, Deák und Beuchat 1994). Wenn diese Methode gegen eine konventionelle, kultivierungsabhängige Methode kalibriert wurde, kann sie zur Bestimmung der Zellzahl genutzt werden (Deák 1995). Verglichen mit der Ermittlung der KBE verringert sich mit dieser Methode, die auch leichter zu automatisieren ist, der Zeitaufwand auf 10 bis 30 % (Deák 1995). Die Entwicklung von selektiven Medien, die das Wachstum von Bakterien unterdrücken und den Probenmatrices angepasst wurden, ermöglicht den Nachweis von 102 bis 103 Hefezellen/ml nach 12 bis 24 Stunden (Connolly et al. 1988, Schaertel et al. 1987, Watson-Craik et al. 1990, Zindulus 1984). Durch die indirekte Messung der Leitfähigkeit, bei der die produzierte CO2-Menge nach Absorption in einer alkalischen Lösung gemessen wird, kann die Methode unabhängig vom Wachstumsmedium eingesetzt werden (Deák und Beuchat 1994). Zur Anwendung kam die Impedanz Methode bereits zur Überwachung von unterschiedlichen Probenmatrices wie Orangensaftkonzentrat (Weihe et al. 1984), Wein (Henschke und Thomas 1988) und Bier (Evans 1982). Die ATP-Messung über Biolumineszenz ist eine schnelle und sensitive Methode, da unter optimalen Bedingungen 10 Zellen/ml innerhalb von 5 Minuten nachweisbar sind (Fleet 1992). Besonders für Bereiche der Getränkeindustrie wie die Herstellung von Bier und karbonathaltigen Getränken ist die Methode als Summenparameter zur Überwachung geeignet (Hope und Tubb 1985, Hysert et al. 1976, La Rocco et al. 1985, Miller und Galston 1989). Wenn die Filtration von Endprodukten (z. B. Bier) über Membranfilter möglich ist, kann die Sensitivität noch in den Bereich von einigen Zellen pro Liter verbessert werden (Takahashi et al. 2000). Eine Differenzierung zwischen Bakterien, Hefen und Pilzen ist mit dieser Methode jedoch nicht möglich, da alle lebenden Mikroorganismen ATP enthalten. Auch können falschpositive Ergebnisse durch die benutzten Filter, Medien und das Endprodukt auftreten. Daher hat diese Methode in der Lebensmittelindustrie den Stellenwert einer universellen Hygieneüberwachung z. B. bei der Überprüfung der Reinigungseffektivität und der Sterilitätskontrolle von Lebensmitteln (Fleet 1992, Hawronskyj und Holah 1997, Krämer 1997). 12 1 Einleitung 1.2.4 Phänotypische Identifizierung Methoden zur Identifizierung können in der Praxis nicht nur angewendet werden, um zwischen Hefearten zu differenzieren und die relevante Spezies, die für den Verderb verantwortlich ist, zu erkennen, sondern auch, um den Ausgangspunkt für den Verderb in einer Produktionslinie auszumachen (van der Vossen und Hofstra 1996). Typischerweise benötigt man zur Identifizierung von Reinkulturen über phänotypische Merkmale 50 bis 100 Tests, um genügend morphologische, physiologische und biochemische Charakteristika zur sicheren, taxonomischen Einordnung zu erhalten. Diese Prozedur ist arbeitsintensiv, zeitaufwendig, benötigt ein besonderes Maß an Erfahrung und kann aufgrund der Instabilität von physiologischen Merkmalen, zu unklaren Ergebnissen führen (Deák 1995, Scheda und Yarrow 1966). Einige kommerziell erhältliche Hefeidentifizierungssysteme (wie z. B. API 20C, API ID 32C [BioMerieux] oder Biolog MicroLog YT Station [Biolog]) können diesen Aufwand minimieren, sind allerdings für den Bereich der Getränkeindustrie nur begrenzt einsetzbar (Török und King 1991). Die Saccharomyces sensu stricto Gruppe lässt sich z. B. nicht differenzieren oder Z. bailii von Z. bisporus unterscheiden (Baleiras Couto et al. 1996b). 1.2.5 Konventionelle, PCR-basierte Methoden Die Bemühungen, die Genauigkeit und Zuverlässigkeit von Nachweisen und Identifizierungen zu erhöhen, führten in den letzten Jahren in zunehmendem Maße zur Nutzung genotypischer Differenzierungsmerkmale. Die Fortschritte in der Molekularbiologie haben dies durch die Entwicklung einer großen Anzahl an DNA- und RNA-basierten Methoden für die Identifizierung und Charakterisierung ermöglicht. Unterschiede der genomischen DNA, der rRNA oder der Mitochondrien-DNA von Hefen können mit Hilfe der DNA-DNA Hybridisierung (Török et al. 1993, Vaughan Martini und Martini 1987b), der Dot Blot Hybridisierung mit Oligonucleotid-Sonden (Kosse et al. 1997), der Restriktionsenzym Analyse, der Puls-FeldGelelektrophorese (Vezinhet et al. 1990, Guillamón et al. 1996), des RestriktionsfragmentLängenpolymorphismus (RFLP) (Belloch et al. 1997, Guillamón et al. 1994, 1997, Versavaud und Hallet 1995), des DNA-Fingerprinting und der DNA-Sequenzierung (Kurtzman und Robnett 1998) bestimmt werden. Für die Anwendbarkeit in der Routine der Lebensmittelindustrie sind diese Methoden jedoch zu arbeitsaufwändig und zeitintensiv (van Vossen und Hofstra 1996). Eine Weiterentwicklung bei den molekularbiologischen Methoden in Bezug auf Zeit- und Arbeitsaufwand konnte durch die Einbeziehung der Polymerase-Kettenreaktion (PCR), die von Kary Mullis 1983 erdacht und von Saiki et al. (1985) zuerst angewandt wurde, erzielt werden. Bei der Polymerase-Kettenreaktion (PCR) wird ein spezifisches DNA-Fragment über einen 13 1 Einleitung enzymatischen Prozess, der von einem Temperaturzyklus abhängig ist, amplifiziert. Dabei wird die DNA zunächst in einem ersten Schritt (Denaturierungsschritt) bei hoher Temperatur (z. B. 95 °C) denaturiert, sodass zwei spezifische Oligonucleotide als Primer mit den komplementären Strängen hybridisieren können. Diese Oligonucleotide sind so angeordnet, dass sie das zu amplifizierende DNA-Fragment einschließen. Damit die Hybridisierung (Annealingschritt) stattfindet, wird die Temperatur in einem zweiten Schritt auf die so genannte Annealingtemperatur abgesengt, die unterhalb der Schmelztemperatur der Oligonucleotide liegt. Abschließend verlängert eine thermostabile DNA-Polymerase, nachdem die optimale Temperatur für dieses Enzym eingestellt wurde, die Oligonucleotide (Elongationsschritt). Als Resultat wird die DNA zwischen den beiden Oligonucleotiden verdoppelt. Wird das dreistufige Temperaturprofil mehrere Male wiederholt, kann das DNA-Fragment zwischen den Oligonucleotiden exponentiell amplifiziert werden (Saiki et al. 1988). Im Gegensatz zu konventionellen Methoden können hiermit Proben direkt getestet werden, ohne dass eine Kultivierung nötig ist. Außerdem sind PCR-Methoden schnell, sehr spezifisch und können zum Nachweis von sehr geringen DNA-Mengen verwendet werden (Atkins und Clark 2004, van der Vossen und Hofstra 1996). Die einzelnen PCR-abhängigen Methoden zum Nachweis und zur Identifizierung von Hefen unterscheiden sich in der Spezifität der Primer, der Stringenz der PCRBedingungen, der weiteren Behandlung der Amplifikate und der Detektionsmethode für die Amplifikate. Die DNA-Zielregion, die neben taxonomischen Untersuchungen auch zur Entwicklung von Nachweis- und Identifizierungssystemen für Hefen am häufigsten eingesetzt wird, ist das in allen Hefen in hoher Kopienzahl vorhandene, ribosomale Gen-Cluster, das aus den Genen für die 26 S, 18 S, 5,8 S rRNA und teilweise auch 5 S rRNA und deren ITS- (internal transcribed spacer 1 und 2) Regionen besteht (Kurtzman 1994, White et al. 1990). Diese Region weist sowohl hoch konservierte als auch hoch variable Bereiche auf, sodass unterschiedlich spezifische PCR-Primer abgeleitet werden können. Die Amplifikation und anschließende Sequenzierung der D1/D2 Region der 26 S rDNA mit universalen Primern scheint, eine zuverlässige Methode zur Arttypisierung von Hefen der Unterabteilung Ascomycota zu sein (Kurtzman und Robnett 1998). Die Mehrheit der Hefen der Unterabteilung Basidiomycota lässt sich ebenfalls über die Sequenz der D1/D2 Region identifizieren und die Variabilität der ITS1- oder der ITS2-Region scheint, zur Differenzierung zwischen phylogenetisch nah verwandten Arten geeignet zu sein (Fell et al. 2000, Scorzetti et al. 2002). Klinisch relevante Hefen konnten allein aufgrund der Längenpolymorphismen der gebildeten PCR-Produkte der ITS1- und ITS2-Regionen identifiziert werden (Chen et al. 2001, Turenne et al. 1999). Auch wenn die Mehrzahl der PCR-Systeme besonders im klinischen Bereich die ribosomalen Gene als Target nutzt, wurden auch gattungs-, art- und stammspezifische Systeme für 14 1 Einleitung andere Zielregionen entwickelt. Ein Beispiel für eine gattungsspezifische PCR ist das System von Yamagishi et al. (1999), bei dem das FLO1 Gen nur bei Arten der Gattung Saccharomyces vervielfältigt wird. Der stammspezifische Nachweis von Saccharomyces cerevisiae var. diastaticus war mit den STA1-3 Genen als Targetregion möglich (Yamauchi et al. 1998). Falls mit einem einzelnen Primerpaar keine ausreichende Spezifität erreicht wird, kann der Einsatz einer Nested-PCR sinnvoll sein, die auch sensitiver ist (Atkins und Clark 2004). Bei dieser Methode wird nach der ersten PCR mit dem dabei erhaltenen Fragment als Target eine zweite PCR durchgeführt. Bei dieser zweiten PCR wird ein Primerpaar verwendet, das komplementär zu einer innerhalb des ersten Produktes liegenden Sequenz ist. Ibeas et al. (1996) konnten eine Nested-PCR zur Detektion von Dekkera sp. in Sherry entwickeln. Verschiedene PCR-Systeme können zu einer so genannten Multiplex-PCR kombiniert werden, um in einer Probe das Vorhandensein von unterschiedlichen Arten simultan zu prüfen. Eine Differenzierung zwischen S. cerevisiae, S. bayanus und deren Hybriden, die wichtig im Bereich der Wein- und Bierherstellung sein kann, war durch eine Multiplex-PCR ebenso möglich (Torriani et al. 2004) wie die Unterscheidung zwischen S. cerevisiae, Z. bailii und Z. rouxii (Pearson und McKee 1992). Weitere Möglichkeiten, ohne Sequenzierung Polymorphismen im Genotyp aufzudecken, bieten die RAPD-PCR (random amplified polymorphic DNA-PCR) und das PCR-Fingerprinting. Die RAPD-PCR beruht auf der Nutzung von kurzen Primern aus 5 bis 15 Nucleotiden, mit willkürlichen Sequenzen, die bei niedrigen Annealingtemperaturen (z. B. 36 °C) angewendet werden und mit zufällig im Genom verteilten, homologen Sequenzen hybridisieren. Balairas Couto et al. (1995) konnten mit der Methode zwischen einigen für Verderbnis relevanten Hefearten wie z. B. Z. bailii, Z. rouxii und S. cerevisiae differenzieren und Xufre et al. (2000) konnten sie zur Differenzierung von Saccharomyces sp. in einer Winzerei anwenden. Das PCR-Fingerprinting ist im Hinblick auf die Reproduzierbarkeit robuster als die RAPD-PCR, da höhere Annealingtemperaturen verwendet werden (van der Vossen und Hofstra 1996). Diese Methode konnte unter Verwendung von Mikrosatelliten-Primern wie z. B. (GTG)5, (GAC)5, (GACA)4, der M13 Sequenz (GAGGGTGGCGGTTCT) und anderen sich wiederholenden DNA-Sequenzen zur Identifizierung von Hefen bis zur Spezies- oder Subspeziesebene verwendet werden (Baleiras Couto et al. 1996a,b, de Barros Lopes et al. 1998, Hierro et al. 2004, Lavallee et al. 1994, Lieckfieldt et al. 1993, Meyer et al. 1993). Bei der Kombination aus PCR und RFLP werden die PCR-Produkte mit Restriktionsendonucleasen geschnitten, um ein charakteristisches Restriktionsmuster zu erhalten. Diese Methode wurde besonders auf rDNA und deren ITS-Regionen angewendet, um Differenzierungen auf Subspezies oder Stammebene zu ermöglichen (Baleiras Couto et al. 1995, Molina et al. 1993, Niesters et al. 1993, Vilgalys und Hester 1990). Mit einer PCR-RFLP, die die Regi- 15 1 Einleitung on zwischen den 5 S und 26 S rRNA Genen als Target hatte, war eine Differenzierung zwischen Brauereihefen und Fremdhefen sogar zu sehr nah verwandten Stämmen wie S. cerevisiae var. diastaticus möglich (Yamagishi et al. 1999). Eine weitere DNA-Fingerprinting Methode ist die AFLP- („amplified fragment length polymorphism“) Technik, bei der Restriktionsfragmente der gesamten, genomischen DNA nach einem Ligationsschritt selektiv mit Primern amplifiziert werden, die am 3´-Ende spezifisch für die Restriktionsschnittstelle sind (Vos et al. 1995). Diese Methode konnte erfolgreich zur Unterscheidung von Hefestämmen und zur Artidentifizierung von Hefeisolaten eingesetzt werden (de Barros Lopes et al. 1999, Perpète et al. 2001). Eine PCR-Technik, die potentiell zum Nachweis und zur Differenzierung zwischen lebenden und toten Zellen geeignet ist, ist die Umkehrtranskriptions-PCR oder Reverse TranskriptasePCR (RT-PCR). Das Targetmolekül ist hierbei mRNA, die in einem ersten Schritt mit einer Reverse Transkriptase (RTase) in DNA umgeschrieben und in einem zweiten Schritt durch eine PCR amplifiziert wird. Die Differenzierung zwischen lebensfähigen, lebensfähigen aber nicht kultivierbaren („viable but nonculturable“, VBNC) und toten Zellen erfolgt unter der Annahme, dass die Halbwertszeit der mRNA sehr kurz ist und daher nach dem Tod einer Zelle sehr schnell nicht mehr nachzuweisen ist (Sheridan et al. 1998). Von Vaitilingom et al. 1998 wurde eine RT-PCR zur Detektion von lebensfähigen Bakterien, Schimmelpilzen und Hefen in pasteurisierter Milch mit Primern entwickelt, die spezifisch für Gene der Elongationsfaktoren EF-Tu und EF-1α sind. Bei allen bisher erwähnten PCR-Methoden erfolgt nach der Amplifikation eine elektrophoretische Auftrennung der Amplifikate der Länge nach in Agarose- oder Polyacrylamidgelen. Der Nachweis der Amplifikate kann dann in einem letzten Schritt mit unterschiedlichen Methoden detektiert werden, wobei hier nur die Möglichkeiten der Bindung von unspezifischen Fluoreszenzfarbstoffen (z. B. Ethidiumbromid), die Markierung der in der PCR eingesetzten Oligonucleotide mit radioaktiven/fluoreszierenden Nucleotiden oder die Hybridisierung der Amplifikate mit radioaktiven/fluoreszierenden Oligonucleotiden (Southern Blot) genannt werden sollen. Auch der colorimetrische Nachweis von PCR-Produkten der ITS-Regionen von hefeartigen Pilzen über Enzym-Immunoassays wurde erfolgreich zur Identifizierung verwendet (Lindsley et al. 2001). 16 1 Einleitung 1.2.6 Real-Time PCR-Methoden Trotz der wesentlichen Erleichterungen in der täglichen Laborarbeit, die die verhältnismäßig leicht zu automatisierende Methode der PCR mit sich gebracht hat, bedeutet der sensitive, reproduzierbare und spezifische Nachweis der PCR-Produkte noch immer einen hohen Zeitund Arbeitsaufwand. Um das Automatisierungsniveau der PCR zu erhöhen und nicht nur qualitative sondern auch quantitative Aussagen zu ermöglichen, wurde ein so genanntes homogenes Assay entwickelt, bei dem die Amplifikation und der Nachweis des PCRProduktes simultan in einem Reaktionsgefäß möglich ist. Dies gelang erstmals 1993 durch die Weiterentwicklung des 1991 von Holland et al. beschriebenen 5´-Nuclease PCR-Assays unter Ausnutzung der 5´-Exonukleaseaktivität der Taq DNA-Polymerase und Einbeziehung von fluorogenen Sonden zur Detektion der Amplifikation (Lee et al. 1993). Die fluorogenen Sonden dieses so genannten TaqMan™ PCR-Systems sind am 5´-Ende mit einem fluoreszierenden Reporter-Farbstoff und am 3´-Ende mit einem Quencher-Farbstoff markiert. Der Quencher-Farbstoff nimmt zunächst über einen Fluoreszenz- (oder Förster-) ResonanzEnergie-Transfer (FRET) die Absorptionsenergie des Reporter-Farbstoffs auf und unterdrückt damit dessen Fluoreszenz. Während der PCR hybridisiert die Sonde zusammen mit den Primern an den Amplifikaten und in der Extensionsphase wird die Sonde durch die 5´-3´Exonuklease Aktivität der Taq DNA-Polymerase hydrolysiert. Dadurch werden die räumliche Nähe und damit auch der FRET zwischen Reporter und Quencher unterbrochen. Entsprechend der Akkumulation von PCR-Produkten steigt die Fluoreszenz durch freie Reportermoleküle mit jedem PCR-Zyklus an und kann mit einem geeigneten Detektionssystem während der Amplifikation gemessen werden. Neben dem TaqMan™-System existieren eine Reihe von weiteren Varianten der so genannten Real-Time PCR wie das Molecular-Beacons-System, das Scorpions™-System und das Hybridisierungssonden-System, die alle auf unterschiedliche Weise den FRET zwischen Fluoreszenzfarbstoffen ausnutzen, die sich in ihren Spektren überlagern (Caplin et al. 1999, Tyagi und Kramer 1996, Whitcombe et al. 1999). Für das Nachweissystem mit Hybridisierungssonden sind zwei fluoreszenzmarkierte Sonden notwendig, die zusammen mit den Primern an die Amplifikate hybridisieren und dadurch in räumliche Nähe gebracht werden. Nach Anregung des so genannten Donator-Farbstoffes der einen Sonde mit Licht einer bestimmten Wellenlänge kann diese Energie über einen FRET auf den Reporter-Farbstoff der anderen Sonde übertragen werden. Der Repoter-Farbstoff emittiert dann die übertragene Energie als Licht einer bestimmten Wellenlänge, die zur Online-Verfolgung der Amplifikation gemessen wird. Eine sequenzunabhängige Detektion von Amplifikaten ist mit Fluoreszenzfarbstoffen wie SYBR®-Green I möglich, die unspezifisch besonders bei doppelsträngiger DNA zwischen 17 1 Einleitung benachbarten Basen eines Strangs interkalieren. In diesem Zustand absorbieren diese Farbstoffe Licht einer bestimmten Wellenlänge und strahlen diese aufgenommene Energie wieder als Licht mit einer längeren Wellenlänge ab. Für die praktische Anwendung in der Getränkeindustrie wurden bereits zwei artspezifische, quantitative Real-Time PCR-Systeme im SYBR®-Green-Format für die Hefeart Dekkera/Brettanomyces bruxellensis entwickelt (Delaherche et al. 2004, Phister und Mills 2003). 1.3 Ziele der Arbeit In dieser Arbeit sollten Real-Time PCR Nachweissysteme auf Basis der LightCycler® Technologie entwickelt werden, die für eine Anwendung in der Qualitätskontrolle und Qualitätssicherung der Getränkeindustrie geeignet sind. Ein System sollte die obligat bierschädliche Hefe Saccharomyces cerevisiae var. diastaticus spezifisch und sensitiv in unterschiedlichen Probenmatrices wie der Anstellhefe, dem Jungbier und dem Endprodukt nachweisen. Für die Sterilitätskontrolle und die betriebliche Hygieneüberwachung sollte eine weitere Real-Time Consensus-PCR für alle getränkerelevanten Hefen entwickelt werden. Zunächst sollten spezifische Genregionen gesucht und falls notwendig Sequenzinformationen für diese Regionen neu generiert werden. In einem weiteren Schritt sollten von den Sequenzen und Sequenzalignments spezifische Oligonucleotide wie Primer und Sonden abgeleitet werden. Die Spezifität der Systeme sollte sowohl mit einer möglichst großen Anzahl an Targetorganismen als auch mit Mikroorganismen, die als Begleitflora eine Rolle spielen können, getestet werden. Für die praktische Anwendung der Real-Time PCR-Systeme sollte außerdem die Konstruktion und Implementierung von internen Amplifikationskontrollen erfolgen, um negative Ergebnisse aufgrund von Inhibitionen der PCR erkennen zu können. Die kompletten Real-Time PCR-Systeme in Kombination mit geeigneten Probenaufarbeitungsmethoden sollten abschließend mit möglichst praxisnahen Proben auf ihre Sensitivität getestet werden. Damit wären schnelle, selektive und sensitive Werkzeuge für die mikrobiologische Kontrolle von Getränken verfügbar. 18 2 Material und Methoden 2 Material und Methoden 2.1 Mikroorganismen Zusätzlich zu den in der Tabelle 2.1 aufgeführten und taxonomisch bestimmten Hefestämmen wurden nicht näher bestimmte Fremdhefen von den Brauereien A (12 Isolate), B (8 Isolate) und D (34 Isolate) bezogen und ebenfalls in den Spezifitäts- und Sensitivitätstests eingesetzt. Tab. 2.1: Hefestämme Spezies Bullera dendrophila Candida albicans Candida boidinii Candida boidinii Candida boidinii Candida boidinii Candida cariosilignicola Candida catenulata Candida chilensis Candida diddensiae Candida ernobii Candida ethanolica Candida freyschussii Candida friedrichii Candida fructus Candida glabrata Candida glaebosa Candida haemulonii Candida inconspicua Candida intermedia Candida krusei Candida magnoliae Candida maltosa Candida multigemmis Candida norvegica Candida palmae Candida parapsilosis Candida parapsilosis Candida pseudointermedia Candida quercitrusa Candida rhagii Candida rugosa Candida sake Candida sake Candida salmanticensis Candida santamariae Candida santamariae Candida solani Candida succiphila Candida tenuis Stamm/Herkunft DSM 70745 ATCC 10231 DSM 70024 DSM 70033 DSM 70034 Brauerei F DSM 2148 DSM 70136 ATCC 22076 DSM 70042 DSM 70858 Brauerei F DSM 70047 DSM 70050 CBS 6381 BCD 8932 CBS 5691 DSM 70624 MUCL 27868 BCD 685 BCD 689 DSM 70638 BCD 806 DSM 70862 DSM 70863 Brauerei F ATCC 20384 Brauerei F Brauerei F Brauerei F CBS 4237 BCD 814 CBS 2920 BCD 1054 ATCC 16042 CBS 4515 CBS 4261 BCD 818 DSM 2149 BCD 819 Spezies Pichia membranaefaciens Pichia methanolica Pichia minuta Pichia ohmeri Pichia pini Pichia trehalophila Pichia stripitis Rhodotorula sp. Rhodotorula glutinis Rhodotorula minuta Rhodotorula rubra Saccharomyces bayanus Saccharomyces bayanus Saccharomyces bayanus Saccharomyces bayanus Saccharomyces cerevisiae Saccharomyces cerevisiae S. carlsbergensis (=S. pastorianus) Saccharomyces cerevisiae Saccharomyces cerevisiae Saccharomyces cerevisiae S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. carlsbergensis (=S. pastorianus) S. carlsbergensis (=S. pastorianus) S. carlsbergensis (=S. pastorianus) S. carlsbergensis (=S. pastorianus) Saccharomyces cerevisiae Saccharomyces cerevisiae Saccharomyces cerevisiae Saccharomyces cerevisiae S. cerevisiae var. diastaticus 19 Stamm/Herkunft Brauerei F DSM 2147 DSM 70718 BCD 862 DSM 70385 DSM 70391 CBS 5773 ATCC 20254 BCD 3530 DSM 70408 BCD 4081 BCD 1256 BCD 1392 DSM 70412 Brauerei F DSM 1333 DSM 70416 BCD 728 ATCC 44075 CBS 6503 ATCC 42296 BCD 1257 BCD 1432 BCD 1433 BCD 1499 BCD 1501 BCD 2573 BCD 2574 BCD 2581 ATCC 9080 ATCC 12341 ATCC 18790 ATCC 28383 DSM 70452 BCD 13974 2 Material und Methoden Tab. 2.1: Fortsetzung Spezies Candida tropicalis Candida tropicalis Candida versatilis Candida vini Candida viswanathii Candida zeylanoides Citeromyces matritensis Citeromyces matritensis Clavispora lusitaniae Clavispora lusitaniae Cryptococcus albidus Cryptococcus curvatus Cryptococcus curvatus Cryptococcus flavus Cryptococcus flavescens Cryptococcus humicola Cryptococcus laurentii Cryptococcus neoformans Debaryomyces etchellsii Debaryomyces hansenii Debaryomyces hansenii Debaryomyces marama Debaryomyces vanrijiae Dekkera anomala Dekkera anomala Dekkera bruxellensis Dekkera bruxellensis Dekkera custersiana Endomyces fibuliger Endomyces fibuliger Filobasidium capsuligenum Guilliermondella selenospora Hanseniaspora guilliermondii Hanseniaspora uvarum Hanseniaspora uvarum Hanseniaspora vineae Hyphopichia burtonii Hyphopichia burtonii Issatchenkia orientalis Kazachstania unispora Kluyveromyces marxianus Kluyveromyces marxianus Kluyveromyces marxianus Kluyveromyces marxianus Kluyveromyces marxianus Kluyveromyces lactis Lachancea thermotolerans Lachancea thermotolerans Lodderomyces elongisporus Metschnikowia lunata Metschnikowia pulcherrima Stamm/Herkunft ATCC 20247 ATCC 20326 DSM 6956 DSM 70184 ATCC 20385 BCD 690 DSM 70187 BCD 1062 DSM 70102 Brauerei F DSM 70197 DSM 70022 BCD 2578 BCD 823 Brauerei F DSM 70067 BCD 824 BCD 3511 ATCC 20126 BCD 589 BCD 3512 ATCC 11627 DSM 70252 DSM 70727 DSM 70732 DSM 3429 DSM 70726 DSM 70736 BCD 3514 DSM 70554 DSM 70253 DSM 3431 DSM 70285 BCD 3526 ATCC 9774 DSM 70283 BCD 859 DSM 3505 CBS 5147 BCD 877 DSM 70106 BCD 811 DSM 70792 BCD 2563 BCD 5186 DSM 70807 CBS 6340 CBS 137 DSM 70320 CBS 5946 DSM 70321 Spezies S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus Saccharomyces cerevisiae S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus Saccharomyces cerevisiae S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus Saccharomyces cerevisiae Saccharomyces cerevisiae Saccharomyces cerevisiae Saccharomyces castellii Saccharomyces exiguus Saccharomyces exiguus Saccharomyces exiguus Saccharomyces kluyveri Saccharomyces pastorianus Saccharomyces pastorianus Saccharomycopsis fibuligera Schizosaccharomyces octosporus Schizosaccharomyces octosporus Schizosaccharomyces pombe Schizosaccharomyces pombe Sporidiobolus johnsonii Sporidiobolus johnsonii Sporidiobolus johnsonii Stephanoascus ciferrii Torulaspora delbrueckii Torulaspora delbrueckii Torulaspora delbrueckii Trichosporon cutaneum Willipsis saturnus Yarrowia lipolytica Yarrowia lipolytica Yarrowia lipolytica Yarrowia lipolytica 20 Stamm/Herkunft BCD 13980 DSM 70487 VTT C-68059 VTT C-70060 VTT C-82101 Brauerei A Brauerei A Brauerei A Brauerei A Brauerei A Brauerei A Brauerei E Brauerei E Brauerei C Brauerei C Brauerei D Brauerei D Brauerei D Brauerei D Brauerei B Brauerei B Brauerei F Brauerei F Brauerei F Brauerei F BCD 1491 BCD 1493 MUCL 29838 DSM 70517 NCYC 73 DSM 6580 ATCC 9947 BCD 14122 DSM 70573 DSM 70572 BCD 773 BCD 778 BCD 4982 DSM 70847 DSM 70749 CBS 5636 CBS 6339 DSM 70607 DSM 70684 DSM 70388 ATCC 20225 ATCC 20226 BCD 2003 BCD 2556 2 Material und Methoden Tab. 2.1: Fortsetzung Spezies Metschnikowia reukaufii Pichia angusta Pichia anomala Pichia anomala Pichia anomala Pichia anomala Pichia canadensis Pichia carsonii Pichia farinosa Pichia fermentans Pichia fermentans Pichia guilliermondii Pichia membranaefaciens Tab. 2.2: Stamm/Herkunft DSM 70337 DSM 70277 BCD 1082 DSM 70783 Brauerei F Brauerei F CBS 601 DSM 70392 BCD 861 DSM 70090 BCD 711 BCD 804 DSM 70178 Spezies Zygosaccharomyces bailii Zygosaccharomyces bailii Zygosaccharomyces bisporus Zygosaccharomyces cidri Zygosaccharomyces fermentati Zygosaccharomyces florentinus Zygosaccharomyces lentus Zygosaccharomyces microellipsoides Zygosaccharomyces rouxii Zygosaccharomyces rouxii Stamm/Herkunft BCD 1424 MUCL 28823 DSM 70415 MUCL 31280 MUCL 27824 DSM 70506 CBS 8516 DSM 6959 DSM 70835 ATCC 48230 Bakterienstämme Spezies Acetobacter pasteurianus Achromobacter xylosoxidans Acinetobacter baumanii Acinetobacter calcoaceticus Aeromonas hydrophila Bacillus alcalophilus Bacillus badius Bacillus cereus Bacillus firmus Bacillus stearothermophilus Brevundimonas vesicularis Brochotrix campestis Brochotrix thermospacta Carnobacterium piscicola Citrobacter freundii Clostridium perfringens Corynebacterium glutamicum Delftia acidovorans Enterobacter cloacae Enterobacter sakazakii Enterococcus faecalis Erysipelothrix rhusiopathiae Escherichia coli E. coli Serovar O157:H7 Jonesia denitrificans Klebsiella oxytoca Klebsiella pneumoniae Kurthia zopfii Lactobacillus brevis Lactobacillus casei Lactobacillus collinoides Lactobacillus coryniformis Lactobacillus delbrueckii Lactobacillus hilgardii Stamm/Herkunft DSM 3509 DSM 30026 BCD 10388 DSM 1139 DSM 30188 DSM 485 BCD 2929 DSM 508 DSM 1530 DSM 456 DSM 7226 DSM 4712 DSM 20171 DSM 20730 DSM 30040 BCD 8800 DSM 20300 DSM 39 DSM 30054 DSM 4485 DSM 2570 DSM 5055 DSM 30083 BCD 5579 DSM 20603 DSM 5175 ATCC 13883 DSM 20580 DSM 20054 DSM 20011 DSM 20515 DSM 20001 DSM 20072 DSM 20051 Spezies Lactobacillus perolens Lactobacillus sakei Lactococcus lactis subsp. lactis Leuconostoc citreus Leuconostoc mesenteroides subsp. mesenteroides Macrococcus caseolyticus Megasphaera cerevisiae Micrococcus luteus Moraxella catarrhalis Pantoea agglomerans Pectinatus cerevisiiphilus Pectinatus frisingensis Pediococcus damnosus Pediococcus inopinatus Pediococcus parvulus Pediococcus claussenii Pediococcus pentosaceus Planococcus kocurii Plesiomonas shigelloides Proteus mirabilis Proteus vulgaris Pseudomonas aeruginosa Salmonella enterica subsp. enterica Serovar Enteritidis Salmonella senftenberg Serratia marcescens Shewanella putrefaciens Shigella boydii Shigella sonnei Sporosarcina urea Staphylococcus aureus subsp. aureus 21 Stamm/Herkunft DSM 12744 DSM 20494 DSM 20729 DSM 20188 DSM 20241 DSM 20597 DSM 20462 BCD 3906 DSM 9143 DSM 3493 DSM 20467 DSM 6306 DSM 20331 DSM 20285 DSM 20332 DSM 14800 DSM 20336 DSM 3493 DSM 8224 DSM 788 DSM 2140 DSM 288 BCD 14151 BCD 6173 DSM 1636 DSM 6067 DSM 7532 BCD 4301 DSM 2281 DSM 20231 2 Material und Methoden Tab. 2.2: Fortsetzung Spezies Lactobacillus kefiri Lactobacillus lindneri Lactobacillus parabuchneri Lactobacillus plantarum Tab. 2.3: Spezies Streptococcus uberis Weissella confusa Yersinia enterocolitica subsp. enterocolitica Stamm/Herkunft DSM 20569 DSM 20196 DSM 4780 Spezies Hyalodendron lignicola Monilia sp. Mucor circinelloides Paecilomyces variotii Penicillium crustosum Penicillium funiculosum Phialophora hoffmannii Phomopsis phaseoli Phytophthera infestans Rhizopus nigricans Syncephalastrum racemosum Talaromyces flavus Trichoderma viride Verticillium sp. Wallemia sebi Stamm/Herkunft DSM 1877 BCD 8535 BCD 6069 CBS 62866 BCD 6994 DSM 1960 DSM 2693 CBS 42250 MUCL 43045 BCD 3506 BCD 162 BCD 12179 BCD 352 BCD 13586 DSM 5329 Schimmelpilzstämme Spezies Absidia sinosa Alternaria alternata Aspergillus flavus Aspergillus fumigatus Aspergillus parasiticus Aureobasidium pullulans Botrytis cinerea Cephalosporium aphidicola Claviceps purpurea Diaporthe citri Eremascus albulus Fusarium oxysporum Fusarium cerealis Fusarium culmorum Geomyces pannorum 2.2 Stamm/Herkunft DSM 20588 DSM 20690 DSM 5707 DSM 20174 Stamm/Herkunft BCD 3485 BCD 12263 ATCC 9643 DSM 819 DSM 2038 DSM 3042 DSM 4709 ATCC 28300 DSM 714 DSM 1159 BCD 12125 BCD 14059 BCD 14058 DSM 62184 DSM 2689 Nährmedien Für die Nährmedienherstellung wurden nur Chemikalien und Nährmedienzusätze der Firmen Merck, Roth und Sigma-Aldrich verwendet, die vom Hersteller für den Gebrauch in der Mikrobiologie ausgewiesen waren. Die Nährmedien wurden bei 121 °C für 15 Minuten autoklaviert. Tab. 2.4: YM-Medium (yeast extract-malt extract broth) 3,0 g/l 3,0 g/l 5,0 g/l 10,0 g/l 15,0 g/l Hefeextrakt Malzextrakt Pepton D(+)-Glucose Agar-Agar Die Zugabe von Agar-Agar wurde optional je nach Verwendung vorgenommen. Tab. 2.5: CASO-Bouillon 17,0 g/l 3,0 g/l 2,5 g/l 5,0 g/l 2,5 g/l 7,3 ± 0,2 Pepton aus Casein Pepton aus Sojamehl D(+)-Glucose NaCl K2HPO4 pH-Wert bei 25 °C 22 2 Material und Methoden Tab. 2.6: Peptonwasser (gepuffert) 10,0 g/l 5,0 g/l 3,5 g/l 1,5 g/l 7,0 ± 0,2 Tab. 2.7: MRS-Bouillon 10,0 g/l 8,0 g/l 4,0 g/l 20,0 g/l 2,0 g/l 1,0 g/l 2,0 g/l 5,0 g/l 0,2 g/l 0,04 g/l 5,7 ± 0,2 Tab. 2.8: Pepton aus Casein NaCl Na2HPO4 KH2PO4 pH-Wert bei 25 °C Pepton aus Casein Fleischextrakt Hefeextrakt D(+)-Glucose K2HPO4 Tween® 80 Di-Ammoniumhydrogencitrat Natriumacetat MgSO4 MnSO4 pH-Wert bei 25 °C LB-Medium (Luria-Bertani-Medium) (Sambrook et al. 1989) 10,0 g/l 5,0 g/l 5,0 g/l 0,1 g/l Trypton Hefeextrakt NaCl Ampicillin Die Zugabe von Ampicillin erfolgte erst kurz vor der Verwendung des Mediums. Tab. 2.9: LB-Agarplatten 10,0 g/l 5,0 g/l 5,0 g/l 0,1 g/l 0,08 g/l 0,5 mM 15,0 g/l Trypton Hefeextrakt NaCl Ampicillin X-Gal IPTG Agar-Agar Die Zugabe von Ampicillin erfolgte, nachdem das autoklavierte Medium auf ca. 50 °C abgekühlt war. Tab. 2.10: SOC-Medium 0,2 g/l 0,05 g/l 10,0 mM 2,5 mM 2,0 mM 10,0 mM 10,0 mM Trypton Hefeextrakt NaCl KCl Glucose MgCl2 • 6 H2O MgSO4 • 7 H2O Die Herstellung erfolgte gemäß den Angaben, die in der Vorschrift für das pGEM®-T Vektor Kit [Promega] gemacht werden. 23 2 Material und Methoden 2.3 Oligonucleotide Die verwendeten Oligonucleotide wurden von den Firmen Thermo Electron Corporation (Primer), MWG-Biotech (Primer) und Metabion (Hybridisierungssonden) bezogen. Die Nomenklatur der Basen in den Nucleinsäuresequenzen entspricht den Vorgaben der NC-IUB (Nomenclature Committee of the International Union of Biochemistry): A= Adenin; C= Cytosin; G= Guanin; T= Thymin; I= Inosin; N= A/C/G/T; Y= C/T; R= A/G; M= A/C; K= G/T; S= C/G; W= A/T; D= A/G/T; B= C/G/T Tab. 2.11: Primer für die DNA-Kontrolle Bezeichnung ITS1 ITS4 Sequenz 5´-3´ TCCGTAGGTGAACCTGCGG TCCTCCGCTTATTGATATGC Zielregion 18S rDNA 26S rDNA Referenz White et al. 1990 White et al. 1990 Tab. 2.12: Primer zur Amplifikation von PCR-Fragmenten des EF-3 Gens Bezeichnung HS03 HS04 HS09 HS10 HS12/IV HS12/V HS12/VI HS12/VII HS12/VIII HS12/IX HS14/III HS14/IV HS14/V HS14/VI HS14/VII HS14/VIII HSwb1 HSabc3 Sequenz 5´-3´ GAATTYTCTYTKGCWTAYGG TGACTYCTTCARACCYS ACARTGYTBYTCDATYTC ATGGMGITWCCANWCYGGTGA TGGCGATACCAAACCGGTGAAG TGGCGGTTCCATACCGGTGAGG TGGCGATACCAGACTGGTGAGG TGGCGATACCAGACCGGTGAGG TGGAGATACCAGACCGGTGAGG TGGAGGTTCCAGACCGGTGAGG CCATGACTTTCTTTTCGAAACCTC CGAGAATCTTCTTCTCGAAACCAC CAAGAACCTTCTTTTCGAAACCTC CCATAACCTTCTTCTCGAAACCAC CGAGGACCTTCTTCTCGAAACCAC CGAGGACCTTCTTCTCGAACCCAC ITIITIITIGAYGARCCIACYAACCATYTNG CIAIIACIAIYTTIACYTTYTGRCCACCNG Zielregion EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen Referenz Uritani et al. 1999 Uritani et al. 1999 Tab. 2.13: Primer für Real-Time PCR Nachweissysteme Bezeichnung HS11/I HS11/II HS11/III HS11/IV Ha1f Ha2f Ha3f Ha4f Ha5f Hb1f Hb2f Hb3f Hb4f Hb5f Hb6f Hb7f Ha1r Ha2r Ha3r Sequenz 5´-3´ GGTGAGGATAGAGAAACCATGG GGTGAGGATAGAGAAACTATGG GGTGAGGATAGAGAGACCATGG GGTGAGGATAGAGAGACTATGG WCTGGTGAAGATTTGGARGCTATGG CYGGTGARGAYMGWGAAACCATGG WCYGGTGAAGATMGWGAAACTATGG GGTGARGAYMGWGAGACCATGG CYGGTGARGAYMGWGAGACTATGG GAGGCCGAGCTTGCCAAGATG CCGATGCCGAAAAGGAGAAGATG SYGAGGAGGAGRAGAAGAAGATG TGACCGARGAAGAGAWRCAAAAGATG GCCGAGGAAGAGGCCAAGATG ACCGGTGARGAYTTGGARGARMTG ACNGGTGAGGAYMTYGARGA CTCTTCAARGCYTCAGCACGGTC CGKWGGCAAGWGCTTCCTTCATATC CCRGADGCYAAWGCTTCCTTCATATC 24 Zielregion EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen 2 Material und Methoden Tab. 2.13: Fortsetzung Bezeichnung Ha4r Ha5r Ha6r Ha7r Ha8r Hb1r Hb2r Hb3r HT1r HT2r HT3r HT4r HT5r HT6r Yfa1 Yfa2 Yfs1 SD1f SD1r Sequenz 5´-3´ GACCDGADGCYAAAGCTTCTTTCATATC GARGCMARRGCCTCCTTCATGTC CRGAWGCMARAGCCTCCTTCATATC GACCWGAWGCTAAGGCTTCTTTCATATC CGGAAGCCAAAGCTTCCTTCATGTC CAAGTTCMAKRACYTTCTTTTCGAAACCTC CTCSAKRAYCTTCTTCTCGAAACCAC GAGGACCTTCTTCTCGAASCCAC GCYARWGCTTCCTTCATATC GADGCYAARGCTTCTTTCATATC GCMARRGCYTCCTTCATRTC CAARGCYTCAGCACGGTC GACCTTCTTCTCGAASCCAC RAYYTTCTTYTCGAAACCWC GTGARGAYMGWGARACCATG GGTGARGAYMGWGARACTATG GGTGAAGATTTGGARGCTATG TTGCGAATACACTACTGAAGC CGTATACCACTGTCCCATTCAT Zielregion EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen STA1-3 Gen STA1-3 Gen Tab. 2.14: Mutageneseprimer zur Herstellung von internen Amplifikationskontrollen und Positivkontrollen Bezeichnung SDip1r SDip1f SDpo3f SDpo3r Yip1r Yip1f Sequenz 5´-3´ TGGCACTGGAAGAACGTATCGGATAATGATACATAGGTGGTTG GTACAG CATTATCCGATACGTTCTTCCAGTGCCATCAAAGCTGCGGCGG TG CACAACAAAGGCTGTACCAACCACCTATGT ACATAGGTGGTTGGTACAGCCTTTGTTGTG TGGCACTGGAAGAACGTATCGGATAATGTGTTCTTGAACTTTCT TCTG CATTATCCGATACGTTCTTCCAGTGCCAATTGGTATGAAATCTG AAAG Zielregion STA1-3 Gen STA1-3 Gen STA1-3 Gen STA1-3 Gen EF-3 Gen EF-3 Gen Die Veränderungen in der Sequenz gegenüber dem Wildtyp wurden unterstrichen. Tab. 2.15: Hybridisierungssonden für die Real-Time PCR-Assays Bezeichnung SDR1f SDF1f LMRST1 Yff1 Yff2 Yff3 Yff4 Yff5 Yff6 Yff8 Yfr1 Yfr2 Yfr3 Sequenz 5´-3´ LCRed-640-TTGACTTTGGCAAGGGCATTCTCGA-Pho CACAACAAAGTCTGTACCAACCACCTATGT-Fluo LCRed-705-CATTATCCGATACGTTCTTCCAGTGCCA-Pho GAGTTGCTGGTRTICAYKCIAGAAGAAAGTTYAAGAAC-Fluo GAGTTAAAGAAATTITGGCYAGAAGAAARTTYAARAAT-Fluo GAGTTCAAGARATTCAYGCIAGAAGRAARTTCAAGAAC-Fluo GAGTTCAAGGTATTCAYGCTMGAMGIAAGTTYAAGAAC-Fluo GACGAGCTTGTIGSCMGIAAGAAGYTSAAGCARTC-Fluo GATTTTGGGTATYCACAGCCGTMGIAAGCTYAARAAC-Fluo GTGTGAACGARGTTCTGTCCCGCCGTAARTTYAARAAC-Fluo LCRed-640-CTTAYGARTAYGARGTTTCTTGGITITTGGGTGA GAAC-Pho LCRed-640-CTTAYGAATATGAAATTGGITGGTAYTTRGKTGA GAAC-Pho LCRed-640-CYTAYGARTAYGAITGTTCTTTCACTTTGGGTGA GAAC-Pho 25 Zielregion STA1-3 Gen STA1-3 Gen IAK EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen 2 Material und Methoden Tab. 2.15: Fortsetzung Bezeichnung Yfr4 Yfr5 Yfr7 Yfr8 Sequenz 5´-3´ LCRed-640-CYTAYGARTAYGARTGTTCTTTCTTGTTIGGTGA GAAC-Pho LCRed-640-TACGARTACGAARTITCITTCAARGGTCTWTCWT CTGC-Pho LCRed-640-TWCGAGTACGAGGTIWCSTTCAAGGSIMTGT CGTC-Pho LCRed-640-CTTAYGARTAYGARGTCTCGTACCTGCTCGGAGA CAAC-Pho Zielregion EF-3 Gen EF-3 Gen EF-3 Gen EF-3 Gen LCRed-640 oder 705: LightCycler®-Red-640 oder 705 Fluorophor, Pho: Phosphat, Fluo: Fluorescein 2.4 Probenmatrices Tab. 2.16: Getränkeproben Getränk Alkoholfreies Bier (Jever Fun) Alkoholfreies Bier Apfelsaft (naturtrüb, Direktsaft) Apfelsaft (klar) Biermixgetränk (Bibop) Coca-Cola Eistee (Tropical Mango) Gatorade Light Bier Orangensaft Pils Pils Radler Rotwein (Chianti) Schwarzbier (Köstritzer) Traubensaft Weißwein (Riesling) Hersteller Jever Bitburger Dietz Kaufland Bitburger Coca-Cola Nestle Pepsi-Cola Bitburger Kaufland Oettinger Bitburger Oettinger Italien Bitburger Kaufland Deutschland Tab. 2.17: Nährmedien Medium SSL-Bouillon SSL-Bouillon/alkoholfreies Bier (50/50 v/v) NBB-Bouillon MRSF-Bouillon (MRS-Bouillon mit 1 % Fructose und 1/3 Anteil alkoholfreies Pils) Tab. 2.18: Prozessproben von Brauerei A Probe Vorwürze Würze (Pfanne voll) Würze (Plattenkühler-Auslauf) Retourwasser/ Vorspülwasser Gär- und Lagerkeller Desinfektionsmittelwanne Jungbier (Lagerkeller) Wasser aus Kastenwäscher 26 Hersteller Döhler Brauerei D Brauerei D Brauerei D 2 Material und Methoden 2.5 Anzucht von Mikroorganismen Die Hefen wurden bei 25 bis 28 °C in 20 ml YM-Medium auf einem Schüttler (150 U/min) für 48 Stunden angezogen. Die Schimmelpilze wurden bei 25 bis 28 °C auf YM-Agarplatten für sieben Tage kultiviert. Die Bakterien wurden je nach Spezies in CASO-Bouillon oder MRSBouillon bei Temperaturen zwischen 30 und 37 °C für 24 Stunden angereichert. 2.6 Extraktion von Nucleinsäuren 2.6.1 Mechanisch/thermische DNA-Extraktion 1 ml einer Flüssiganreicherung oder Probe wurden in einem Reaktionsgefäß zusammen mit Zirkonium/Glas-Kügelchen [Roth] 1 min bei 8000 x g (Hefen und Schimmelpilze) oder 5 min bei 10000 x g (Bakterien) zentrifugiert. Für Bakterienkulturen wurden 150 mg Zirkonium/Glas-Kügelchen mit einem Durchmesser von 0,1 mm und für Hefe- und Schimmelpilzkulturen 500 mg Zirkonium/Glas-Kügelchen mit einem Durchmesser von 0,5 mm verwendet. Die sedimentierten Zellen wurden mit 200 µl einer 5 %-igen (w/w) Chelex® 100 [Bio-Rad] Lösung resuspendiert und 10 min bei 95 °C inkubiert. Anschließend erfolgte der mechanische Aufschluss mit dem MagNA Lyser Instrument [Roche Diagnostics] für 1 min bei 6500 Einheiten oder alternativ mit dem Disruptor Genie Instrument [Scientific Industries] für 10 min. Abschließend wurden die Zelllysate 15 min bei 95 °C inkubiert und 5 min bei 13000 x g zentrifugiert. Die Proben wurden direkt in der PCR eingesetzt, bei -20 °C gelagert oder wie unter 2.6.2 beschrieben weiter aufgereinigt. 2.6.2 Extraktion quantifizierbarer und RNA-freier DNA Quantifizierbare/RNA-freie DNA wurde präpariert, indem sich an die unter 2.6.1 beschriebene Methode eine Aufreinigung mit dem „High Pure PCR Template Preparation Kit“ [Roche Diagnostics] anschloss, wobei die in dem Protokoll für die Zelllyse und den Proteinase K Verdau vorgesehenen Schritte ausgelassen wurden. Nach dieser Aufreinigung wurden die in 50 µl eluierten Nucleinsäuren mit 1 µl RNase A (10 mg/ml) [Sigma-Aldrich] 10 min bei 37 °C inkubiert. Die RNase A wurde aus den Proben durch eine erneute Aufreinigung mit dem „High Pure PCR Template Preparation Kit“ entfernt. Das endgültige Elutionsvolumen betrug 50 µl. Verdünnungen der DNA wurden für PCR Experimente mit Heringssperma-TE-Puffer (10,0 µg/ml Heringssperma DNA [Roche Diagnostics], 0,5 mM EDTA [Sigma-Aldrich], 1,0 mM Tris-HCl [Sigma-Aldrich], pH=7,6) hergestellt. 2.6.3 Erweiterte, mechanisch/thermische DNA-Extraktion Die unter 2.6.1 beschriebene Methode wurde für komplexe Probenmatrices erweitert, wobei bis auf Isopropanol (absolut) [Roth] alle eingesetzten Komponenten aus dem „High Pure PCR Template Preparation Kit“ [Roche Diagnostics] stammten. Die sedimentierten Proben wurden zusätzlich zu den 200 µl der 5 %-igen (w/w) Chelex® 100 Suspension mit 200 µl Bindepuffer und 40 µl Proteinase K versetzt, resuspendiert und 10 min bei 72 °C inkubiert. Anschließend wurde wie unter 2.6.1 beschrieben verfahren. Die abschließende Aufreinigung erfolgte nach Zugabe von 100 µl Isopropanol mit dem „High Pure PCR Template Preparation Kit“ den Herstellerangaben entsprechend. Das Elutionsvolumen betrug 50 µl. 27 2 Material und Methoden 2.7 Konzentrationsbestimmung von DNA-Lösungen 2.7.1 Fluorometrische Bestimmung Die Konzentration von RNA-freien DNA-Lösungen wurde fluorometrisch mit dem „PicoGreen® dsDNA Quantification Kit“ [Molecular Probes] und dem LightCycler® 2.0 Instrument [Roche Diagnostics] bestimmt. Das „PicoGreen dsDNA quantification reagent“ wurde für die Messung 1:50 mit 1 x TE-Puffer verdünnt und je 15 µl in eine LightCycler® Kapillare [Roche Diagnostics] pipettiert. Nach Zugabe von 5 µl der DNA-Probe oder 5 µl der dekadisch verdünnten Lambda Standard DNA (Konzentrationsbereich: 10 ng–10 pg) wurden die Proben mit dem LightCycler® 2.0 Instrument gemessen. Die Messung erfolgte bei 530 nm mit folgendem Programm: Analysis Mode Cycles None 1 Quantification 20 None 1 Target Temperature Incubation 40 °C Fluorescence Measuring 40 °C Ending 40 °C Segment Ramp Rate 20 °C/s 20 °C/s 20 °C/s Hold Time 10 s 1s 30 s Acquisition Mode None Single None Alle weiteren Einstellungen wurden auf 0 gesetzt. Die Auswertung erfolgte mit der Analysenmethode „Nucleic Acid Quantification“ der LightCycler® Software 4.0. Die Standardgerade wurde mit der als Standard eingesetzten Lambda DNA berechnet. Die Konzentration der DNA-Proben musste zur Berechnung innerhalb des Bereichs der Standardgeraden liegen. 2.7.2 Konzentrationsbestimmung über Absorptionsspektrometrie Die Konzentrationsbestimmung über die Messung der optischen Dichte (OD) bei einer Wellenlänge von 260 nm wurde bei gereinigter Plasmid-DNA und zur Kontrolle von Oligonucleotiden angewendet. Die Messungen erfolgten mit dem Ultrospec 4000 Photometer UV/Visible Spectrophotometer der Firma Pharmacia Biotech. Ein OD-Wert von 1 entspricht bei einer Wellenlänge von 260 nm einer DNA-Konzentration von 50 µg/ml. 2.8 Agarosegelelektrophorese PCR-Fragmente, DNA-Extraktionen, gereinigte und linearisierte Plasmide wurden je nach Größe zur Kontrolle in 1 bis 2 %-igen (w/v) Agarosegelen [Biozym] der Größe nach bei einer angelegten Spannung zwischen 100 und 120 V elektrophoretisch aufgetrennt. Die Proben wurden zum Auftragen mit 1/5 (v/v) Ladepuffer (0,25 % (w/w) Bromphenolblau [Merck], 0,25 % (w/w) Xylencyanol FF [Sigma-Aldrich], 30,0 % (w/w) Glycerin [Roth]) versetzt. 1 x TBE-Puffer (90 mM Tris-Borat, 2,0 mM EDTA, pH=8,3 bei 25 °C) [Merck] wurde als Elektrophoresepuffer und der DNA-Längenstandard VI (154, 220, 234, 298, 394, 453, 517, 653, 1033, 1230, 1766 und 2176 bp) [Roche Diagnostics] zur Größenbestimmung verwendet. Die DNA-Banden wurden durch Anfärbung mit dem Fluoreszenzfarbstoff Ethidiumbromid (0,3 µg/ml) [Merck] und Bestrahlung bei 312 nm mit dem Gel-Dokumentationssystem E.A.S.Y Win32 [Herolab] sichtbar gemacht und dokumentiert. 28 2 Material und Methoden 2.9 Klonierung von PCR-Fragmenten 2.9.1 Erzeugung von PCR-Fragmenten für die Klonierung PCR-Fragmente für die Klonierung wurden mit dem Themocycler GeneAmp 9700 [Perkin Elmer] erzeugt. Eingesetzt wurden entweder die Super Taq DNA-Polymerase [HT Biotechnology], die FastStart Taq DNA-Polymerase [Roche Diagnostics] oder die Taq DNAPolymerase [Biomaster] inklusive des jeweiligen 10 x PCR-Puffers. Die Aktivität der eingesetzten Super Taq DNA-Polymerase [HT Biotechnology] wurde vor der Zugabe zum MasterMix (alle Komponenten ohne DNA) mit dem TaqStart® Antikörper [Clontech Laboratories] den Herstellerangaben folgend blockiert. Die Aktivierung der Taq DNA-Polymerase erfolgte durch einen einleitenden Temperaturschritt bei 95 °C für 5 min. Die Nucleotide (dATP, dCTP, dGTP und dTTP) stammten von der Firma Roche Diagnostics und das MgCl2 wurde von der Firma Sigma-Aldrich bezogen. 2.9.1.1 EF-3-Gen Fragmente Die Amplifizierbarkeit der DNA-Proben wurde mit dem universalen Primerpaar ITS1/ITS4 getestet. Sequenzabschnitte des EF-3-Gens wurden für die Sequenzierung mit fünf Primerkombinationen amplifiziert. Von Hefen aus der Unterabteilung Ascomycota wurde ein PCRProdukt entweder direkt mit einem der Primerpaare HS10/HS09 und HS10/HS04 oder in einer Nested- oder Semi-Nested-PCR generiert, indem zunächst in einer separaten, vorgeschalteten PCR ein Amplifikat mit dem Primerpaar HS03/HS04 erzeugt wurde. Mit den Primerpaar HSwb1/Hsabc3 und dem Primermix HS12IV-IX/HS14/III-VIII wurde von Hefen der Unterabteilung Basidiomycota ein Amplifikat erzeugt. Das folgende PCR-Programm wurde je nach verwendeten Primern (Tab. 2.11 und Tab. 2.12) mit der geeigneten Annealingtemperatur eingesetzt: Schritt Initiale Denaturierung Denaturierung Annealing Elongation Finale Elongation Anzahl Zyklen 1 35 1 Temperatur [°C] 95 95 45 50 50 52 58 62 72 72 Zeit [min] 5,0 0,5 0,5 0,5 0,5 0,5 0,5 0,5 1,0 10,0 verwendete Primer HSwb1/HSabc3 HS03/HS04 HS10/HS04 HS10/HS09 ITS1/ITS4 HS12IV-IX/HS14/III-VIII Die Reaktionsbedingungen der PCR waren bis auf die eingesetzten Primer und Primerkonzentrationen identisch: Komponente 10 x PCR-Puffer MgCl2 (50 mM) dNTP-Mix (je 10 mM) Primer (je 100 µM) Taq DNA-Polymerase (5/6 U/µl) Template H2O Volumen 2,5 µl 1,5 µl 0,5 µl 0,6 µl 2,0 µl 2,0 µl 2,0 µl 0,6 µl 1,2 µl variabel ad. 25 µl Endkonzentration 1x 3,0 mM 0,2 mM (je Nucleotid) 1,2 µM (je Primer) 4,0 µM (je Primer) 4,0 µM (je Primer) 4,0 µM (je Primer) 0,2 µM (je Primer) 1,0 U/Reaktion 29 Primerpaar HSwb1/HSabc3 HS03/HS04 HS10/HS09 HS10/HS04 HS12IV-IX/HS14/III-VIII 2 Material und Methoden 2.9.1.2 Interne Amplifikationskontrolle und Positivkontrolle Die PCR-Fragmente für die Herstellung der internen Amplifikationskontrolle und der Positivkontrollen (IAK und PK) der beiden Real-Time PCR Nachweissysteme, die auf einer Detektion mit Hybridisierungssonden beruhten, wurden über PCR-Mutagenese, wie bei Higuchi et al. (1988) beschrieben, hergestellt. Für die Herstellung der Kontrollen wurden jeweils zwei komplementäre Mutageneseprimer (Tab. 2.14) verwendet, die entweder eine Basenfehlpaarung in die Sondenbindungsregion einfügten (PK) oder die komplette Sequenz einer Sonde durch eine neue Sequenz substituierten (IAK). Dabei wurden alle PCR-Ansätze mit dem folgenden PCR-Programm durchgeführt: Schritt Initiale Denaturierung Denaturierung Annealing Elongation Finale Elongation Anzahl Zyklen 1 35 1 Temperatur [°C] 95 95 50 72 72 Zeit [min] 5,0 0,5 0,5 1,0 10,0 Mit zwei PCR-Reaktionen wurden zunächst für jede Kontrolle zwei überlappende PCRFragmente hergestellt, die die gewünschte Veränderung gegenüber der natürlichen Sequenz am 3´- (Fragment A) bzw. am 5´-Ende (Fragment B) aufwiesen. Die Primerkombinationen für die Kontrollen waren wie folgt: Real-Time PCR-Nachweissystem Kontrolle S. cerevisiae var. diastaticus IAK PK IAK Hefen Gesamtnachweis PCR-Fragment A 5´-Primer 3´-Primer SD1f SDip1r SD1f SDpo3r HS10 Yip1r PCR-Fragment B 5´-Primer 3´-Primer SDip1f SD1r SDpo3f SD1r Yip1f HS09 Die Reaktionsbedingungen bei der Amplifikation der PCR-Fragmente A und B mit den Mutageneseprimern waren die folgenden: Komponente 10 x PCR-Puffer MgCl2 (50 mM) dNTP-Mix (je 10 mM) Primer (je 10 µM) FastStart Taq DNA Polymerase (5 U/µl) S. c. var. diastaticus (DSM 70487) DNA H2O Volumen 2,5 µl 1,5 µl 0,5 µl 5,0 µl 0,5 µl 1,0 µl ad. 25 µl Endkonzentration 1x 3,0 mM 0,2 mM (je Nucleotid) 1,0 µM (je Primer) 2,5 U/Reaktion 1,0 ng/Reaktion Die PCR-Fragmente A und B wurden mit dem QIAquick PCR Purification Kit oder dem QIAquick Gel Extraction Kit [Qiagen] gereinigt, bevor sie in der abschließenden PCR eingesetzt wurden. Die PCR, bei der durch Annealing der beiden PCR-Fragmente A und B im Bereich der Mutageneseprimer, anschließender Elongation zu einem doppelsträngigen Gesamtfragment und abschließender Amplifikation mit den im Gesamtfragment außen liegenden Primern (SD1f/SD1r oder HS10/09) das PCR-Fragment C hergestellt wurde, wurde unter den folgenden Reaktionsbedingungen durchgeführt: Komponente 10 x PCR-Puffer MgCl2 (50 mM) dNTP-Mix (je 10 mM) Primer (je 10 µM) Biomaster Taq (5 U/µl) PCR-Fragment A und B H2O Volumen 2,5 µl 1,5 µl 0,5 µl 5,0 µl 0,25 µl 2,0 µl ad. 25 µl 30 Endkonzentration 1x 3,0 mM 0,2 mM (je Nucleotid) 1,0 µM (je Primer) 1,25 U/Reaktion 2 Material und Methoden 2.9.2 Reinigung von PCR-Fragmenten für die Klonierung Die Kontrolle der Amplifikate erfolgte über Agarosegelelektrophorese (Kap. 2.8). Die PCRProdukte wurden mit dem QIAquick PCR Purification Kit gereinigt. Amplifikate, die nach der Auftrennung im Agarosegel mit einem Skalpell bei Bestrahlung mit UV-Licht (365 nm) ausgeschnitten wurden, wurden mit dem QIAquick Gel Extraction Kit [Qiagen] gereinigt. 2.9.3 Ligation von gereinigten DNA-Fragmenten PCR-Produkte wurden mit dem pGEM®-T Vector Kit [Promega] den Herstellerangaben entsprechend ligiert. Die Ligationsansätze (5 µl 2 x Puffer, 0,4 µl pGEM-T Vector, 0,8 µl T4 DNA Ligase und 3,8 µl PCR-Produkt) wurden bei 4 °C für 16 Stunden inkubiert. 2.9.4 Transformation von E. coli Zellen 2.9.4.1 Herstellung kompetenter E. coli Zellen Kompetente E. coli XL-1 Blue Zellen [Stratagene] wurden mit der Magnesium-/Calciumchlorid Methode hergestellt. Aus einer E. coli XL-1 Blue Vorkultur, die über Nacht bei 37 °C in LB-Medium (Tab. 2.8) angezogen wurde, wurden 0,5 ml in 50 ml LBMedium überimpft und mit 150 U/min bis zum Erreichen einer OD550 nm von ca. 0,5 bei 37 °C inkubiert. Alle folgenden Schritte erfolgten bei 4 °C und mit auf 4 °C gekühlten Lösungen. Die Zellen wurden nach einer Inkubation von 15 min auf Eis zentrifugiert (5000 x g, 10 min), in 20 ml 0,1 M MgCl2 resuspendiert und erneut zentrifugiert (5000 x g, 10 min). Das Zellpellet wurde in 10 ml 0,1 M CaCl2 resuspendiert, 20 min auf Eis inkubiert und erneut zentrifugiert (5000 x g, 10 min). Anschließend wurden die Zellen in 1,0 ml 0,1 M CaCl2 resuspendiert, 250 µl 87 % (v/v) Glycerin zugegeben und nach einer Inkubation von 5 min auf Eis wurden Aliquots von je 100 µl bei -80 °C eingefroren. 2.9.4.2 Transformationsansatz 100 µl kompetente E. coli XL-1 Blue Zellen wurden mit 5 µl Ligationsansatz vorsichtig gemischt und 20 min auf Eis inkubiert. Der nachfolgende Hitzeschock erfolgte bei 42 °C im Wasserbad für 2 min. Nach einer weiteren Inkubation für 10 min auf Eis wurden 500 µl SOCMedium (Tab. 2.10) zugegeben und die Ansätze 1 Stunde bei 37 °C inkubiert. 100 µl des Transformationsansatzes wurden anschließend auf LB-Platten (Tab. 2.9) ausgestrichen und 24 Stunden bei 37 °C inkubiert. Nach einer Inkubation der Platten für 2 Stunden bei 4 °C wurden die gewünschten Klone aufgrund der Blau-Weiß-Selektion ausgewählt. Da die PCRFragmente alle kleiner als 1 kbp waren, wurden neben weißen auch blaue Kolonien für die Testung ausgewählt. 2.9.4.3 Kontrolle der Transformation Der Erfolg der Klonierungen wurde mit der PCR kontrolliert, wobei die Bedingungen wie bei der Herstellung der PCR-Produkte gewählt wurden (Kap. 2.9.1). Von weißen und blauen Kolonien wurden 2,0 ml Flüssigkulturen mit LB-Medium (Tab. 2.8) mit Ampicillin (100 µg/ml) angesetzt und 24 Stunden bei 37 °C inkubiert. 100 µl der Flüssigkulturen wurden 10 min bei 95 °C inkubiert und anschließend bei 13000 x g für 5 min zentrifugiert. 1 µl des Überstandes wurde in der PCR eingesetzt und das Ergebnis über Agarosegelelektrophorese (Kap. 2.8) ausgewertet. Die Lagerung der positiven Klone erfolgte bei -80 °C in 80 % (v/v) Glycerin. 31 2 Material und Methoden 2.9.5 Präparation von Plasmid-DNA Für Sequenzierungen wurden 4 ml einer Flüssigkultur (LB-Medium mit 100 µg/ml Ampicillin, 24 Stunden, 37 °C) mit dem QIAprep Spin Miniprep Kit [Qiagen] den Herstellerangaben folgend präpariert. Die Plasmid-DNA wurde in 100 µl Elutionspuffer aufgenommen. Plasmid-DNA für die interne Amplifikationskontrolle (IAK) oder die Positivkontrollen (PK) wurden aus 50 ml Flüssigkultur (LB-Medium mit 100 µg/ml Ampicillin, 24 Stunden, 37 °C) mit dem QIAprep Spin Midiprep Kit [Qiagen] den Herstellerangaben folgend präpariert. 2.9.6 Restriktionsverdau von Plasmid-DNA Die internen Amplifikationskontrollen (IAK) und die Positivkontrollen (PK) wurden nach der Reinigung mit der Restriktionsendonuclease Sac I oder Sca I [New England BioLabs] linearisiert. 170 µl der gereinigten Plasmid-DNA wurden mit 10 µl Enzym (10 U/µl), 20 µl NE-Puffer 1 (Sac I) oder 20 µl H-Puffer (Sca I) und 2 µl BSA versetzt, 2 Stunden bei 37 °C und abschließend 20 min bei 65 °C inkubiert. Der Erfolg der Linearisierung wurde über Agarosegelelektrophorese kontrolliert (Kap. 2.8). Verdünnungen der Kontrollen wurden für den späteren Gebrauch mit Heringssperma-TEPuffer (10,0 µg/ml Heringssperma DNA [Roche Diagnostics], 0,5 mM EDTA [Sigma-Aldrich], 1,0 mM Tris-HCl [Sigma-Aldrich], pH=7,6) hergestellt und bei -20 °C gelagert. 2.10 Sequenzierung Gereinigte Plasmid-DNA mit einem Sequenzabschnitt des EF-3 Gens und die über PCRMutagenese hergestellten Kontrollen (IAK und PK) wurden von der Firma GATC Biotech mit den Standardprimern M13-forw und M13-rev sequenziert. 2.11 Sequenzanalyse Distanz Matrices und Alignments von bekannten und selbst erzeugten Sequenzen wurden mit dem Align X Programm aus dem Programmpaket Vector NTI® Suite 7.0 [InforMax] erstellt. Das Programm nutzt einen modifizierten CLUSTAL W Algorithmus (Needleman und Wunsch 1970, Thompson et al. 1994) und erstellt Stammbäume über die Neighbour-Joining Methode (Saitou und Nei 1987). Die Schmelztemperatur von Oligonucleotiden wurde mit der MeltCalcPro Software (Professional Edition, Version 2.06) berechnet (Schütz und von Ahsen 1999, von Ahsen et al. 1999). 2.12 Zellzahlbestimmung Zellzahlen von Hefekulturen wurden licht-mikroskopisch mit einer Neubauer Zählkammer bestimmt. Von einer dekadischen Verdünnungsreihe, die mit gepuffertem Peptonwasser (Tab. 2.6) hergestellt wurde, wurde die Verdünnungsstufe ausgezählt, bei der zwischen 50 und 200 Zellen in einem Großquadrat lagen. Die Zellzahl der Hefekultur ergab sich indem die vier Großquadrate ausgezählt, der Mittelwert gebildet wurde und dieser Wert mit 104 und der Verdünnungsstufe multipliziert wurde. Zusätzlich zu der Zellzahl wurden die Koloniebildenden Einheiten (KBE) mit YM-Agar Platten (Tab. 2.4) durch Ausplattieren geeigneter Verdünnungsstufen ermittelt. 32 2 Material und Methoden 2.13 Real-Time LightCycler® PCR Alle Real-Time LightCycler® PCR Versuche wurden mit einem LightCycler® 1.2 Instrument oder einem LightCycler® 2.0 Instrument in 20 µl LightCycler® Kapillaren durchgeführt und mit der LightCycler® Software 3.5 oder 4.0 ausgewertet [Roche Diagnostics]. Die spezifische Amplifikation der Target-DNA oder der Positivkontrolle wurde bei den auf dem Einsatz von Hybridisierungssonden basierenden Real-Time LightCycler® PCR-Systemen im Fluoreszenzkanal 640/Back 530 bzw. F2/Back F1 analysiert. Die spezifische Amplifikation der internen Amplifikationskontrolle wurde im Fluoreszenzkanal 705/Back 530 bzw. F3/Back F1 detektiert. Real-Time PCR-Reaktionen, die mit SYBR®-Green I [Molecular Probes] durchgeführt wurden, wurden im Fluoreszenzkanal 530 bzw. F1 ausgewertet. Die eingesetzte FastStart Taq DNA Polymerase [Roche Diagnostics] inklusive des 10 x PCR-Puffers, die Nucleotide (dATP, dCTP, dGTP, dTTP und dUTP) und BSA (bovine serum albumin) stammten von der Firma Roche Diagnostics. Eine 1 M MgCl2-Stammlösung wurde von der Firma Sigma-Aldrich bezogen. 2.13.1 Real-Time LightCycler® PCR-Programme 2.13.1.1 S. cerevisiae var. diastaticus Nachweis mit Hybridisierungssonden Das PCR-Programm zum Nachweis von S. cerevisiae var. diastaticus mit Hybridisierungssonden bestand aus folgenden vier Teilprogrammen: Teilprogramm UNG Inkubation und initiale Denaturierung Amplifikation Schmelzkurven-Analyse Kühlen Anzahl Zyklen 1 45 1 1 Analysis Mode None Quantification Melting Curves None Die Teilprogramme hatten folgende Temperaturprofile: UNG Inkubation und initiale Denaturierung Target Hold Ramp Rate [°C] [hh:mm:ss] [°C/s] 37 00:02:00 20 95 00:15:00 20 Sec. Target [°C] 0 0 Amplifikation Target [°C] 95 64 72 Hold [hh:mm:ss] 00:00:02 00:00:30 00:00:15 Ramp Rate [°C/s] 20 20 20 Sec. Target [°C] 0 50 0 Schmelzkurven-Analyse Target Hold [°C] [hh:mm:ss] 95 00:00:00 38 00:01:00 80 00:00:00 Ramp Rate [°C/s] 20 20 0.1 Sec. Target [°C] 0 0 0 Kühlung Target [°C] 40 Ramp Rate [°C/s] 20 Sec. Target [°C] 0 Hold [hh:mm:ss] 00:00:30 33 Step Size [°C] 0 0 Step Size [°C] 0 0.5 0 Step Size [°C] 0 0 0 Step Size [°C] 0 Step Delay [cycles] 0 0 Acquisition Mode None None Step Delay [cycles] 0 5 0 Acquisition Mode None Single None Step Delay [cycles] 0 0 0 Acquisition Mode None None Continuous Step Delay [cycles] 0 Acquisition Mode None 2 Material und Methoden 2.13.1.2 Hefegesamtnachweis mit Hybridisierungssonden Das PCR-Programm zum Nachweis von Hefen mit Hybridisierungssonden bestand aus folgenden vier Teilprogrammen: Teilprogramm UNG Inkubation und initiale Denaturierung Amplifikation Schmelzkurven-Analyse Kühlen Anzahl Zyklen 1 45 1 1 Analysis Mode None Quantification Melting Curves None Die Teilprogramme hatten folgende Temperaturprofile: UNG Inkubation und initiale Denaturierung Target Hold Ramp Rate [°C] [hh:mm:ss] [°C/s] 37 00:02:00 20 95 00:15:00 20 Sec. Target [°C] 0 0 Amplifikation Target [°C] 95 60 72 Hold [hh:mm:ss] 00:00:05 00:01:00 00:00:15 Ramp Rate [°C/s] 20 20 20 Sec. Target [°C] 0 40 0 Schmelzkurven-Analyse Target Hold [°C] [hh:mm:ss] 95 00:00:00 40 00:01:00 75 00:00:00 Ramp Rate [°C/s] 20 20 0.1 Sec. Target [°C] 0 0 0 Kühlung Target [°C] 40 Ramp Rate [°C/s] 20 Sec. Target [°C] 0 2.13.1.3 Hold [hh:mm:ss] 00:00:30 Step Size [°C] 0 0 Step Size [°C] 0 0.5 0 Step Size [°C] 0 0 0 Step Size [°C] 0 Step Delay [cycles] 0 0 Acquisition Mode None None Step Delay [cycles] 0 0 0 Acquisition Mode None Single None Step Delay [cycles] 0 0 0 Acquisition Mode None None Continuous Step Delay [cycles] 0 Acquisition Mode None Hefegesamtnachweis mit SYBR®-Green I Das PCR-Programm zum Nachweis von Hefen mit SYBR®-Green I [Molecular Probes] bestand aus den gleichen vier Teilprogrammen wie der Nachweis mit Hybridisierungssonden. Einige Einstellungen in den Teilprogrammen Amplifikation und Schmelzkurven-Analyse wurden jedoch angepasst: Amplifikation Target [°C] 95 62 72 Hold [hh:mm:ss] 00:00:05 00:00:30 00:00:15 Ramp Rate [°C/s] 20 20 20 Sec. Target [°C] 0 0 0 Schmelzkurven-Analyse Target Hold [°C] [hh:mm:ss] 95 00:00:00 70 00:00:30 95 00:00:00 Ramp Rate [°C/s] 20 20 0.05 Sec. Target [°C] 0 0 0 34 Step Size [°C] 0 0 0 Step Size [°C] 0 0 0 Step Delay [cycles] 0 0 0 Acquisition Mode None None Single Step Delay [cycles] 0 0 0 Acquisition Mode None None Continuous 2 Material und Methoden 2.13.2 Real-Time PCR-Ansätze Bei der Amplifikation der STA1-3 Gen-Fragmente wurde statt dTTP dUTP verwendet und bei der Amplifikation des EF-3 Gen-Fragments wurden dTTP und dUTP zu gleichen Teilen (je 0,1 mM) eingesetzt, um den Einsatz von Uracil-N-Glycosylase (UNG) (hitze-instabil, 1 U/µl) [Roche Diagnostics] zum Abbau von PCR-Produkten aus vorangegangenen PCR-Ansätzen zu ermöglichen, die versehentlich in die Reaktionen verschleppt wurden. 2.13.2.1 S. cerevisiae var. diastaticus Nachweis mit Hybridisierungssonden Komponente 10 x PCR-Puffer MgCl2 (100 mM) dNTP-Mix (je 10 mM) BSA (30 µg/µl) 3´-Primer SD1f (10 µM) 5´-Primer SD1r (10 µM) LC-Fluorescein Sonde SDF1f (10 µM) LC-Red-640 Sonde SDR1f (10 µM) LC-Red-705 Sonde LMRST1 (10 µM) Taq DNA Polymerase (5 U/µl) Uracil-DNA-Glycosylase (1 U/µl) IAK (0,2 fg/µl) Probe H2O 2.13.2.2 Volumen 2,0 µl 0,5 µl 0,4 µl 1,5 µl 1,2 µl 1,2 µl 0,1 µl 0,6 µl 0,4 µl 0,4 µl 0,1 µl 1,0 µl 5,0 µl ad. 20 µl Endkonzentration 1x 2,5 mM 0,2 mM (je Nucleotid) 2,25 µg/µl 0,8 µM 0,8 µM 0,05 µM 0,3 µM 0,2 µM 2,0 U/Reaktion 0,1 U/Reaktion 0,2 fg/Reaktion Hefegesamtnachweis mit Hybridisierungssonden Komponente 10 x PCR-Puffer MgCl2 (100 mM) dATP, dCTP, dGTP (je 10 mM) dTTP, dUTP (je 10mM) BSA (30 µg/µl) 3´-Primer-Mix Yfa1-2, HS11/I-IV, Hb6f-7f (je 10 µM) 3´-Primer Yfs1 (10µM) 5´-Primer-Mix HT1r-3r, HT5r-6r (10 µM) 5´-Primer HT4r (10 µM) LC-Fluorecein Sonden-Mix Yff1-4, 6 (je 10 µM) LC-Fluorecein Sonde Yff5 (10 µM) LC-Fluorecein Sonde Yff8 (10 µM) LC-Red-640 Sonden-Mix Yfr1-4 (je 10 µM) LC-Red-640 Sonden-Mix Yfr5, 7 (je 10 µM) LC-Red-640 Sonde Yfr8 (10 µM) LC-Red-705 Sonde LMRST1 (10 µM) Taq DNA Polymerase (5 U/µl) Uracil-DNA-Glycosylase (1 U/µl) IAK (0,5 fg/µl) Probe H2O 35 Volumen 2,0 µl 0,8 µl 1,2 µl 0,2 µl 0,5 µl 0,4 µl 0,2 µl 0,4 µl 0,2 µl 0,15 µl 0,2 µl 0,1 µl 0,3 µl 0,4 µl 0,15 µl 0,4 µl 0,4 µl 0,1 µl 1,0 µl 5,0 µl ad. 20 µl Endkonzentration 1x 4,0 mM 0,2 mM (je Nucleotid) 0,1 mM (je Nucleotid) 0,75 µg/µl 0,2 µM (je Primer) 0,1 µM 0,2 µM (je Primer) 0,1 µM 0,075 µM (je Sonde) 0,1 µM 0,05 µM 0,15 µM (je Sonde) 0,2 µM (je Sonde) 0,075 µM 0,2 µM 2,0 U/Reaktion 0,1 U/Reaktion 0,5 fg/Reaktion 2 Material und Methoden 2.13.2.3 Hefegesamtnachweis mit SYBR®-Green I Komponente 10 x PCR-Puffer MgCl2 (100 mM) dATP, dCTP, dGTP (je 10 mM) dTTP, dUTP (je 10mM) BSA (30 µg/µl) 3´-Primer-Mix Ha1f-5f, Hb1f-5f (je 10 µM) 5´-Primer-Mix Ha1r-8r (10 µM) 5´-Primer-Mix Hb1r-3r (10 µM) SYBR®-Green I (100-fach) Taq DNA Polymerase (5 U/µl) Uracil-DNA-Glycosylase (1 U/µl) Probe H2O 2.14 Volumen 2,0 µl 0,7 µl 1,2 µl 0,2 µl 0,5 µl 0,4 µl 0,4 µl 0,4 µl 0,05 µl 0,4 µl 0,1 µl 5,0 µl ad. 20 µl Endkonzentration 1x 3,5 mM 0,2 mM (je Nucleotid) 0,1 mM (je Nucleotid) 0,75 µg/µl 0,2 µM (je Primer) 0,2 µM (je Primer) 0,2 µM (je Primer) 0,25-fach 2,0 U/Reaktion 0,1 U/Reaktion Spezifitätstestung der Real-Time LightCycler® PCR Die PCR-Systeme wurden mit DNA von Zielorganismen und Nicht-Zielorganismen, die mit den im Kap. 2.6.1 und Kap. 2.6.2 beschriebenen Methoden gewonnen wurde, getestet. Zusätzlich wurden die im Kap. 2.4 aufgeführten Probenmatrices, mit den DNAExtraktionsmethoden, die im Kap. 2.6.1 und Kap. 2.6.3 beschrieben wurden, getestet. 2.15 Sensitivitätstestung der Real-Time LightCycler® PCR 2.15.1 Sensitivität ermittelt mit quantifizierter, RNA-freier DNA Die Sensitivität der PCR-Systeme wurde mit quantifizierter (Kap. 2.7.1), RNA-freier DNA (Kap. 2.6.2) von Hefen bestimmt. Die Umrechnung der quantifizierten DNA-Mengen auf Genomäquivalente (GÄ) erfolgte mit den bekannten Genomgrößen von S. cerevisiae (12,1 Mbp), Schizosaccharomyces pombe (13,8 Mbp) und Cryptococcus neoformans (21,0 Mbp). 2.15.2 Sensitivität ermittelt mit dotierten Probenmatrices 10 ml Probenmatrix wurden 1:10 mit YM-Medium verdünnt und 48 Stunden bei 28 ± 2 °C auf einem Schüttler bei 150 U/min inkubiert. Die Dotierung mit ausgezählten Hefekulturen erfolgte entweder vor oder nach der Anreicherung, um die Nachweisgrenze und die Detektionszeit der PCR-Systeme zu ermitteln. Die Probenaufarbeitungen wurden mit den mechanisch/thermischen DNA-Extraktionsmethoden (Kap. 2.6.1 und Kap. 2.6.3) durchgeführt. 2.15.3 Sensitivität ermittelt bei einer hohen Begleitflora Die PCR-Systeme wurden mit Aufarbeitungen von dotierten Proben getestet, die neben den Zielorganismen eine sehr hohe Begleitflora an S. cerevisiae (DSM 1333) Zellen (S. cerevisiae var. diastaticus Nachweissystem) oder E. coli (DSM 30083) Zellen (Hefegesamtnachweissystem) aufwiesen. 1 ml einer S. cerevisiae Kultur (YM-Medium) mit 1 x 108 Zellen/ml oder 1 ml einer E. coli Kultur (Peptonwasser) mit 1 x 1010 KBE/ml wurden mit unterschiedlichen Zellzahlen der jeweiligen Zielorganismen inokuliert und mit einer der mechanisch/thermischen DNA-Extraktionsmethoden (Kap. 2.6.1 und Kap. 2.6.3) aufgearbeitet. Die Zellzahlen der Hefekulturen wurden wie im Kap. 2.12 beschrieben ermittelt. Die Zellzahl der E. coli Kultur wurde als KBE/ml mit Caso-Agar bestimmt. 36 2 Material und Methoden 2.16 Praxisnahe Testung der Real-Time PCR für S. cerevisiae var. diastaticus Das komplette S. cerevisiae var. diastaticus Real-Time PCR-System wurde von vier Brauereien (A-D) in Kombination mit der mechanisch/thermischen DNA-Extraktionsmethode (Kap. 2.6.1) getestet. Von jeder Brauerei wurden undotierte Probenmatrices aus unterschiedlichen Bereichen des Brauprozesses in zwei Probenvolumina (1,0 ml und 0,1 ml) getestet (Versuchsteil 1). Außerdem untersuchte jede Brauerei S. cerevisiae var. diastaticus Reinkulturen, die aus dem eigenen Prozess isoliert wurden oder von Kulturstammsammlungen bezogen wurden (Versuchsteil 2). Mit 4 bis 5 unterschiedlichen Probenmatrices wurde die Sensitivität des PCR-Systems nach Dotierung mit 102, 103 oder 104 Zellen/ml S. cerevisiae var. diastaticus getestet (Versuchsteil 3). Zum Einsatz kamen sowohl LightCycler® 1.2 Instrumente (Brauerei A, B und D) als auch LightCycler® 2.0 Instrumente (Brauerei B und C) [Roche Diagnostics]. Die mechanisch/thermische Probenaufarbeitung wurde bei zwei Brauereien (A und B) mit dem Disruptor Genie [Scientific Industries] und bei den beiden anderen Brauereien mit dem MagNA Lyser Instrument [Roche Diagnostics] durchgeführt. Die Brauerei A testete das PCR-System außerdem beim Versuchsteil 1 in Kombination mit Proben, die mit dem MagNA Pure DNA Isolation Kit III [Roche Diagnostics] aufgearbeitet wurden. 37 3 Ergebnisse 3 Ergebnisse 3.1 Entwicklung einer Real-Time PCR für S. cerevisiae var. diastaticus 3.1.1 Auswahl der STA1-3 Gene als Zielregionen Saccharomyces cerevisiae var. diastaticus Stämme besitzen als physiologisches Unterscheidungsmerkmal zu anderen Stämmen der gleichen Art die Fähigkeit Stärke zu Glucose, Maltose und Dextrinen abzubauen (Andrews und Gilliland 1952). Die hierfür verantwortliche extrazelluläre Glucoamylase (1,4-α-Glucosidase, EC 3.2.1.3) wird von einem von drei unabhängigen Genen der Multigen-Familie STA kodiert, die auf den Chromosomen IV (STA1), II (STA2) und XIV (STA3) im Genom angeordnet sind (Tamaki 1978, Erratt und Stewart 1978, Pretorius und Marmur 1988, Bignell und Evans 1990). Der größte Teil der codierenden Sequenz der STA Gene ist identisch mit dem Gen SGA1 (Chromosom IX), das bei allen S. cerevisiae Stämmen vorkommt und eine intrazelluläre, sporulations-spezifische Glucoamylase kodiert (Pretorius und Marmur 1988). S. cerevisiae SGA1 5´ MUC1 3´ S2 5´ 1530 bp 2538 bp S. cerevisiae var. diastaticus 5´ S1 909 bp STA 2538 bp S2 3´ 129 bp 780 bp S1 1530 bp 3´ SGA1 Abb. 3.1: Anordnung der identischen Sequenzabschnitte der Gene SGA1 und MUC1 in der STA Multigen-Familie Die Gene SGA1 und MUC1, die in allen S. cerevisiae Stämmen vorkommen, beinhalten jeweils Sequenzabschnitte, die in einer veränderten Anordnung auch in den Genen STA1-3 vorkommen. Die STA Multigen-Familie ist im Gegensatz zu den Genen SGA1 und MUC1 nur in S. cerevisiae var. diastaticus zu finden. Eine direkte Sequenzwiederholung im S1 Sequenzabschnitt von 129 bp Länge ist nicht in den STA Genen enthalten. In der Konfiguration der STA Gene kodiert die SGA1 Sequenz die katalytische Domäne und die S2-S1 Sequenzen bilden den Promotor, ein hydrophobes, membrangängiges Leaderpeptid und einen Threonin/Serin-reichen Bereich (Abbildung verändert nach Vivier et al. 1997). 38 3 Ergebnisse Die STA Gene unterscheiden sich jedoch von dem SGA1 Gen in zwei zusätzlichen Sequenzabschnitten (S1 und S2), die ein hydrophobes, membrangängiges Leaderpeptid und einen Threonin/Serin-reichen Bereich kodieren (Yamashita et al. 1985b, 1987). Diese Sequenzabschnitte S1 und S2, die in den STA Genen in der 5´-Region nebeneinander vorliegen, sind ebenfalls bei allen S. cerevisiae Stämmen im Gen MUC1 (=Flo11) (Chromosom IX) vorhanden und sind dort ca. 2,5 kbp getrennt von einander angeordnet (Lambrechts et al. 1995, 1996). Die genaue Anordnung der Genabschnitte verdeutlicht die Abbildung 3.1. 3.1.2 Anordnung der Primer und Hybridisierungssonden im STA Gen Die Sequenzen der Gene STA1 und STA2 (GenBank Acc. No. X02649.1 und X13857.1) dienten als Grundlage für die Konstruktion der Primer und Hybridisierungssonden. Der 5´Primer SD1f wurde im S1 Bereich (Position 848-868) und der 3´-Primer SD1r im SGA Bereich (Position 1086-1107) platziert, da diese Bereiche nur in den STA Genen nebeneinander angeordnet sind. Das resultierende Amplifikat hatte eine Länge von 260 bp. Die Sonden SDF1f (Position 962-991) und SDR1f (Position 994-1018) wurden so konstruiert, dass sie im Übergangsbereich zwischen den Sequenzabschnitten S1 und SGA hybridisieren. Das mit Fluorescein markierte 3´-Ende der Donator-Sonde SDF1f schloss mit dem Ende des S1 Sequenzabschnitts ab. Der Targetbereich der Akzeptor-Sonde SDR1f, die mit dem LightCycler®-Red 640 Fluorochrom am 5´-Ende markiert wurde, begann zwei Basen nach Beginn des SGA Sequenzabschnitts (Abb. 3.2). 841------------SD1f--------------------------------------------900 CTGGTACTGG CGAATACACT ACTGAAGCTA CCGCCCCTGT TACAACAGCT GTCACAACCA 901------------------------------------------------------------960 CCGTTGTTAC CACTGAATCC TCTACGGGTA CTAACTCCGC TGGTAAGACG ACAACTAGTT 961-----------SDF1f----------------------------SDR1f----------1020 ACACAACAAA GTCTGTACCA ACCACCTATG TATTTGACTT TGGCAAGGGC ATTCTCGATC 1021----------------------------------------------------------1080 AAAGCTGCGG CGGTGTATTT TCAAACAACG GCTCTTCGCA AGTGCAGCTG CGGGATGTAG 1081-----------SD1r----------1110 TCTTGATGAA TGGGACAGTG GTATACGATT Abb. 3.2: Anordnung der Primer und Hybridisierungssonden im STA1 Gen Dargestellt ist der Sequenzabschnitt des STA1 Gens (5´ - 3´ Orientierung, GenBank Acc. No. X02649.1), der bei der Real-Time PCR für S. cerevisiae var. diastaticus mit dem 5´-Primer SD1f und dem 3´-Primer SD1r amplifiziert wurde. Die Primer lagen im S1 (SD1f) bzw. SGA (SD1r) Sequenzbereich. Die Detektion der Amplifikate erfolgte mit den Hybridisierungssonden SDF1f und SDR1f, die im Übergangsbereich der S1 und SGA Sequenzabschnitte hybridisierten. 39 3 Ergebnisse 3.1.3 Konstruktion der internen Amplifikationskontrolle und der Positivkontrolle Falsch-negative Ergebnisse, die durch Inhibition von PCR-Reaktionen auftreten können, wurden durch den Einsatz einer linearisierten Plasmid-DNA, die in jeder PCR-Reaktion konkurrierend eingesetzt wurde, ausgeschlossen. Der Nachweis der Amplifikation dieser internen Amplifikationskontrolle (IAK), deren Sequenz bis auf den Austausch der Zielregion der Hybridisierungssonde SDR1f durch Einbau eines komplett neuen Sequenzabschnittes identisch mit der Sequenz des Wildtyps war, erfolgte mit der LightCycler®-Red 705 markierten Akzeptor-Sonde LMRST1. Konstruiert wurde die interne Amplifikationskontrolle über PCRMutagenese mit den Primern SDip1f und SDip1r (Kap. 2.9.1.2). Nach Ligation der PCRProdukte in den Vektor pGEM®-T (Kap. 2.9.3), Transformation in E. coli XL-1 Blue Zellen (Kap. 2.9.4.2), Kontrolle der Klone über PCR (Kap. 2.9.4.3) und Linearisierung der gereinigten Plasmide mit der Restriktionsendonuclease Sca I (Kap. 2.9.6) wurde der Erfolg der Herstellung durch Sequenzierung (Kap. 2.10) und Alignment (Kap.2.11) mit der Sequenz des STA1 Gens bestätigt (Abb. 3.3). Bei allen weiteren Versuchen wurde von der IAK je Reaktion 0,2 fg eingesetzt. IAK STA1 841-----------SD1f----------------------------------------900 -------TGGCGAATACACTACTGAAGCTACCGCCCCTGTTACAACAGCTGTCACAACCA CTGGTACTGGCGAATACACTACTGAAGCTACCGCCCCTGTTACAACAGCTGTCACAACCA IAK STA1 901-------------------------------------------------------960 CCGTTGTTACCACTGAATCCTCTACGGGTACTAACTCCGCTGGTAAGACGACAACTAGTT CCGTTGTTACCACTGAATCCTCTACGGGTACTAACTCCGCTGGTAAGACGACAACTAGTT IAK STA1 961----------SDF1f-----------------------SDR1f-LMRST1----1020 ACACAACAAAGTCTGTACCAACCACCTATGTATCATTATCCGATACGTTCTTCCAGTGCC ACACAACAAAGTCTGTACCAACCACCTATGTATTTGACTTTGGCAAGGGCATTCT---CG IAK STA1 1021-----------------------------------------------------1080 ATCAAAGCTGCGGCGGTGTATTTTCAAACAACGGCTCTTCGCAAGTGCAGCTGCGGGATG ATCAAAGCTGCGGCGGTGTATTTTCAAACAACGGCTCTTCGCAAGTGCAGCTGCGGGATG IAK STA1 1081-----------SD1r----------------------------1130 TAGTCTTGATGAATGGGACAGTGGTATACG-------------------TAGTCTTGATGAATGGGACAGTGGTATACGATTCAAACGGCGCTTGGGAC Abb. 3.3: Sequenzvergleich der IAK mit dem STA1 Gen Das Alignment zeigt die Sequenzen der IAK des Real-Time PCR Nachweissystems für S. cerevisiae var. diastaticus und die Wildtyp Sequenz des STA1 Gens (GenBank Acc. No. X02649.1). Die Primer SD1f und SD1r sowie die Hybridisierungssonde SDF1f waren für beide Sequenzen spezifisch. Die Hybridisierungssonde SDR1f war für die Wildtyp-Sequenz und die Sonde LMRST1 für die IAKSequenz spezifisch. Die Markierung der Sonden SDR1f und LMRST1 mit unterschiedlichen Fluoreszenzfarbstoffen ermöglichte eine Unterscheidung zwischen IAK und Wildtyp Amplifikaten in der PCR. 40 3 Ergebnisse Mit dem Einsatz einer Positivkontrolle (PK) können die eingesetzten Reagenzien und die Herstellung des PCR-Mixes kontrolliert werden. Die PK wurde auf die gleiche Weise wie die IAK hergestellt (Kap. 2.9.1.2), jedoch wurde nicht die gesamte Zielsequenz einer Sonde ausgetauscht, sondern im Targetbereich der Sonde SDF1f eine Punktmutation eingefügt (Abb. 3.4). Durch diese Punktmutation war eine Differenzierung zwischen der PK und positiven Ergebnissen über die Schmelzkurven-Analyse im Kanal 640/Back 530 möglich. Diese Differenzierung war notwendig, um ein positives Ergebnis, das durch Verschleppung von Plasmid-DNA der PK in den Reaktionsansatz zustande kommen könnten, sicher ausschließen zu können. Die Hybridisierungsonde SDF1 schmolz ca. 4 °C früher vom Amplifikat der PK ab als beim Wildtyp (Abb. 3.5). Die PK war über den Schmelzhöchstwert (Maximum der negativen ersten Ableitung der Fluoreszenz, aufgenommen über die Temperatur, -(d/dT)) bei ca. 58 °C deutlich von positiven Proben zu unterscheiden, bei denen die Sonde SDF1f ab 62 °C abschmolz. In der Real-Time PCR wurden 5 fg je Reaktion eingesetzt. PK STA1 841-----------SD1f----------------------------------------900 -------TGGCGAATACACTACTGAAGCTACCGCCCCTGTTACAACAGCTGTCACAACCA CTGGTACTGGCGAATACACTACTGAAGCTACCGCCCCTGTTACAACAGCTGTCACAACCA PK STA1 901-------------------------------------------------------960 CCGTTGTTACCACTGAATCCTCTACGGGTACTAACTCCGCTGGTAAGACGACAACTAGTT CCGTTGTTACCACTGAATCCTCTACGGGTACTAACTCCGCTGGTAAGACGACAACTAGTT PK STA1 961----------SDF1f-------------------------SDR1f---------1020 ACACAACAAAGGCTGTACCAACCACCTATGTATTTGACTTTGGCAAGGGCATTCTCGATC ACACAACAAAGTCTGTACCAACCACCTATGTATTTGACTTTGGCAAGGGCATTCTCGATC PK STA1 1021-----------------------------------------------------1080 AAAGCTGCGGCGGTGTATTTTCAAACAACGGCTCTTCGCAAGTGCAGCTGCGGGATGTAG AAAGCTGCGGCGGTGTATTTTCAAACAACGGCTCTTCGCAAGTGCAGCTGCGGGATGTAG PK STA1 1081----------SD1r-----------------------------1130 TCTTGATGAATGGGACAGTGGTATACG----------------------TCTTGATGAATGGGACAGTGGTATACGATTCAAACGGCGCTTGGGACAGT Abb. 3.4: Sequenzvergleich der PK mit dem STA1 Gen Das Alignment zeigt die Sequenzen der PK des Real-Time PCR Nachweissystems für S. cerevisiae var. diastaticus und die Wildtyp Sequenz des STA1 Gens (GenBank Acc. No. X02649.1). Die Primer SD1f und SD1r sowie die Hybridisierungssonde SDR1f waren für beide Sequenzen spezifisch. Die Hybridisierungssonde SDF1f war für die Wildtyp Sequenz 100-%ig spezifisch. Bei der PK bestannt im Bereich der Bindungsstelle der Sonde SDF1f die Nucleotidfehlbindung T:C. Bei der SchmelzkurvenAnalyse verminderte diese Fehlbindung zwischen den Amplifikaten der PK und der Sonde SDF1f die Schmelztemperatur gegenüber dem Wildtyp um ca. 4 °C, sodass eine klare Abtrennung zwischen positiven Proben und der PK möglich war. 41 3 Ergebnisse Abb. 3.5: Differenzierung zwischen der PK und positiven Proben bei der Real-Time PCR für S. cerevisiae var. diastaticus Dargestellt ist die Schmelzkurven-Analyse im Kanal 640/Back 530, die bei der Real-Time PCR für S. cerevisiae var. diastaticus eine Differenzierung zwischen der PK und positiven Proben zuließ. Die Real-Time PCR wurde mit 2500 GÄ (blaue Linie), 1000 GÄ (grüne Linie), 100 GÄ (rote Linie) und 10 GÄ (blaue Punkte) quantifizierter, RNA-freier DNA (Kap. 2.6.2) von S. cerevisiae var. diastaticus (DSM 70487) durchgeführt. Von der PK wurden 5 fg (schwarze Linie) eingesetzt und als Negativkontrolle wurde PCR-H2O (rote Punkte) verwendet. 3.1.4 Spezifität der Real-Time PCR für S. cerevisiae var. diastaticus Die Spezifität der Real-Time PCR wurde mit 25 S. cerevisiae var. diastaticus Stämmen, 24 weiteren Saccharomyces Stämmen, 32 anderen, brauereirelevanten Hefearten und 18 Bakterienarten getestet. Nur die 25 S. cerevisiae var. diastaticus Stämme wurden nach mechanisch/thermischer DNA-Extraktion (Kap. 2.6.1) mit dem System qualitativ nachgewiesen (Tab. 3.1 und Abb. 3.6). Die Cp-Werte der Isolate lagen zwischen 15 und 25, da nicht quantifizierte DNA eingesetzt wurde. Detaillierte Angaben zu den getesteten Stämmen zeigt die Tabelle 6.1 im Anhang. Die IAK wurde in allen Reaktionsansätzen, die negativ im Kanal 640/Back 530 waren, amplifiziert und wurde demnach nicht durch eine konkurrierende Bildung unspezifischer Amplifikate unterdrückt. Die Schmelzkurven-Analyse zeigte, dass bei allen Stämmen die Sonden ihren Schmelzhöchstwert, bei der die Fluoreszenzabnahme ein Maximum erreichte, bei ca. 62 °C hatten (Abb. 3.6). 42 3 Ergebnisse Tab. 3.1: Spezifität der Real-Time PCR für S. cerevisiae var. diastaticus Getestete Gruppen Anteil positiv getesteter Stämme S. cerevisiae var. diastaticus 25/25 nicht-diastaticus Saccharomyces sp. 0/24 weitere Hefearten 0/32 Bakterienarten 0/18 Die Testung erfolgte mit DNA-Proben, die mit der mechanisch/thermischen Extraktionsmethode gewonnen wurden (Kap. 2.6.1). Angegeben wurde die Anzahl an Stämmen, die mit der Real-Time PCR für S. cerevisiae var. diastaticus nachgewiesen wurden, an der Gesamtheit der getesteten Stämme. Abb. 3.6: Amplifikation und Schmelzkurven-Analyse des STA Genfragments von S. cerevisiae. var. diastaticus Stämmen Die Real-Time PCR wurde mit DNA von 25 S. cerevisiae var. diastaticus Stämmen (blaue Linien) getestet. Die DNA-Extraktion erfolgte mit der mechanisch/thermischen Methode (Kap. 2.6.1), nachdem die S. c. var. diastaticus Stämme 48 Stunden in YM-Medium angezogen wurden. Zur Kontrolle der PCR wurden 5 fg der PK (schwarze Linie) eingesetzt. Als Negativkontrolle (rote Linie) wurde undotiertes YM-Medium zusammen mit den Hefestämmen aufgearbeitet und in der PCR eingesetzt. Die Versuche zur Spezifität wurden auch ohne IAK durchgeführt und anschließend über Agarosegelelektrophorese aufgetrennt, um die Länge der gebildeten Amplifikate zu kontrollieren und mögliche unspezifische PCR-Produkte zu detektieren. Die IAK wurde bei diesen Versuchen nicht eingesetzt, da das gebildete Fragment mit 263 bp fast die gleiche Länge wie das beim Wildtyp gebildete Amplifikat hatte und demnach über Agarosegelelektrophorese nicht von diesem zu unterscheiden gewesen wäre. Die mit DNA von S. cerevisiae var. diastaticus amplifizierten PCR-Produkte hatten alle eine Länge von 260 bp. Bei den getesteten „Nicht“Targetorganismen wurde keine Amplifikation beobachtet. Die Abbildung 3.7 zeigt Agarosegelelektrophorese Ergebnisse nach Real-Time PCR mit DNA einiger S. cerevisiae var. diastaticus Stämme (Typstämme und Brauereiisolate) und nahe verwandter Saccharomyces sp.. 43 3 Ergebnisse Abb. 3.7: Agarosegelelektrophorese nach Real-Time PCR mit dem S. cerevisiae var. diastaticus System Die Real-Time PCR wurde ohne IAK und mit DNA-Proben, die mit der mechanisch/thermischen Extraktionsmethode gewonnen wurden (Kap. 2.6.1), durchgeführt. Die Agarosegelelektrophorese wurde mit je 5 µl der Reaktionsansätze in einem 2-%igen Gel durchgeführt (Kap. 2.8). A.: 1: Molekulargewichtsmarker VI 2: Saccharomyces cerevisiae (DSM 1333) 3: S. cerevisiae var. diastaticus (BCD 1257) 4: Saccharomyces exiguus (BCD 1491) 5: Saccharomyces exiguus (BCD 1493) 6: S. cerevisiae var. diastaticus (VTT C-68059) 7: S. cerevisiae var. diastaticus (VTT C-70060) 8: S. cerevisiae var. diastaticus (VTT C-82101) 9: Saccharomyces pastorianus (DSM 6580) 10: Saccharomyces bayanus (DSM 70412) 11: S. cerevisiae var. diastaticus (DSM 70487) 12: Negativkontrolle B.: 1: Molekulargewichtsmarker VI 2: S. cerevisiae (Brauerei D, Brauhefe) 3: S. cerevisiae var. diastaticus (Brauerei D) 4: S. cerevisiae var. diastaticus (Brauerei D) 5: S. cerevisiae var. diastaticus (Brauerei B) 6: S. cerevisiae var. diastaticus (Brauerei B) 7: S. cerevisiae var. diastaticus (Brauerei A) 8: S. cerevisiae var. diastaticus (Brauerei A) 9: S. cerevisiae var. diastaticus (Brauerei A) 10: S. cerevisiae var. diastaticus (Brauerei A) 11: S. cerevisiae var. diastaticus (Brauerei A) 12: S. cerevisiae var. diastaticus (Brauerei A) 13: S. cerevisiae var. diastaticus (BCD 1257) 14: Negativkontrolle 44 3 Ergebnisse Die Anwendbarkeit des Enzyms Uracil-N-Glycosylase (UNG), das zum Abbau von Amplifikaten aus vorherigen Reaktionen bei jeder PCR-Reaktion eingesetzt wurde, wurde mit aufgereinigten (Kap. 2.9.2) und quantifizierten Amplifikaten (Kap. 2.7.2) von S. c. var. diastaticus (DSM 70487) getestet. Amplifikatmengen zwischen 103 und 107 Amplifikaten je Reaktion wurden mit der UNG vollständig abgebaut und die Kontrollen ohne UNG wurden alle amplifiziert (Tab. 3.2). Tab. 3.2: Abbaubarkeit von Amplifikaten des STA Gens mit dem Enzym UNG Amplifikatmenge [Kopien/Reaktion] 103 104 105 106 107 Cp-Werte im Kanal 640/Back 530 ohne UNG mit UNG 28,13 negativ 25,05 negativ 20,70 negativ 17,96 negativ 14,97 negativ Die Real-Time PCR für S. cerevisiae var. diastaticus wurde mit bzw. ohne 0,1 U/Reaktion UNG mit unterschiedlichen Mengen an Amplifikaten des STA Gens von S. cerevisiae var. diastaticus durchgeführt. Die Amplifikate wurden zuvor aufgereinigt und quantifiziert (Kap. 2.9.2 und 2.7.2). 3.1.5 Sensitivität der Real-Time PCR für S. cerevisiae var. diastaticus Die Sensitivität der Real-Time PCR wurde mit fluorometrisch quantifizierter, RNA- und Protein-freier DNA (Kap. 2.6.2 und Kap. 2.7.1) der S. cerevisiae var. diastaticus Stämme DSM 70487 und VTT C-82101 getestet. Außerdem wurde das System unter Einbeziehung der mechanisch/thermischen DNA-Extraktion mit dotiertem YM-Medium evaluiert. Das YMMedium wurde mit 102, 103 oder 104 Zellen/ml S. cerevisiae var. diastaticus (DSM 70487) und zusätzlich mit 108 Zellen/ml S. cerevisiae (DSM 1333) dotiert (Kap. 2.15.3). Mit den S. cerevisiae Zellen als Begleitflora wurde getestet, ob sich eine lineare Amplifikation aufgrund der auch bei S. cerevisiae vorhandenen Bindungssequenzen der Primer SD1f und SD1r in den Genen SGA1 und MUC1 störend auf das PCR-System auswirkt. Beide Instrumente für den mechanischen Zellaufschluss (MagNA Lyser und Disruptor Genie) wurden getestet. Die mit quantifizierter DNA ermittelte Nachweisempfindlichkeit des PCR-Systems lag zwischen 5 (96 % positive Proben) und 10 (100 % positive Proben) Genomäquivalenten pro Reaktionsansatz (Tab. 3.3 und Abb. 3.8). 1 GÄ wurde noch in 11 von 24 getesteten Proben nachgewiesen. Bei einer angenommenen Genomgröße von S. cerevisiae von 12,2 Mbp (GenBank) entsprach 1 GÄ 13,3 fg DNA. Unterschiede zwischen den ermittelten CpMittelwerten der beiden untersuchten S. cerevisiae var. diastaticus Stämme wurden nicht festgestellt. 45 3 Ergebnisse Tab. 3.3: Sensitivität der Real-Time PCR für S. cerevisiae var. diastaticus S. c. var. diastaticus Stamm DSM 70487 VTT C-82101 DNA Konzentration Anteil positiver [GÄ/Reaktion] Proben Cp-Mittelwerte (640/Back 530) 1000 100 50 25 10 5 1 1000 100 50 25 10 5 1 27,59 ± 0,17 30,64 ± 0,16 31,49 ± 0,28 32,19 ± 0,31 32,85 ± 0,44 32,95 ± 0,34 33,29 ± 0,79 27,81 ± 0,28 30,87 ± 0,22 31,63 ± 0,24 32,35 ± 0,40 32,99 ± 0,58 33,04 ± 0,35 33,31 ± 0,98 12/12 = 100 % 12/12 = 100 % 12/12 = 100 % 12/12 = 100 % 12/12 = 100 % 12/12 = 100 % 6/12 = 50 % 12/12 = 100 % 12/12 = 100 % 12/12 = 100 % 12/12 = 100 % 12/12 = 100 % 11/12 = 92 % 5/12 = 42 % Die Real-Time PCR für S. cerevisiae var. diastaticus wurde mit quantifizierter, RNA-freier DNA (Kap. 2.6.2) von zwei S. cerevisiae var. diastaticus Stämmen (DSM 70487 und VTT C-82101) getestet. Abb. 3.8: Sensitivität der Real-Time PCR für S. cerevisiae var. diastaticus Dargestellt sind die Amplifikationskurven im Kanal 640/Back 530, die mit der Real-Time PCR für S. cerevisiae var. diastaticus mit 1000 GÄ (schwarze Linie), 100 GÄ (rote Linie), 50 GÄ (grüne Linie), 25 GÄ (baue Linie), 10 GÄ (schwarze Punkte), 5 GÄ (rote Punkte) und 1 GÄ (grüne Punkte) quantifizierter, RNA-freier DNA (Kap. 2.6.2) von S. cerevisiae var. diastaticus (DSM 70487) generiert wurden. Als Negativkontrolle wurde PCR-H2O (blaue Punkte) verwendet. 46 3 Ergebnisse Die Sensitivität des Real-Time PCR-Systems unter Einbeziehung der Probenaufarbeitung und bei einem Hintergrund von 108 Zellen/ml S. cerevisiae lag zwischen 102 und 103 Zellen/ml (Tab. 3.4 und Abb. 3.9). Umgerechnet auf das in der PCR eingesetzte Probenvolumen von 5 µl entsprach dies ca. 2,5 bis 25 GÄ pro Reaktionsansatz, wenn eine 100-%ige DNAExtraktion vorausgesetzt wird. Durch die mechanisch/thermische DNA-Extraktion oder die Begleitflora entstanden demnach keine Sensitivitätsverluste. Beide Instrumente waren für den mechanischen Zellaufschluss (MagNA Lyser oder Disruptor Genie) geeignet. Über die Schmelzkurven-Analyse waren positive Proben von der PK zu unterscheiden (Abb. 3.9). Tab. 3.4: Sensitivität der Real-Time PCR für S. cerevisiae var. diastaticus bei einer hohen Begleitflora Instrument MagNA Lyser Disruptor Genie S. c. var. diastaticus [Zellen/ml] 104 103 102 104 103 102 Anteil positiver Proben 6/6 = 100 % 6/6 = 100 % 4/6 = 67 % 6/6 = 100 % 6/6 = 100 % 3/6 = 50 % Cp-Mittelwerte (640/Back 530) 31,13 ± 0,40 33,05 ± 0,19 33,82 ± 0,30 30,58 ± 0,63 33,43 ± 0,99 34,52 ± 0,75 Die Real-Time PCR für S. cerevisiae var. diastaticus wurde mit dotierten Proben, die mechanisch/thermisch mit dem MagNA Lyser oder Disruptor Genie Instrument aufgearbeitet wurden, getestet (Kap. 2.6.1). Hierfür wurde YM-Medium mit 108 Zellen/ml S. cerevisiae (DSM 1333) und der jeweiligen Konzentration an S. cerevisiae var. diastaticus (DSM 70487) dotiert. Abb. 3.9: Sensitivität der Real-Time PCR für S. cerevisiae var. diastaticus bei einer hohen Begleitflora Dargestellt sind die Amplifikationskurven (links) und die Schmelzkurven-Analyse (rechts), die mit der Real-Time PCR für S. cerevisiae var. diastaticus und mechanisch/thermisch aufgearbeiteten, dotierten Proben (Kap. 2.6.1) generiert wurden. Die Proben (YM-Medium) waren mit 104 Zellen/ml (grüne Linie), 103 Zellen/ml (rote Linie), 102 Zellen/ml (blaue Linie) S. cerevisiae var. diastaticus (DSM 70487) dotiert. Alle Proben waren zusätzlich mit 108 Zellen/ml S. cerevisiae (DSM 1333) dotiert. Als Kontrollen wurden eine undotierte Probe (grüne Punkte) und die PK (schwarze Linie) mitgeführt. 47 3 Ergebnisse Die Amplifikation der internen Amplifikationskontrolle wurde in Proben, die nur mit 108 Zellen/ml S. cerevisiae dotiert wurden, nicht negativ beeinflusst (Tab. 3.5). Tab. 3.5: Amplifikation der IAK der Real-Time PCR für S. cerevisiae var. diastaticus bei einer hohen Begleitflora Instrument S. cerevisiae [Zellen/ml] Anteil positiver Proben Cp-Mittelwerte (705/Back 530) MagNA Lyser 108 8/8 = 100 % 33,90 ± 0,80 8 8/8 = 100 % 34,29 ± 0,52 Disruptor Genie 10 Die IAK der Real-Time PCR für S. cerevisiae var. diastaticus wurde mit Proben (YM-Medium), die mit 108 Zellen/ml S. cerevisiae (DSM 1333) dotiert und mechanisch/thermisch mit dem MagNA Lyser oder Disruptor Genie Instrument aufgearbeitet wurden, getestet (Kap. 2.6.1). 3.1.6 Kompatibilität der Real-Time PCR für S. cerevisiae var. diastaticus mit unterschiedlichen Probenmatrices Die Real-Time PCR für S. cerevisiae var. diastaticus wurde mit 16 unterschiedlichen Anreicherungsmedien, Prozessproben und Endprodukten getestet (Herkunft siehe Kap. 2.4). Dotiert wurden je 1 ml Probe mit 103 oder 104 Zellen/ml S. cerevisiae var. diastaticus (DSM 70487). Die mechanisch/thermische Aufarbeitung der Proben erfolgte zum Vergleich mit dem MagNA Lyser und Disruptor Genie Instrument. 104 Zellen/ml wurden in allen Probenmatrices unabhängig vom verwendeten Probenaufarbeitungsinstrument 100-%ig nachgewiesen (Tab. 3.6). 103 Zellen/ml waren in den Proben SSL Bouillon, Desinfektionsmittelwanne, Pils (Bitburger), Biermixgetränk (Bibop) im Gegensatz zu den restlichen Probenmatrices nicht 100-%ig nachweisbar. Tab. 3.6: Eignung der Real-Time PCR für S. cerevisiae var. diastaticus in Kombination mit der mechanisch/thermischen Aufarbeitung für unterschiedliche Probenmatrices Probenmatrix SSL-Bouillon SSL-Bouillon/alkoholfreies Bier (50/50 v/v) NBB-Bouillon MRSF-Bouillon Vorwürze Würze (Pfanne voll) Instrument MagNA Lyser Disruptor Genie MagNA Lyser Disruptor Genie MagNA Lyser Disruptor Genie MagNA Lyser Disruptor Genie MagNA Lyser Disruptor Genie MagNA Lyser Disruptor Genie 48 Anteil positiver Proben im Kanal 640/Back 530 104 Zellen/ml 103 Zellen/ml 3/3 = 100 % 0/3 = 0 % 3/3 = 100 % 2/3 = 67 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3 Ergebnisse Tab. 3.6: Fortsetzung Probenmatrix Instrument Würze (PlattenkühlerAuslauf) MagNA Lyser Disruptor Genie MagNA Lyser Disruptor Genie MagNA Lyser Disruptor Genie MagNA Lyser Disruptor Genie MagNA Lyser Disruptor Genie MagNA Lyser Disruptor Genie MagNA Lyser Disruptor Genie MagNA Lyser Disruptor Genie MagNA Lyser Disruptor Genie MagNA Lyser Disruptor Genie Retourwasser Desinfektionsmittelwanne Jungbier Wasser aus Kastenwäscher Pils (Bitburger) Light Bier (Drive) Biermixgetränk (Bibop) Schwarzbier (Köstritzer) Alkoholfreier Bier Anteil positiver Proben im Kanal 640/Back 530 103 Zellen/ml 104 Zellen/ml 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 1/3 = 33 % 3/3 = 100 % 0/3 = 0 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 2/3 = 67 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 2/3 = 67 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 3/3 = 100 % 1ml der jeweiligen Probenmatrix wurden mit 103 bzw. 104 Zellen/ml S. cerevisiae var. diastaticus (DSM 70487) dotiert, mechanisch/thermisch aufgearbeitet (Kap. 2.6.1) und je 5 µl in der Real-Time PCR eingesetzt. Alle undotierten Proben und alle dotierten Proben, die im Kanal 640/Back 530 negativ waren, waren im für die IAK spezifischen Kanal 705/Back 530 positiv. 3.1.7 Anwendbarkeit der Real-Time PCR für S. cerevisiae var. diastaticus in der Praxis Die Real-Time PCR für S. cerevisiae var. diastaticus und die mechanisch/thermische Aufarbeitungsmethode wurde von vier Brauereien getestet. Die Testung gliederte sich in drei Versuchsteile. Im ersten Versuchsteil wurden Proben aus der Routine getestet, um die Robustheit des Systems in Bezug auf die interne Amplifikationskontrolle zu testen. Der zweite Versuchsteil umfasste den Test von S. cerevisiae var. diastaticus Reinkulturen (Typstämme oder Eigenisolate der Brauereien). Die Sensitivität des Systems wurde in einem dritten Teil mit Verdünnungsreihen von unterschiedlichen, dotierten Probenmaterialien getestet (Kap. 2.16). 3.1.7.1 Versuchsteil 1: Robustheit Je Probenart wurden zwei Probenvolumina aufgearbeitet und mit dem PCR-System im Duplikat getestet (Tab. 3.7). Bis auf eine Probe (Hygieneabstrich, Brauerei D) wies keine Probe eine Kontamination mit S. cerevisiae var. diastaticus auf. Die IAK wurde nur bei den Probenmatrices Presshefe (Brauerei C), Hefe-Lagertank (Brauerei C) und Laugetank (Brauerei B) inhibiert. Die Reduktion des Probevolumens von 1,0 ml auf 0,1 ml beseitigte die Inhibition 49 3 Ergebnisse bei den Probematrices Presshefe und Hefe-Lagertank jedoch nicht bei der Probenmatrix Laugetank. Eine Reduktion des Probevolumens verbesserte auch bei den Proben Sauergut 3, Hefetank, Säuretank (Brauerei B) und Sirup (Brauerei D) die Amplifikation der IAK. Die drei eingesetzten Methoden zur Probenaufarbeitung (MagNA Pure DNA Isolation Kit III [Brauerei A], mechanisch/thermischer Aufschluss mit MagNA Lyser [Brauerei C und D] oder Disruptor Genie [Brauerei B]) waren für die Anwendung bei unterschiedlichen Probenmatrices geeignet. Tab. 3.7: Ergebnisse des Versuchsteils 1: Robustheit Brauerei Probe A B C Würze Erntehefe Pallanlage = Hefebiergewinnung Hefereinzucht Filtereinlauf + Kieselgur Recycling-Wasser mit Desinfektionsmittel Kronenkorken 3 Tage in Pils Spülwasserflasche mit Ringerlösung ausgespült Abstrich verkeimte Zapfanlage mit Fremdhefe Lactobacillus lindneri in betriebseigenem Medium 0,5 l Dose Schwarzbier vor der Pasteurisierung 0,33 l Dose Pils aus der Abfüllung Sauergut 2 Sauergut 3 Jungbierkühler Hefetank Säuretank Laugetank Seperator-Unfiltrat Puffertank Unfiltrat KG-Filter ZHF-Filter Spülwasser Alkoholfreies Bier Presshefe Hefe-Lagertank Anzuchttank Würzekühler Standwasser Fermentationstank (Tag 0) Fermentationstank (Tag 3) Fermentationstank (RUH) Lagerbiertank Filtration Helles Bier Flasche vor der Pasteurisation Flasche nach der Pasteurisation Würze 50 Cp-Werte F3/BackF1 oder 705/Back530 je Probenvolumen 1,0 ml 0,1 ml 35,48 34,32 33,62 33,43 34,01 34,12 33,32 34,27 33,91 34,05 34,42 34,49 34,40 33,60 34,06 33,92 34,15 34,23 34,02 33,80 34,47 34,16 34,28 33,80 33,72 34,52 33,63 34,48 33,63 34,00 34,10 33,73 33,60 34,09 33,93 34,31 34,65 33,79 33,73 34,18 34,51 33,97 33,89 34,07 34,11 33,79 33,93 34,61 34,22 33,97 34,56 32,94 40,28 34,69 35,13 33,91 34,27 33,18 35,22 34,59 39,25 36,41 35,17 33,62 34,46 > 40 35,93 32,61 35,18 34,10 35,07 33,55 35,15 34,06 34,54 34,17 36,25 33,30 35,25 34,47 34,30 33,83 35,26 34,00 35,29 35,12 33,25 33,87 32,97 33,47 33,57 34,51 34,63 34,55 34,04 35,68 33,69 34,10 33,23 32,82 33,09 32,88 33,08 33,60 33,11 32,48 32,32 32,72 33,12 34,06 33,30 32,50 34,64 34,54 33,16 32,74 33,63 33,18 33,08 33,11 32,26 32,86 32,21 32,68 32,86 32,76 32,90 33,49 33,06 32,62 33,18 33,22 32,91 32,81 32,84 33,07 32,25 32,70 32,94 32,93 33,30 32,51 32,50 33,03 3 Ergebnisse Tab. 3.7: Fortsetzung Brauerei Probe D Pils Pils+NBB-C Bouillon MRSF Bouillon (Charge 1) MRSF Bouillon (Charge 2) Kieselgur Einlauf Reinzuchthefe Jungbier Hefebier Anstellwürze MRS Bouillon Hygieneabstrich in SSL Bouillon* Sirup (für die Herstellung von Biermixgetränken) Cp-Werte F3/BackF1 oder 705/Back530 je Probenvolumen 1,0 ml 0,1 ml 34,28 33,78 33,76 33,66 35,01 34,51 33,87 35,10 34,30 34,15 34,61 33,56 34,43 33,49 34,53 34,27 33,87 33,75 33,77 33,80 33,96 34,01 34,24 33,99 34,33 33,99 33,89 34,55 34,01 34,09 33,68 34,06 33,51 35,02 33,84 34,49 34,18 33,82 33,70 34,14 32,23 31,86 32,34 32,87 35,02 38,02 33,81 34,02 Alle Proben der Brauereien B, C und D wurden mit der mechanisch/thermischen DNAExtraktionsmethode (Kap. 2.6.1) behandelt und 5 µl des Eluats in der Real-Time PCR für S. cerevisiae var. diastaticus eingesetzt. Die Proben der Brauerei A wurden mit dem MagNA Pure DNA Isolation Kit III behandelt. Die Amplifikation der IAK wurde im Kanal F3/Back F1 bzw. 640/Back 530 detektiert. *: Probe war positiv im Kanal F2/Back F1 (1,0 ml: Cp-Werte 32,09 und 31,71; 0,1 ml: Cp-Werte 32,17, 32,71). 3.1.7.2 Versuchsteil 2: Spezifität Alle 19 Reinkulturen (Eigenisolate oder Stämme aus Stammsammlungen) wurden bei den Brauereien mit dem Real-Time PCR-System als S. cerevisiae var. diastaticus identifiziert (Tab. 3.8). Bei der Schmelzkurven-Analyse waren die Proben mit einem Schmelzhöchstwert oberhalb von 62 °C eindeutig von der PK mit einem Schmelzhöchstwert von ca. 58 °C zu unterscheiden. Tab. 3.8: Ergebnisse des Versuchsteils 2: Spezifität Brauerei A B C D S. c. var. diastaticus Stämme 4 Eigenisolate DSM 70487 5 Eigenisolate 2 Eigenisolate DSM 70487 VTT C-82101 5 Eigenisolate Ergebnis positiv positiv positiv positiv positiv positiv positiv Die Proben der Hefestämme wurden mit dem mechanisch/thermischen DNA-Extraktionsverfahren aufgearbeitet (Kap. 2.6.1) und mit der Real-Time PCR für S. cerevisiae var. diastaticus getestet. 3.1.7.3 Versuchsteil 3: Sensitivität Unabhängig von der Probenaufarbeitung und den Probenmatrices war bei 17 von 19 Probenmatrices ein Kontaminationslevel von 102 Zellen/ml mit der Real-Time PCR für S. cerevisiae var. diastaticus nachweisbar (Tab. 3.9 und Abb. 3.10). Nur bei den Probenmatrices Reinzuchthefe und SSL-Bouillon lag der nachweisbare Level bei 103 Zellen/ml. 51 3 Ergebnisse Tab. 3.9: Brauerei A B C D Ergebnisse des Versuchsteils 3: Sensitivität Probenmatrix Jungbier Stabibier Pils Würze MRS Bouillon Würze NBB Bouillon Dunkles Bier Biermixgetränk Hefe-Lagertank Fermentationstank Biertank (hell) Lagerbiertank Flaschenbier filtriertes Pils Jungbier Reinzuchthefe SSL-Bouillon MRSF Bouillon 104 29,28 29,70 31,53 30,43 27,74 26,94 26,18 27,50 27,93 29,63 29,62 29,52 29,66 29,74 30,90 30,54 31,51 31,30 30,76 Cp-Wert (640/Back530 bzw. F2/BackF1) je Zellzahl [Zellen/ml] 103 102 undotiert 32,98 33,17 32,34 33,88 33,12 34,05 32,96 34,54 30,88 32,14 30,47 33,92 30,47 33,92 30,52 32,61 29,14 32,55 31,44 33,60 32,86 33,98 32,70 32,50 32,11 32,84 32,62 33,81 33,16 33,65 33,44 34,12 33,56 33,87 33,32 33,56 - Die Proben wurden bei den Brauereien dotiert und undotiert mechanisch/thermisch aufgearbeitet (Kap. 2.6.1) und mit der Real-Time PCR für S. cerevisiae var. diastaticus untersucht. Abb. 3.10: Real-Time PCR Nachweis von S. cerevisiae var. diastaticus in Flaschenbier Flaschenbier wurde bei der Brauerei C mit 104 Zellen/ml (schwarze Linie), 103 Zellen/ml (rote Linie) bzw. 102 Zellen/ml (blaue Linie) dotiert, mechanisch/thermisch aufgearbeitet (Kap. 2.6.1) und mit der Real-Time PCR für S. cerevisiae var. diastaticus untersucht. Die Auswertung der Amplifikation erfolgte im Kanal 640/Back 530. Als Negativkontrolle wurde eine undotierte Probe (grüne Linie) mitgeführt. 52 3 Ergebnisse 3.2 Entwicklung einer Real-Time Consensus-PCR für Hefen 3.2.1 Auswahl des EF-3 Gens als Zielregion Das EF-3 Gen wurde bisher teilweise oder vollständig von den Hefen S. cerevisiae, C. albicans, C. maltosa, C. melibiosica, C. zeylanoides, Cr. neoformans, K. lactis, P. pastoris, Sch. pombe und Y. lipolytica sequenziert (Blakely 2001, Di Domenico et al. 1992, Mita et al. 1997, Myers et al. 1992, Qin et al. 1990, Sandbaken et al. 1990a,b, Uritani et al. 1999). Aus dem Reich der Eukaryoten liegen außerdem von dem humanpathogenen Schimmelpilz Aspergillus fumigatus (Acc. No. XM 743850) und der hefeähnlichen Art Pneumocystis carinii Sequenzen dieses Gens vor (Ypma-Wong et al. 1992). Der Elongationsfaktor 3 wurde als essentielles Protein der Elongationsphase bei der Translation von mRNA zum Protein beschrieben und bisher wurde kein entsprechendes Gegenstück bei Prokaryoten oder anderen Eukaryoten als bei Hefen und Schimmelpilzen entdeckt (Dasmahapatra und Chakraburtty 1981, Hutchison et al. 1984, Sandbaken et al. 1990a,b, Skogerson und Wakatama 1976). Bei dem Chlorella Virus CVK2 und E. coli wurden zwar je ein Gen mit teilweiser Sequenzhomologie zum EF-3 Gen entdeckt, (Belfield et al. 1995, Kiel et al. 1999, Yamada et al. 1993) die ausgewählte Sequenzregion zwischen den beiden Walker Signaturen der zweiten ATP-Bindekassette wurde jedoch als spezifisch für das EF-3 Gen beschrieben (Abb. 3.11) (Uritani et al. 1999). EF-3 spezifische Sequenz 768-873 Walker A Walker B Walker A Walker B NH COOH 1 1044 HS04 960-965 HSwb1 565-575 HS03 435-441 HS10 758-764 HS12/IV-IX 758-765 HSabc3 898-908 HS09 874-879 HS14/III-VIII 848-856 Abb. 3.11: Schematische Darstellung der Aminosäuresequenz des Elongationsfaktors 3 von Hefen Der Elongationsfaktor 3 besitzt zwei ATP-Bindungskassetten mit je einer Walker A und B Signatur (schwarz). Innerhalb der zweiten ATP-Bindungsstelle liegt der für den Elongationsfaktor 3 spezifische Sequenzbereich (grau), der als Target für die Real-Time Condsensus-PCR für Hefen ausgewählt wurde. Die 5´-Primer (rot) und 3´-Primer (blau), mit denen zur Sequenzierung Abschnitte des EF-3 Gens von unterschiedlichen Hefearten amplifiziert wurden, wurden mit Angaben zu deren Position dargestellt. 53 3 Ergebnisse 3.2.2 Sequenzierung und Alignment des EF-3 Genbereichs Aufbauend auf einem Alignment der bereits bekannten EF-3 Gen Sequenzen von C. albicans (Acc. No. AF038153), C. maltosa (Acc. No. AB018532), C. melibiosica (Acc. No. AB018533), C. zeylanoides (Acc. No. AB018534), Cr. neoformans (Acc. No. AF316889), K. lactis (Acc. No. AB018535), P. pastoris (Acc. No. AB018536), Sch. pombe (Acc. No. AB018538) und Y. lipolytica (Acc. No. AB018537) wurden Primer entwickelt, um den EF-3 spezifischen Sequenzbereich einer größeren Anzahl an Hefen zu amplifizieren und anschließend zu sequenzieren (Kap. 2.9 und 2.10) (Abb. 3.11). Außerdem wurde ein von Uritani et al. (1999) beschriebenes Primerpaar (HS03/04) verwendet. Die Primer HS10 und HS09 wurden am 5´-Ende um ein Nucleotid mit der Base Adenin verlängert, um die Ligationseffizienz der PCR-Produkte in den Vektor pGEM®-T zu erhöhen. Mit dem Primerpaar HS10/09 wurde mit der DNA folgender 49 Hefestämme direkt oder über eine Nested-PCR ein ca. 367 bp großes Fragment amplifiziert und sequenziert. Bei der Nested-PCR wurde zunächst ein 1,6 kbp großes PCR-Produkt mit dem Primerpaar HS03/HS04 amplifiziert und anschließend 1:1000-verdünnt eingesetzt. C. albicans (ATCC 10231) C. krusei (BCD 689) C. rugosa (BCD 814) C. tenuis (BCD 819) C. zeylanoides (BCD 690) Deb. etchelsii (ATCC 20126) Deb. marama (ATCC 11627) Hyp. burtonii (BCD 859) K. marxianus (BCD 2563) K. marxianus (DSM 70106) L. elongisporus (DSM 70320) P. angusta (DSM 70277) P. fermentans (DSM 70090) S. bayanus (BCD 1256) S. c. var. diastaticus (BCD 1257) Z. bailii (BCD 1424) Tr. cutaneum (DSM 70684) C. glaebosa (CBS 5691) C. maltosa (BCD 806) C. sake (BCD 1054) C. tropicalis (ATCC 20326) Ci. matritensis (BCD 1062) Deb. hansenii (BCD 3512) En. fibuliger (BCD 3514) Hyp. burtonii (DSM 3505) K. marxianus (BCD 5186) K. marxianus (DSM 70792) La. thermotolerans (CBS 6340) P. farinosa (BCD 861) P. guilliermondii (BCD 804) S. bayanus (BCD 1392) S. pastorianus (BCD 728) Z. rouxii (ATCC 48230) C. intermedia (BCD 685) C. parapsilosis (ATCC 20384) C. santamariae (CBS 4261) C. vini (DSM 70184) Cl. lusitaniae (DSM 70102) Deb. hansenii (BCD 589) G. selenospora (DSM 3431) I. orientalis (CBS 5147) K. marxianus (BCD 811) Ka. unispora (BCD 877) M. pulcherrima (DSM 70321) P. fermentans (BCD 711) P. ohmeri (BCD 862) S. cerevisiae (DSM 1333) T. delbrueckii (DSM 70607) Sch. pombe (BCD 773) Mit dem Primerpaar HS10/04 wurde mit der DNA folgender 32 Hefestämme direkt oder in einer Semi-Nested PCR ein ca. 624 bp großes Fragment amplifiziert und sequenziert. Bei der Semi-Nested PCR wurde zunächst ein 1,6 kbp großes PCR-Produkt mit dem Primerpaar HS03/HS04 amplifiziert und anschließend 1:1000-verdünnt eingesetzt. C. boidinii (DSM 70034) C. ernobii (DSM70858) C. multigemmis (DSM 70862) D. bruxellensis (DSM 3429) En. fibuliger (DSM 70554) H. uvarum (BCD 3526) P. anomala (DSM 70783) P. membranaefaciens (DSM 70178) Sch. octosporus (DSM 70573) Z. bisporus (DSM 70415) C. catenulata (DSM 70136) C. glabrata (BCD 8932) C. solani (BCD 818) D. bruxellensis (DSM 70726) H. guilliermondii (DSM 70285) H. vineae (DSM 70283) P. canadensis (CBS 601) S. bayanus (DSM 70412) S. exiguus (MUCL 29838) Y. lipolytica (BCD 2556) Z. florentinus (DSM 70506) 54 C. diddensiae (DSM 70042) C. haemulonii (DSM 70624) C. versatilis (DSM 6956) D. custersiana (DSM 70736) H. uvarum (ATCC 9774) P. anomala (BCD 1082) P. carsonii (DSM 70392) S. c. var. diastaticus (DSM 70487) S. pastorianus (DSM 6580) Y. lipolytica (BCD 2003) Z. microellipsoides (DSM 6959) 3 Ergebnisse Kein spezifisches PCR-Produkt wurde mit den Primerpaaren HS03/04, HS10/04 oder HS10/09 mit Ausnahme von Tr. cutaneum von Hefen der Unterabteilung Basidiomycota amplifiziert. Daher wurde das degenerierte Primerpaar HSwb1/abc3 aufgrund der Sequenzinformationen, die über die Walker B Sequenzbereiche vorlagen, konstruiert. Ein ca. 1032 bp großes PCR Produkt wurde von folgenden Hefen amplifiziert und sequenziert: Bul. dendrophila (DSM 70745) R. minuta (DSM 70408) Cr. curvatus (BCD 2578) Cr. laurentii (BCD 824) Ein ca. 263 bp langes PCR Fragment wurde von folgenden Hefen mit dem Primermix aus den 5´-Primern HS12/IV-IX und den 3´-Primern HS14/III-VIII, die aufgrund der Sequenzinformationen der zuvor sequenzierten Hefen der Unterabteilung der Basidiomycota konstruiert wurden, amplifiziert und anschließend sequenziert: Cr. albidus (DSM 70197) Cr. humicola (DSM 70067) Sp. johnsonii (BCD 778) Cr. curvatus (DSM 70022) R. glutinis (BCD 3530) Sp. johnsonii (DSM 70847) Cr. flavus (BCD 823) Sp. johnsonii (BCD 4982) Die Abbildung 6.1 im Anhang zeigt das vollständige Alignment (Kap. 2.11) der sequenzierten Nucleinsäuresequenzen des EF-3 Gen Abschnitts von der Position 2272 bis 2637 (Aminosäureposition 758 bis 879, S. cerevisiae Sequenz) unter Einbeziehung der bereits bekannten Sequenzen. 3.2.3 Sequenzvergleich des EF-3 Genbereichs Die Unterabteilungen der Ascomycota und der Basidiomycota waren aufgrund der Sequenzinformation des EF-3 Genabschnitts deutlich von einander zu unterscheiden. Die Übereinstimmung der Aminosäuresequenz lag zwischen den Vertretern der beiden Unterabteilungen unter 35 % (Tab. 6.3). Die prozentuale Übereinstimmung innerhalb der Unterabteilung der Basidiomycota betrug mindestens 67 % (Tab. 6.3). Hefen aus der Klasse der Hemiascomycetes (Ordnung Saccharomycetales) wiesen untereinander eine Übereinstimmung in der Aminosäuresequenz von mindestens 68 % auf (Tab. 6.2). Die Gattung Schizosaccharomyces als einziger Vertreter der Klasse der Archiascomycetes sowie die Gattung Dekkera hoben sich als monophyletische Einheiten deutlich von den restlichen Hefen der Klasse der Hemiascomycetes ab (Abb. 3.12). Weitere monophyletische Gattungen waren in dem Dendogramm (Abb. 3.12) nicht zu erkennen. Die Gattung Saccharomyces wies große sequenzielle Übereinstimmung mit den Gattungen Kluyveromyces, Zygosaccharomyces und Torulaspora auf. Variationen der Aminosäuresequenz waren auch unter Stämmen der gleichen Art vorhanden, da z. B. die Arten S. pastorianus und S. bayanus keine monophyletischen Gruppen bildeten. Aufgrund dieser Sequenzvergleiche wurden drei Bereiche der Aminosäuresequenz ausgewählt, die als Basis für ein Primer- und Sondendesign dienten. 55 3 Ergebnisse 56 3 Ergebnisse Abb. 3.12: Dendrographische Auswertung der EF-3 Gensequenzen Der Baum basiert auf den sequenzierten EF-3 Genabschnitten von Hefen der Unterabteilung der Ascomycota (App. 6.1 im Anhang) und wurde unter Verwendung der Neighbour-Joining Methode (Saitou und Nei 1987) konstruiert (Kap. 2.11). Alle nicht in dieser Arbeit generierten Sequenzen sind mit ihren GenBank Zugangsnummern angegeben. Die genauen prozentualen Übereinstimmungen der Aminosäuresequenzen sind in der Tabelle 6.2 im Anhang angegeben. 3.2.4 Anordnung der Primer und Hybridisierungssonden im EF-3 Gen Für zwei Real-Time LightCycler® PCR-Systeme, die sich in der Art der Detektion der gebildeten Amplifikate unterschieden, wurden Primer und Hybridisierungssonden von dem Nucleinsäurealignment des EF-3 Genabschnitts (Abb. 6.1) abgeleitet. Die Detektion der gebildeten PCR-Fragmente erfolgte bei dem einen System durch den Fluoreszensfarbstoff SYBR®Green I, mit dem die doppelsträngige DNA unspezifisch durch Interkalation und die damit verbundene Fluoreszenserhöhung nachgewiesen wurde. Bei dem anderen System erfolgte 57 3 Ergebnisse der Nachweis durch spezifische Hybridisierung von zwei Sonden an das gebildete Amplifikat und die damit verbundene Fluoreszenserhöhung über den „fluorescence resonance energy transfer“ (FRET). Die genaue Lage aller Primer und Hybridisierungssonden ist in dem Nucleinsäurealignment der EF-3 Genabschnitte (Abb. 6.1) angegeben. 3.2.4.1 Real-Time Consensus-PCR für Hefen mit SYBR®-Green I Aufgrund der Heterogenität der Sequenzen mussten grundlegend unterschiedliche, degenerierte Primer für Hefen der Unterabteilung Ascomycota und Hefen der Unterabteilung Basidiomycota entworfen werden. Das für die Gattung Schizosaccharomyces spezifische Primerpaar Ha1f/Ha1r und ein für die weiteren Hefen der Unterabteilung Ascomycota spezifischer Mix aus den 5´-Primern Ha2f-5f und den 3´-Primern Ha2r-8r wurden für die Amplifikation eines ca. 315 bp großen DNA-Fragments eingesetzt. Für die Amplifikation eines ca. 213 bp großen Fragments von Hefen der Unterabteilung der Basidiomycota wurden die 5´-Primer Hb1f-5f und die 3´-Primer Hb1r-3r ausgewählt. 3.2.4.2 Real-Time Consensus-PCR für Hefen mit Hybridisierungssonden Auch für die Real-Time Consensus-PCR mit Hybridisierungssonden mussten wie bei dem System mit SYBR®-Green I zwei grundlegend unterschiedliche Teilsysteme für die Ascomyceten auf der einen Seite und die Basidiomyceten auf der anderen Seite entwickelt werden. Das für die Gattung Schizosaccharomyces spezifische Primerpaar Yfs1/HT4r und ein für die weiteren Hefen der Unterabteilung Ascomycota spezifischer Mix aus den 5´-Primern Yfa1, Yfa2, HS11/I-IV und den 3´-Primern HT1r-3r wurde für die Amplifikation eines ca. 305 bp großen DNA-Fragments eingesetzt. Für die Amplifikation eines ca. 246 bp großen Fragments von Hefen der Unterabteilung der Basidiomycota wurden die 5´-Primer Hb6f-7f und die 3´-Primer HT5r-6r ausgewählt. Die Hybridisierungssonden mussten wie die Primer aufgrund der hohen Heterogenität der Zielsequenzen degeneriert werden. Hierbei wurde nicht jede Sequenzvariation, die das Nucleinsäurealignment (Abb. 6.1) vorgab, oder jede durch die Aminosäuresequenz mögliche Variation berücksichtigt. Die Sonden wurden bis zu 32-fach degeneriert und außerdem bis zu zwei Basen durch Inosin substituiert. Außerdem wurden die Sonden möglichst lang konstruiert, um trotz möglicher Nucleotidfehlpaarungen eine ausreichend hohe Schmelztemperatur für die Detektion durch Hybridisierung zu erreichen. Die Abbildung 3.13 verdeutlicht die Vorgehensweise bei der Konstruktion der Hybridisierungssonden am Beispiel der Sonde Yff3. Degenerierungen wurden bevorzugt dort vorgenommen, wo aufgrund der Aminosäuresequenz die Variation auf zwei Basen reduziert werden konnte. Ikuta et al. (1987) zeigten, dass die Nucleotidfehlpaarungen G:A, G:T und G:G nur leicht, die Nucleotidfehlpaarungen 58 3 Ergebnisse A:A, T:T, C:T und C:A dagegen signifikant destabilisierend wirken. Daher wurden Degenerierungen auch vorgenommen, um ungünstige Nucleotidfehlpaarungen zu vermeiden. H. H. H. S. T. C. C. P. P. guilliermondii (DSM 70285)GAATTCAAGAAATTCACGCTAGAAGAAAATTCAAGAAC uvarum (BCD 3526) GAATTCAAGAAATTCACGCTAGAAGAAAATTCAAGAAC uvarum (ATCC 9774) GAATTCAAGAAATTCACGCTAGAAGAAAATTCAAGAAC bayanus (BCD 1392) GAATCCAAGAGATTCACGCCAGAAGAAAGTTCAAGAAC delbrueckii (DSM 70607) GAATCCAAGAGATTCACGCCAGAAGAAAGTTCAAGAAC glabrata (BCD 8932) GAGTTCAAGAAATCCATGCCAGAAGAAAATTCAAGAAC solani (BCD 818) GTATTCATGAAATTCATGCTAGAAGGAAATTCAAGAAC anomala (BCD 1082) GTATTCATGAAATTCATGCTAGAAGAAAATTCAAGAAC anomala (DSM 70783) GTATTCATGAAATTCATGCTAGAAGAAAATTCAAGAAC Hybridisierungssonde Yff3 GAGTTCAAGARATTCAYGCIAGAAGRAARTTCAAGAAC Abb. 3.13: Konstruktion der Hybridisierungssonde Yff3 für das EF-3 Genfragment Bei dem Design der Hybridisierungssonden für die Real-Time Consensus-PCR für Hefen wurden Nucleinsäurefehlpaarungen (grau) und Degenerierungen (Rahmung) mit einkalkuliert. Dargestellt sind die Sequenz der Hybridisierungssonde Yff3 und die Sequenzen der Targetorganismen in 5´-3´ Orientierung. Für Ascomyceten wurden sechs mit Fluorescein am 3´-Ende markierte Donator-Sonden (Yff1-4, Yff6 und Yff8) und fünf am 5´-Ende mit dem Fluoreszenzfarbstoff LightCycler®-Red 640 markierte Akzeptor-Sonden (Yfr1-4 und Yfr8) entwickelt. Die Sonde Yff6 wurde für Hefen der Gattung Schizosaccharomyces und das Sondenpaar Yff8/Yfr8 für die Art C. magnoliae designt. Für Basidiomyceten wurden eine mit Fluorescein am 3´-Ende markierte DonatorSonde (Yff5) und zwei am 5´-Ende mit dem Fluoreszenzfarbstoff LightCycler®-Red 640 markierte Akzeptor-Sonden (Yfr5 und Yfr7) entwickelt. Alle Hybridisierungssonden wurden im EF-3 Gen in 5´-3´-Richtung orientiert. Das PCR-Profil wurde den niedrigen Schmelztemperaturen der Sonden angepasst, indem eine „Touchdown-PCR“ gewählt wurde, bei der die Annealingtemperatur je PCR-Zyklus kontinuierlich um 0,5 °C von 60 auf 40 °C abnimmt. Dieses Profil ermöglichte eine spezifische Amplifikation der Targetsequenzen durch die Primer zu Beginn der PCR und die später im Zyklusprofil erfolgende Detektion mit den Hybridisierungssonden. 3.2.5 Konstruktion der internen Amplifikationskontrolle und der Positivkontrolle Wie im Kap. 3.1.3 für das S. cerevisiae var. diastaticus Nachweissystem beschrieben, wurden auch für die Real-Time Consensus-PCR mit Hybridisierungssonden eine interne Amplifikationskontrolle (IAK) konstruiert. Die Sequenz der IAK entsprach bis auf den Austausch der Zielregion der LightCycler®-Red 640 markierten Sonde Yfr4 durch Einbau eines Sequenzabschnittes, der komplementär zu der Sequenz der LightCycler®-Red 705 markierten Sonde LMRST1 war, der Sequenz des EF-3 Genabschnitts von S. c. var. diastaticus (DSM 70487). 59 3 Ergebnisse Konstruiert wurde die interne Amplifikationskontrolle über die PCR-Mutagenese mit den Primern Yip1f und Yip1r (Kap. 2.9.1.2). 1--------Yfa1----------------------------------------------60 S.dia. GTGAAGATAGAGAAACCATGGACAGAGCTAACAGACAAATCAACGAAAACGATGCTGAAG IAK GTGAAGATAGAGAAACCATGGACAGAGCTAACAGACAAATCAACGAAAACGATGCTGAAG 61------------------------------------------Yff1----------120 S.dia. CTATGAACAAGATCTTCAAGATTGAAGGTACCCCTAGAAGAATTGCCGGTATCCACTCCA IAK CTATGAACAAGATCTTCAAGATTGAAGGTACCCCTAGAAGAATTGCCGGTATCCACTCCA 121---------------------------Yfr4-----LMRST1-------------180 S.dia. GAAGAAAGTTCAAGAACACTTACGAATATGAATGTTCTTTCTTATTGGGTGAAAACATTG IAK GAAGAAAGTTCAAGAACACATT--A-TCCGA---TACGTTCTTCCAGTGCCA----TTTT 181-------------------------------------------------------240 S.dia. GTATGAAATCTGAAAGATGGGTTCCAATGATGTCCGTCGACAACGCTTGGATTCCAAGAG IAK GTATGAAATCTGAAAGATGGGTTCCAATGATGTCCGTCGACAACGCTTGGATTCCAAGAG 241---------------------------------------------HT1r------301 S.dia. GTGAATTGGTTGAATCTCACTCTAAGATGGTTGCTGAAGTTGATATGAAGGAAGCTTTGGC IAK GTGAATTGGTTGAATCTCACTCTAAGATGGTTGCTGAAGTTGATATGAAGGAAGCTTTGGC Abb. 3.14: Sequenzvergleich der IAK mit dem EF-3 Gen von S. cerevisiae var. diastaticus Das Alignment zeigt die Sequenzen der IAK der Real-Time Consensus-PCR für Hefen und die Wildtyp Sequenz des EF-3 Gens von S. cerevisiae var. diastaticus (DSM 70487). Die Primer Yfa1 und HT1r sowie die Hybridisierungssonde Yff1 waren für beide Sequenzen spezifisch. Die Hybridisierungssonde Yfr4 war für die Wildtyp Sequenz und die Sonde LMRST1 für die IAK Sequenz spezifisch. Die Markierung der Sonden Yfr4 und LMRST1 mit unterschiedlichen Fluoreszenzfarbstoffen ermöglichte eine Unterscheidung zwischen IAK und Wildtyp Amplifikaten in der PCR. Nach Ligation der PCR-Produkte in den Vektor pGEM®-T (Kap. 2.9.3), Transformation in E. coli XL-1 Blue Zellen (Kap. 2.9.4) und Linearisierung der gereinigten Plasmide (Kap. 2.9.5) mit der Restriktionsendonuclease Sac I (Kap. 2.9.6) wurde der Erfolg der Herstellung durch Sequenzierung (Kap. 2.10) und Alignment (Kap. 2.11) mit der Sequenz des EF-3 Genabschnitts von S. cerevisiae var. diastaticus bestätigt (Abb. 3.14). In allen folgenden Versuchen wurden von der IAK je PCR-Reaktion 0,5 fg eingesetzt. Bei der Herstellung der PK wurden keine Sequenzveränderungen vorgenommen, sondern eine klonierte E. coli XL-1 Blue Kultur verwendet, die für die Sequenzierung des EF-3 Sequenzabschnitts von C. haemulonii (DSM 70624) hergestellt worden war. Dieses Vorgehen wurde gewählt, da eine eindeutige Unterscheidung zwischen der PK und positiven Proben über Schmelzkurven-Analyse aufgrund der Vielzahl an degenerierten Sonden von vornherein auszuschließen war. Das gereinigte Plasmid (Kap. 2.9.5) wurde mit der Restriktionsendonuclease Sac I linearisiert (Kap. 2.9.6) und 5 fg in der PCR verwendet. 60 3 Ergebnisse 3.2.6 Spezifität und Auswahl des Detektionssystems 3.2.6.1 Spezifität der Real-Time Consensus-PCR für Hefen mit SYBR®-Green I Von allen Hefen, von denen die Sequenzinformationen vorlagen (Kap. 3.2.2), wurde mit der Real-Time Consensus-PCR für Hefen mit SYBR®-Green I das gewünschte PCR-Produkt mit einer Länge von ca. 313 (Ascomycota) bzw. 213 bp (Basidiomycota) amplifiziert (Abb. 3.15). Abb. 3.15: Agarosegelelektrophorese nach Real-Time PCR mit SYBR®-Green I Die Real-Time Consensus-PCR für Hefen mit SYBR®-Green I wurde mit je 250 pg RNA-freier DNA (Kap. 2.6.2) getestet. Die Agarosegelelektrophorese wurde mit 5 µl der Reaktionsansätze in einem 2-%igen Gel durchgeführt (Kap. 2.8). PD=Primerdimere. 1: Molekulargewichtsmarker VI 2: Schizosaccharomyces octosporus (DSM 70573) 3: Candida albicans (ATCC 10321) 4: Candida catenulata (DSM 70136) 5: Citeromyces matritensis (BCD 1062) 6: Dekkera custersiana (DSM 70736) 7: Pichia angusta (DSM 70277) 8: Candida boidinii (DSM 70034) 9: Debaryomyces hansenii (BCD 3512) 10: Guilliermondella selenospora (DSM 3431) 11: Candida haemulonii (DSM 70624) 12: Candida rugosa (BCD 814) 13: Candida zeylanoides (BCD 690) 14: Lachancea thermotolerans (CBS 6340) 61 15: Molekulargewichtsmarker VI 16: Pichia ohmeri (BCD 862) 17: Yarrowia lipolytica (BCD 2556) 18: Candida diddensiae (DSM 70042) 19: Candida versatilis (DSM 6956) 20: Dekkera bruxellensis (DSM 3429) 21: Pichia farinosa (BCD 861) 22: Saccharomyces pastorianus (DSM 6850) 23: Pichia membranaefaciens (DSM 70178) 24: Candida glaebosa (CBS 5691) 25: Pichia carsonii (DSM 70392) 26: Filobasidium capsuligenum (DSM 70253) 27: Rhodotorula minuta (DSM 70408) 28: Cryptococcus curvatus (DSM 70022) 3 Ergebnisse Die Primerkonzentrationen und die PCR-Bedingungen konnten jedoch nicht so eingestellt werden, dass eine ausreichend hohe Stringenz erreicht wurde, um in jeder Hinsicht eindeutige, spezifsche Ergebnisse zu liefern. Die Bildung von Primerdimeren, die mit SYBR®-Green I ebenfalls detektiert wurden, und unspezifische Amplifikate mit Bakterien-DNA ließen eine eindeutige Abtrennung zwischen negativen und positiven Proben nicht zu. Die spezifischen Amplifikate hatten Schmelzhöchstwerte zwischen ca. 81 und 91 °C, die sich an ihrer unteren Grenze mit den Schmelzhöchstwerten der Primerdimere, die in den Negativkontrollen gebildet wurden, überlagerten (Abb. 3.16). Die unspezifische Amplifikation von Bakterien-DNA verhinderte ebenfalls eine Differenzierung zwischen positiven und negativen Proben bei der Schmelzkurven-Analyse (Abb. 3.17). Abb. 3.16: Schmelzkurven-Analyse von spezifischen Amplifikaten und Primerdimeren Die Real-Time Consensus-PCR für Hefen mit SYBR®-Green I wurde mit je 250 pg RNA-freier DNA (Kap. 2.6.2) (schwarze Linien) von 1: Guilliermondella selenospora (DSM 3431), 2: Pichia carsonii (DSM 70392), 3: Pichia angusta (DSM 70277), 4: Cryptococcus albidus (DSM 70197), 5: Yarrowia lipolytica (BCD 2556) und 6: Rhodotorula glutinis (BCD 3530) durchgeführt. Die Negativkontrolle bestand aus PCR-H2O (rote Linie). Die Schmelzkurven-Analyse erfolgte im Kanal 530. 62 3 Ergebnisse Abb. 3.17: Schmelzkurven-Analyse von unspezifisch amplifizierter Bakterien-DNA Die Real-Time Consensus-PCR für Hefen mit SYBR®-Green I wurde mit 250 pg RNA-freier DNA (Kap. 2.6.2) von S. cerevisiae var. diastaticus (schwarze Linie) und Bakterien DNA (blaue Linien) nach mechanisch/thermischer Extraktion (Kap. 2.6.1) von Lactobacillus hilgardii, (DSM 20051), Lactobacillus kefiri (DSM 20588), Pantoea agglomerans (DSM 3493), Proteus vulgaris (DSM 2140), Salmonella enterica (BCD 14151), Shigella sonnei (BCD 4301), Sporosarcina urea (DSM 2281) durchgeführt. Als Negativkontrolle (rote Linie) wurde PCR-H2O eingesetzt. Die Auswertung der Schmelzkurven-Analyse erfolgte im Kanal 530. 3.2.6.2 Spezifität der Real-Time Consensus-PCR für Hefen mit Hybridisierungssonden Alle 198 in der Tabelle 2.1 aufgeführten Hefestämme und die 54 nicht genauer identifizierten Fremdhefen von den Brauereien A, B und D konnten mit dem System nachgewiesen werden. Eine Identifizierung über die Schmelzkurven-Analyse war aufgrund der Vielzahl an degenerierten Sonden, die bei unterschiedlichen Temperaturen abschmolzen, nicht möglich. Einzelne, reproduzierbare Schmelzhöchstwerte, die klar einer Art oder einer Gattung zuzuordnen waren, wurden nicht erhalten (Abb. 3.18). Alle getesteten Bakterien (Tab. 2.2) waren negativ und die Amplifikation der IAK wurde durch DNA dieser Mikroorganismen nicht beeinträchtigt. Die Abgrenzung zu den Schimmelpilzen war nicht vollständig möglich. Von den getesteten Schimmelpilzen (Tab. 2.3) wurden positive Ergebnisse mit DNA von Aspergillus flavus, Aspergillus fumigatus, Aspergillus parasiticus, Cephalosporium aphidicola, Diaporthe citri, Eremascus albulus, Fusarium oxysporum, Fusarium cerealis, Fusarium culmorum, Hyalodendron lignicola, Penicillium funiculosum, Trichoderma viride und Wallemia sebi erzielt. Die Amplifikation der IAK wurde durch die DNA von 63 3 Ergebnisse Schimmelpilzen, die im Kanal 640/Back 530 nicht nachgewiesen wurden, nicht beeinträchtigt. Abb. 3.18: Schmelzkurven-Analyse unterschiedlicher Hefearten Die Real-Time Consensus-PCR für Hefen mit Hybridisierungssonden wurde mit je 250 pg RNA-freier DNA (Kap. 2.6.2) von den Hefen Torulaspora delbrueckii (schwarze Linie), Saccharomycopsis fibuligera (schwarze Punkte), Clavispora lusitaniae (blaue Linie), Candida haemulonii (blaue Punkte), Zygosaccharomyces cidri (rote Linie) und Saccharomyces exiguus (rote Punkte) getestet. Die Schmelzkurven-Analyse wurde im Kanal 640/Back 530 ausgewertet. 3.2.7 Sensitivität der Real-Time Consensus-PCR für Hefen mit Hybridisierungssonden 3.2.7.1 Sensitivitätstestung mit quantifizierter, RNA-freier DNA Die Sensitivität der Real-Time Consensus-PCR für Hefen wurde mit quantifizierter, RNAfreier DNA von 36 unterschiedlichen Hefearten getestet (Tab. 3.10). Mit der Multiplex-PCR wurden unterschiedliche Sensitivitäten erreicht. Die höchste Nachweisgrenze mit 250 GÄ/Reaktion wurde mit DNA von Issatchenkia orientalis ermittelt. Alle weiteren untersuchten Hefearten wurden mit einer Sensitivität zwischen 10 und 100 GÄ/Reaktion nachgewiesen (Tab. 3.10). Die Umrechnung auf Genomäquivalente erfolgte mit den von S. cerevisiae (12,1 Mbp), Schizosaccharomyces pombe (13,8 Mbp) und Cryptococcus neoformans (21,0 Mbp) bekannten Genomgrößen und stellte demnach für einige Arten einen Näherungswert dar. Die Abbildung 3.19 zeigt die Amplifikationskurven der Sensitivitätstestung mit DNA von S. exiguus (MUCL 29838). 64 3 Ergebnisse Tab. 3.10: Sensitivitätstestung mit quantifizierter, RNA-freier DNA Hefestamm 1000 + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + Bullera dendrophila (DSM 70745) Candida albicans (ATCC 10231) Candida parapsilosis (ATCC 20384) Candida tropicalis (ATCC 20247) Citeromyces matritensis (BCD 1062) Clavispora lusitaniae (DSM 70102) Cryptococcus flavus (BCD 823) Debaryomyces hansenii (BCD 589) Dekkera bruxellensis (DSM 70726) Dekkera custersiana (DSM 70736) Endomyces fibuliger (DSM 70554) Filobasidium capsuligenum (DSM 70253) Guilliermondella selenospora (DSM 3431) Hanseniaspora guilliermondii (DSM 70285) Hyphopichia burtonii (BCD 859) Issatchenkia orientalis (CBS 5147) Kazachstania unispora (BCD 877) Kluyveromyces marxianus (DSM 70792) Lachancea thermotolerans (CBS 6340) Lodderomyces elongisporus (DSM 70320) Metschnikowia pulcherrima (DSM 70321) Pichia anomala (BCD 1082) Pichia membranaefaciens (DSM 70178) Rhodotorula minuta (DSM 70408) Saccharomyces bayanus (DSM 70412) S. cerevisiae var. diastaticus (DSM 70487) Saccharomyces exiguus (MUCL 29838) Saccharomyces pastorianus (DSM 6850) Schizosaccharomyces pombe (BCD 773) Sporidiobolus johnsonii (DSM 70847) Torulaspora delbrueckii (CBS 6339) Trichosporon cutaneum (DSM 70684) Yarrowia lipolytica (ATCC 20225) Zygosaccharomyces bailii (MUCL 28823) Zygosaccharomyces lentus (CBS 8516) Zygosaccharomyces rouxii (DSM 70835) +: Probe positiv - : Probe negativ Genomäquivalente/Reaktion 250 100 25 10 + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + Für die Sensitivitätstestung der Real-Time Consensus-PCR für Hefen mit Hybridisierungssonden wurde die RNA-freie DNA (Kap. 2.6.2) fluorometrisch quantifiziert (Kap. 2.7.1) und auf Genomäquivalente (GÄ) umgerechnet (Kap. 2.15.1). 65 3 Ergebnisse Abb. 3.19: Sensitivität der Real-Time Consensus-PCR für Hefen Die Real-Time PCR wurde mit 1000 GÄ (schwarze Linie), 250 GÄ (blaue Linie), 100 GÄ (rote Linie), 25 GÄ (schwarze Punkte), 10 GÄ (blaue Punkte) von S. exiguus (MUCL 29838) durchgeführt. Die Auswertung der Amplifikation erfolgte im Kanal 640/Back 530. Als Negativkontrolle (rote Punkte) wurde PCR-H2O eingesetzt. 3.2.7.2 Sensitivität in Kombination mit der mechanisch/thermischen DNAExtraktion Die Nachweisgrenze in Abhängigkeit von der Hefeart, der Zellzahl pro Aufarbeitung und dem mechanisch/thermischen DNA-Extraktionsverfahren wurde mit vorangereicherten Getränkeproben (1:10-verdünnt mit YM-Medium, 48 Stunden, bei 28 °C) getestet. Nach Dotierung der Anreicherungen mit 103, 104 oder 105 Hefezellen/ml wurden je Dotierungslevel 1 ml im Duplikat mechanisch/thermisch aufgearbeitet. In den trübstofffreien Getränken Pils, alkoholfreies Bier, Coca-Cola, Eistee, Radler, Apfelsaft (klar) und Gatorade wurden zwischen 103 und 104 Zellen/ml der Hefearten D. bruxellensis (DSM 70726), S. cerevisiae (DSM 1333), S. pombe (BCD 773), Z. bailii (MUCL 28823), C. tropicalis (ATCC 20247) und H. vineae (ATCC 20247) nachgewiesen. Die gleichen Arten wurden in den teilweise trübstoffreichen Getränken Apfelsaft (naturtrüb), Traubensaft, Rotund Weißwein mit einem um eine Zehnerpotenz höheren Nachweislevel zwischen 104 und 66 3 Ergebnisse 105 Zellen/ml detektiert (Tab. 3.11). Alle undotierten, vorangereicherten Getränkeproben waren negativ in der PCR im Kanal 640/Back 530 und bei der Kultivierung auf YM-Agar. Tab. 3.11: Eignung der Real-Time Consensus-PCR für Hefen in Kombination mit der mechanisch/thermischen Aufarbeitung für unterschiedliche Probenmatrices und Hefearten Dotierungslevel A: [Zellen/ml] 5 B: C: 1,0 x 10 1,0 x 104 1,0 x 103 undotiert 6,9 x 104 6,9 x 103 6,9 x 102 - [Zellen/ml] [KBE/ml] 1,0 x 105 1,0 x 104 1,0 x 103 undotiert 6,4 x 104 6,4 x 103 6,4 x 102 - [Zellen/ml] [KBE/ml] 5 D: 1,0 x 10 1,0 x 104 1,0 x 103 undotiert 3,2 x 105 3,2 x 104 3,2 x 103 - [Zellen/ml] [KBE/ml] 5 E: 1,0 x 10 1,0 x 104 1,0 x 103 undotiert 1,0 x 105 1,0 x 104 1,0 x 103 - [Zellen/ml] [KBE/ml] 5 F: [KBE/ml] 1,0 x 10 1,0 x 104 1,0 x 103 undotiert 9,4 x 104 9,4 x 103 9,4 x 102 - [Zellen/ml] [KBE/ml] 1,0 x 105 1,0 x 104 1,0 x 103 undotiert 1,1 x 105 1,1 x 104 1,1 x 103 - Cp-Werte im Kanal 640/Back 530 je Probenmatrix Apfelsaft YMRotwein Pils Gatorade (naturtrüb) Medium 31,89/32,2 -/33,25 29,06/29,2 29,45/30,1 27,79 -/-/31,27/30,9 31,95/31,9 n.b. -/-/32,05/32,1 32,68/32,6 n.b. -/-/-/-/Apfelsaft YMRotwein Pils Gatorade (naturtrüb) Medium 31,21/30,6 31,30/31,3 28,42/28,5 29,02/28,8 27,52 -/-/30,58/30,4 30,93/31,0 n.b. -/-/30,42/-/n.b. -/-/-/-/Bier (alTraubenYMEistee Weißwein koholfrei) saft Medium 24,81/25,0 26,63/26,6 30,46/30,4 27,11/27,6 23,14 28,62/28,3 29,95/29,8 31,67/29,2 30,37/30,3 n.b. 31,68/31,0 31,36/-/-/n.b. -/-/-/-/Bier (alTraubenYMEistee Weißwein koholfrei) saft Medium 29,66/29,9 39,91/28,7 28,97/30,5 31,05/30,9 28,90 31,64/31,4 33,85/31,7 -/-/n.b. -/-/-/-/n.b. -/-/-/-/YMApfelsaft Radler Weißwein Coca-Cola (naturtrüb) Medium 30,69/30,6 28,84/28,8 29,02/29,0 30,57/30,4 28,35 -/31,27/31,0 31,49/31,7 31,83/31,7 n.b. -/-/-/-/n.b. -/-/-/-/Apfelsaft YMCoca-Cola Radler Weißwein (klar) Medium 29,72/29,8 28,49/28,5 28,56/28,8 30,23/29,7 28,19 31,15/31,7 31,03/30,8 30,84/30,9 31,36/31,3 n.b. -/-/-/-/n.b. -/-/-/-/- Die Probenmatrices wurden vor der mechanisch/thermischen Aufarbeitung (Kap. 2.6.1) mit A: D. bruxellensis (DSM 70726), B: S. cerevisiae (DSM 1333), C: Sch. pombe (BCD 773), D: Z. bailii (MUCL 28823), E: C. tropicalis (ATCC 20247) oder F: H. vineae (DSM 70283) Zellen dotiert. Die Zellzahlen bzw. KBE wurden mikroskopisch und nach Kultivierung auf YM-Agar bestimmt (Kap. 2.12). n.b.: nicht bestimmt; -: negative Proben. 67 3 Ergebnisse 3.2.7.3 Sensitivität in Kombination mit der erweiterten, mechanisch/thermischen DNA-Extraktion Für einige Probenmatrices wie trübstoffreiche Getränke und Weine wurde die DNAExtraktion erweitert, um die Qualität des in der PCR eingesetzten Probenmaterials und damit die Sensitivität des Nachweissystems zu erhöhen. Die Erweiterung bestand in einem zusätzlichen Proteinase K Verdau und einer Reinigung über Säulenmaterial (Kap. 2.6.3). Mit dieser Erweiterung wurde die Nachweisgrenze für die Probenmatrices Apfelsaft (naturtrüb), Rotwein, Eistee und Traubensaft auf 103 bis 104 Zellen/ml S. cerevisiae gesenkt (Tab. 3.12). Alle undotierten, vorangereicherten Getränkeproben waren negativ in der PCR im Kanal 640/Back 530 und bei der Kultivierung auf YM-Agar. Tab. 3.12: Eignung des Real-Time Consensus-PCR für Hefen in Kombination mit der erweiterten, mechanisch/thermischen Aufarbeitung für unterschiedliche Probenmatrices Dotierungslevel Cp-Werte je Probenmatrix Apfelsaft (naturtrüb) 28,85/29,07 Rotwein Eistee Traubensaft YM-Medium 27,37/27,26 26,55/26,92 29,99/26,95 24,79 [Zellen/ml] [KBE/ml] 1,0 x 105 9,6 x 104 1,0 x 10 4 9,6 x 10 3 30,95/30,79 29,71/29,84 29,25/29,28 29,90/29,94 n.b. 1,0 x 10 3 9,6 x 10 2 -/- -/- 30,05/30,65 27,73/31,46 n.b. -/- -/- -/- -/- - undotiert - Die Probenmatrices wurden vor der erweiterten, mechanisch/thermischen Aufarbeitung (Kap. 2.6.3) mit S. cerevisiae (DSM 1333) Zellen dotiert. Die Zellzahlen bzw. KBE wurden mikroskopisch und nach Kultivierung auf YM-Agar bestimmt (Kap. 2.12). n.b.: nicht bestimmt; -: negative Proben. 3.2.7.4 Detektionszeit für unterschiedliche Hefearten Die Detektionszeit eines Nachweissystems wird in diesem Zusammenhang als die Zeit definiert, die für einen Mikroorganismus benötigt wird, damit dieser über Kultivierung eine Konzentration erreicht, die im Nachweisbereich des Systems liegt. Diese Zeit ist abhängig von der Ausgangskonzentration, der Verdoppelungszeit und der Lag-Phase (Adaptionsphase) des Mikroorganismus in einem bestimmten Medium. Für einen Organismus oder eine Population in einem Medium vergrößert sich die Detektionszeit je geringer die Ausgangskonzentration ist. Um diese Detektionszeit zu ermitteln wurden Getränkeproben mit 1, 10 oder 100 Hefezellen/ml beimpft und in YM-Medium angereichert (1:10-verdünnt, 28 °C, 150 U/min). Die Anreicherungen wurden im Duplikat angesetzt und je Anreicherung zwei 1 ml Proben nach 24 und 48 Stunden aufgearbeitet. Mit den langsam wachsenden Hefearten D. bruxellensis und besonders Sch. pombe (Generationszeiten von bis zu 4 Stunden) und den schwierigen Probenmatrices Orangensaft bzw. 68 3 Ergebnisse Apfelsaft (naturtrüb) wurde das Nachweissystem in Kombination mit der erweiterten, mechanisch/thermischen Aufarbeitung getestet (Tab. 3.13). Tab. 3.13: Detektionszeit für langsam wachsende Hefen Dotierungslevel A: B: [Zellen/ml] [KBE/ml] 1,0 x 102 1,0 x 101 1,0 x 100 undotiert 1,0 x 102 1,0 x 101 1,0 x 100 undotiert 1,0 x 102 1,0 x 101 1,0 x 100 4,1 x 102 4,1 x 101 4,1 x 100 - nach 24 Stunden Anreicherung Anreicherung 1 2 +/+ +/+ -/-/-/-/-/-/-/-/-/-/-/-/-/-/- nach 48 Stunden Anreicherung Anreicherung 1 2 +/+ +/+ +/+ +/+ +/+ +/+ -/-/+/+ +/+ +/+ +/+ +/+ -/-/-/- Die Probenmatrices A: Orangensaft bzw. B: Apfelsaft (naturtrüb) wurden vor der Anreicherung mit YM-Medium mit A: D. bruxellensis (DSM 70726) oder B: Sch. pombe (BCD 773) Zellen dotiert. Die Zellzahlen bzw. KBE wurden mikroskopisch und nach Kultivierung auf YM-Agar bestimmt (Kap. 2.12). Nach 24 bzw. 48 Stunden Anreicherung wurden Proben entnommen, die nach Aufarbeitung mit der erweiterten, mechanisch/thermischen Methode mit der Real-Time Consensus-PCR für Hefen getestet wurden (Kap. 2.15.2). -: Probe negativ; +: Probe positiv. Abb. 3.20: Real-Time PCR Nachweis von D. bruxellensis in Orangensaft Nach 48 Stunden Anreicherung mit YM-Medium wurde der vor der Anreicherung mit 102 Zellen/ml (schwarze Linie), 101 Zellen/ml (blaue Linie) oder 100 Zellen/ml (rote Linie) D. bruxellensis (DSM 70726) dotierte Orangensaft mit der erweiterten, mechanisch/thermischen DNA-Extraktionsmethode aufgearbeitet. Die Proben wurden anschließend mit der Real-Time Consensus-PCR für Hefen getestet. Als Negativkontrolle wurde eine undotierte Anreicherung (grüne Linie) verwendet. 69 3 Ergebnisse Der unterste Dotierungslevel von einer Zelle/ml Orangensaft wurde bei D. bruxellensis nach 48 Stunden Anreicherung nachgewiesen (Tab. 3.13 und Abb. 3.20). Das Wachstum von Sch. pombe in einer Anreicherung mit Apfelsaft (naturtrüb) war dagegen bei der geringsten Ausgangskontamination von einer Zelle/ml (4,1 KBE/ml) nach 48 Stunden in nur einer Anreicherung nachweisbar (Tab. 3.13). Alle undotierten, vorangereicherten Getränkeproben waren negativ in der PCR im Kanal 640/Back 530 und bei der Kultivierung auf YM-Agar. Tab. 3.14: Detektionszeit in Abhängigkeit von der Hefeart und der Probenaufarbeitung Dotierungslevel A: B: C: D: [Zellen/ml] [KBE/ml] 1,0 x 102 1,1 x 102 1,0 x 101 1,1 x 101 1,0 x 100 1,1 x 100 undotiert - 1,0 x 102 6,3 x 101 1,0 x 101 6,3 x 100 1,0 x 100 6,3 x 10-1 undotiert - 1,0 x 102 7,5 x 101 1,0 x 101 7,5 x 100 1,0 x 100 7,5 x 10-1 undotiert - 1,0 x 102 4,1 x 101 1,0 x 101 4,1 x 100 1,0 x 100 4,1 x 10-1 undotiert - nach 24 Stunden Anreicherung Anreicherung 1 2 +/+ (a) +/+ (a) +/+ (b) +/+ (b) +/+ (a) +/+ (a) +/+ (b) +/+ (b) -/- (a) -/- (a) -/- (b) -/- (b) -/- (a) -/- (a) -/- (b) -/- (b) +/+ (a) +/+ (a) -/- (b) -/- (b) -/- (a) -/- (a) -/- (b) -/- (b) -/- (a) -/- (a) -/- (b) -/- (b) -/- (a) -/- (a) -/- (b) -/- (b) +/+ (a) +/+ (a) +/+ (b) +/+ (b) +/+ (a) +/+ (a) +/+ (b) +/+ (b) +/+ (a) -/+ (a) -/+ (b) +/+ (b) -/- (a) -/- (a) -/- (b) -/- (b) -/- (a) -/+ (a) -/+ (b) -/- (b) -/- (a) -/- (a) -/- (b) -/- (b) -/- (a) -/- (a) -/- (b) -/- (b) -/- (a) -/- (a) -/- (b) -/- (b) nach 48 Stunden Anreicherung Anreicherung 1 2 +/+ (a) +/+ (a) +/+ (b) +/+ (b) +/+ (a) +/+ (a) +/+ (b) +/+ (b) +/+ (a) +/+ (a) +/+ (b) +/+ (b) -/- (a) -/- (a) -/- (b) -/- (b) +/+ (a) +/+ (a) +/+ (b) +/+ (b) +/+ (a) +/+ (a) +/+ (b) +/+ (b) +/+ (a) +/+ (a) +/+ (b) +/+ (b) -/- (a) -/- (a) -/- (b) -/- (b) +/+ (a) +/+ (a) +/+ (b) +/+ (b) +/+ (a) +/+ (a) +/+ (b) +/+ (b) +/+ (a) +/+ (a) +/+ (b) +/+ (b) -/- (a) -/- (a) -/- (b) -/- (b) +/+ (a) +/+ (a) +/+ (b) +/+ (b) +/+ (a) +/+ (a) +/+ (b) +/+ (b) +/+ (a) +/+ (a) +/+ (b) +/+ (b) -/- (a) -/- (a) -/- (b) -/- (b) Die Probenmatrices Coca-Cola (A und B) bzw. Radler (C und D) wurden vor der Anreicherung mit YM-Medium mit A: P. membranaefaciens (DSM 70178), B: Z. bailii (MUCL 70178), C: C. tropicalis (ATCC 20247) oder D: H. vineae (DSM 70283) Zellen dotiert. Die Zellzahlen bzw. KBE wurden mikroskopisch und nach Kultivierung auf YM-Agar bestimmt (Kap. 2.12). Nach 24 bzw. 48 Stunden Anreicherung wurden Proben entnommen, die nach Aufarbeitung mit der erweiterten, mechanisch/thermischen (a) oder (b) der mechanisch/thermischen Methode mit der Real-Time ConsensusPCR für Hefen getestet wurden (Kap. 2.15.2). Jede Anreicherung wurde im Duplikat angesetzt und je Extraktionsmethode im Duplikat getestet. -: Probe negativ; +: Probe positiv. 70 3 Ergebnisse Die Detektionszeit in Abhängigkeit von den Hefearten P. membranaefaciens (DSM 70178), Z. bailii (MUCL 70178), C. tropicalis (ATCC 20247) und H. vineae (DSM 70283) wurde mit Anreicherungen mit Coca-Cola und Radler im direkten Vergleich mit der mechanisch/thermischen und der erweiterten, mechanisch/thermischen Aufarbeitungsmethode getestet (Tab. 3.14). Unabhängig von der Hefeart, der Probenmatrix und der eingesetzten Probenaufarbeitung wurde nach 48 Stunden Anreicherung der niedrigste Dotierungslevel mit 1 Zelle/ml detektiert. 3.2.7.5 Sensitivität bei einer hohen Begleitflora Die Auswirkung einer sehr hohen Begleitflora auf die Nachweisgrenzen und die Aufarbeitungsmethoden wurde am Beispiel einer Flüssigkultur (Peptonwasser) mit 1010 KBE/ml E. coli (DSM 30083) getestet. Die beiden Hefearten S. cerevisiae und Z. bailii wurden mit drei Verdünnungsstufen (103, 104 und 105 Zellen/ml), sowohl mit als auch ohne Begleitflora und mit beiden mechanisch/thermischen Probenaufarbeitungsmethoden jeweils im Duplikat getestet. Die Hefearten S. cerevisiae und Z. bailii wurden auch bei einer hohen Begleitflora eines Nicht-Zielorganismus ohne Sensitivitätseinbußen nachgewiesen (Tab. 3.15 und Abb. 3.21). Tab. 3.15: Sensitivität bei einer hohen Begleitflora Dotierungslevel A: B: Cp-Werte (640/Back530) 10 [Zellen/ml] [KBE/ml] mit 10 KBE/ml E. coli ohne E. coli 1,0 x 105 2,9 x 104 1,0 x 104 2,9 x 103 1,0 x 103 2,9 x 102 undotiert - 1,0 x 105 1,6 x 104 1,0 x 104 1,6 x 103 1,0 x 103 1,6 x 102 undotiert - 25,46/25,44 (a) 27,63/27,64 (b) 28,15/28,10 (a) 29,76/29,72 (b) 29,80/30,19 (a) 30,43/30,00 (b) - (a) - (b) 25,80/25,84 (a) 28,74/28,67 (b) 28,23/28,45 (a) 30,29/30,48 (b) 26,14/27,46 (a) 30,01/27,01 (b) - (a) - (b) 26,00/25,90 (a) 28,09/28,26 (b) 28,97/29,27 (a) 30,25/30,67 (b) 30,52/30,78 (a) 31,20/32,56 (b) - (a) - (b) 26,05/26,76 (a) 29,63/29,60 (b) 28,90/29,15 (a) 31,08/31,52 (b) 31,03/31,14 (a) 30,11/33,70 (b) - (a) - (b) Peptonwasser mit oder ohne 1010 KBE/ml E. coli (DSM 30083) wurde mit A: S. cerevisiae (DSM 1333) oder B: Z. bailii (MUCL 28823) Zellen dotiert, und nach Aufarbeitung mit der erweiterten, mechanisch/thermischen (a) (Kap. 2.6.3) oder mit der mechanisch/thermischen Extraktionsmethode (b) (Kap. 2.6.1) mit der Real-Time Consensus-PCR für Hefen getestet. Die Zellzahlen bzw. KBE wurden mikroskopisch und nach Kultivierung auf YM- bzw. Caso-Agar bestimmt (Kap. 2.12). Alle Aufarbeitungen wurden im Duplikat durchgeführt. 71 3 Ergebnisse Abb. 3.21: Sensitivität bei Anwesenheit einer hohen Begleitflora Das Real-Time Consensus-PCR für Hefen wurde mit Proben (Peptonwasser) getestet, die mit (durchgezogene Linien) oder ohne (Punkte) 1010 KBE/ml E. coli und mit 105 Zellen/ml (schwarz), 104 Zellen/ml (blau) oder 103 Zellen/ml (rot) S. cerevisiae (DSM 1333) dotiert wurden. Die Proben wurden mit der mechanisch/thermischen Methode aufgearbeitet. Als Negativkontrolle wurde eine undotierte Probe verwendet (grüne Linie). 72 4 Diskussion 4 Diskussion Im Rahmen dieser Arbeit wurden zwei Real-Time PCR-Systeme zum Nachweis von getränkerelevanten Hefen auf Basis der LightCycler® Technologie mit Hybridisierungssonden entwickelt. Für beide Systeme wurden interne Amplifikationskontrollen und Positivkontrollen hergestellt und zwei DNA-Extraktionssysteme bereitgestellt. Ein hoch spezifischer und sensitiver Einzelnachweis für die wichtigste, bierschädliche Saccharomyces Fremdhefe, S. cerevisiae var. diastaticus, wurde entwickelt, indem die sequenziellen Unterschiede zwischen den Glucoamylase kodierenden Genen von S. cerevisiae var. diastaticus (STA1-3) und S. cerevisiae (SGA1) ausgenutzt wurden. Die hohe Nachweisempfindlichkeit des PCR-Systems von 5 bis 10 GÄ pro Reaktion ermöglichte in Kombination mit einer schnellen, mechanisch/thermischen Probenaufarbeitung den Nachweis von 102 bis 103 S. cerevisiae var. diastaticus Zellen/ml bei einer Hintergrundpopulation von 108 Zellen/ml S. cerevisiae. Die Robustheit des Systems wurde durch Testung von 66 unterschiedlichen Probenmatrices gezeigt und die Praxistauglichkeit direkt bei vier Brauereien verifiziert. Die Sequenzierung eines Abschnitts des EF-3 Gens von 93 Hefestämmen lieferte die Grundlage für die Entwicklung einer Real-Time Consensus-PCR zum Nachweis von getränkerelevanten Hefen. Der Nachweis von allen 252 getesteten Hefestämmen wurde bei dem Assay durch degenerierte Primer und Hybridisierungssonden ermöglicht, ohne dass mit der DNA von einer der 71 getesteten Bakterien falsch-positive Ergebnisse auftraten. Der Nachweis konnte nicht zur Identifizierung der Hefearten oder -gattungen eingesetzt werden und die Abgrenzung zu den Schimmelpilzen, die ebenfalls das EF-3 Gen enthalten, ließ sich nicht zu 100 % erreichen. Die Sensitivität des Systems lag in Abhängigkeit von der Hefeart zwischen 10 und 250 GÄ pro Reaktion und in Kombination mit einer Erweiterung der mechanisch/thermischen Probenaufarbeitung bei 103 bis 104 Zellen/ml. Bei sehr niedrig kontaminierten Getränkeproben mit 1 bis 100 Zellen/ml war ein Nachweis nach zwei bis drei Tagen Flüssiganreicherung in YM-Medium möglich. 4.1 Beurteilung der STA1-3 und EF-3 Gene als Targetmoleküle Die Schädlichkeit und Gefährlichkeit der Hefe S. cerevisiae var. diastaticus für die Bierindustrie beruht auf der Produktion einer extrazellulären Glucoamylase und der ansonsten physiologischen Ähnlichkeit zu den Brauhefen der gleichen Art. Die Glucoamylase (1,4-α-DGlucanglucohydrolase, EC 3.2.1.3) befähigt diese Varietät, sowohl als Primärkontamination im Brauprozess für Geschmacks- und Geruchsveränderungen zu sorgen, als auch als Sekundärkontamination im fertigen Bier die Restnährstoffe aus Stärke und Dextrinen zu Glucose abzubauen und eine Übervergärung mit den negativen Folgen der Nachtrübung, Ge- 73 4 Diskussion schmacks-/Geruchsveränderung und Bodensatzbildung hervorzurufen. Ihre physiologische Ähnlichkeit zu den Brauhefen erschwert zudem die einfache und schnelle Detektion mit konventionellen, kultivierungsabhängigen Methoden besonders innerhalb des Brauprozesses, bei Anwesenheit der Brauhefe. Die Glucoamylase kodierenden Gene STA1-3 sind demnach die idealen Targets für die Entwicklung einer molekularbiologischen Schnellmethode, um S. cerevisiae var. diastaticus nachzuweisen und von S. cerevisiae unterscheiden zu können. Seit der Entdeckung der Glucoamylase Genfamilie STA1-3 durch Tamaki et al. (1978) und Erratt und Stewart (1978) in S. cerevisiae var. diastaticus ist diese Gegenstand umfangreicher Untersuchungen gewesen, nicht nur wegen ihres bierschädlichen Potentials sondern auch aus Interesse an einer biotechnologischen Nutzung zur Gewinnung von Ethanol aus Stärke und der ungewöhnlichen Länge und Komplexität des Promotors (Erratt und Nasim 1986, Laluce und Mattoon 1984, Laluce et al. 1988, Lambrechts et al. 1991, 1994, Vivier et al. 1999). Molekulare Charakterisierungen der Gene zeigten, dass sie auf den Chromosomen II (STA2), IV (STA1) und XIV (STA3) lokalisiert sind und nahezu identische Sequenzen haben (Bignell und Evans 1990, Lambrechts et al. 1991, Pretorius und Marmur 1988, Yamashita et al. 1985a,b). Außerdem zeigte sich, dass die Gene zwar nur bei S. c. var. diastaticus Stämmen vorhanden sind, die einzelnen funktionalen Bereiche der Gene jedoch bei allen untersuchten S. cerevisiae Stämmen als Bestandteil der Gene MUC1 (FLO11) und SGA1 vorkommen. Der 5´-Bereich der STA Gene wird durch die zwei Sequenzabschnitte S1 und S2 gebildet, die beide auch im Gen MUC1 (FLO11) vorliegen, das ein membrangebundenes, mucin-ähnliches Protein kodiert (Lambrechts et al. 1996, Pretorius et al. 1986, Yamashita et al. 1987). Die S2 Sequenz bildet in den STA Genen den Promotor und kodiert die ersten 96 Nucleotide des anschließenden offenen Leserasters, wohingegen die folgende S1 Sequenz einen Serin/Threonin-reichen Bereich kodiert (Yamashita et al. 1985b). Die Sequenzen in der Mitte und dem 3´-Ende der STA Gene kodieren die katalytische Domäne der Proteine, die identisch ist mit einem Bereich im Gen SGA1, das auf dem Chromosom IX lokalisiert ist und eine sporulationsabhängige, intrazelluläre Glucoamylase kodiert (Pretorius und Marmur 1988, Vivier et al. 1997, Yamashita und Fukui 1985, Yamashita et al. 1987). Die Gene STA1-3 sind sehr wahrscheinlich aufgrund ihrer Homologie zu den Genen MUC1 (FLO11) und SGA1 aus einer Rekombination derselben mit anschließender Sequenzvervielfältigung hervorgegangen (Yamashita et al. 1987). Unterstützt wird diese These nicht nur durch die Sequenzübereinstimmungen sondern auch durch drei weitere Argumente. Erstens sind die STA Gene im Bereich der Telomere positioniert, wohingegen die Gene MUC1 (FLO11) und SGA1 eine zentrale Position im Chromosom IX einnehmen. Zweitens sind die STA Gene in nur einigen S. cerevisiae Stämmen vorhanden, die Gene MUC1 (FLO11) und SGA1 liegen jedoch in allen S. cerevisiae Stämmen vor. Drittens existieren übereinstimmen- 74 4 Diskussion de, sich wiederholende Sequenzen an beiden Seiten der propagierten Junktionen (Lambrechts et al. 1995, Yamashita et al. 1985b, 1987). Diese nur in S. c. var. diastaticus vorkommende Anordnung der Sequenzabschnitte in den STA Genen in der Reihenfolge S2-S1-SGA (Abb. 3.1) wurde erfolgreich für die Entwicklung des spezifischen PCR Nachweises ausgenutzt. Ein ähnliches Primerdesign mit einem 5´-Primer aufbauend auf der S1 Sequenz und einem 3´-Primers aufbauend auf der SGA Sequenz wurde bereits von Yamauchi et al. (1998) erfolgreich zur Entwicklung eines spezifischen PCR-Systems zum Nachweis von S. c. var. diastaticus verwendet. Die Detektion eines spezifischen 868 bp langen PCR-Produkts erfolgte hierbei nach Amplifikation mit einem konventionellen Thermocycler über Agarosegelelektrophorese. Für die Entwicklung einer Consensus-PCR zum Nachweis aller getränkerelevanten Hefen wurde ein Target gesucht, das in allen Hefen vorkommt, eine grundlegende Funktion erfüllt und konservierte, spezifische Sequenzabschnitte aufweist. Da die Möglichkeit einer Differenzierung zwischen lebenden und toten Zellen über RT-PCR nicht ausgeschlossen werden sollte, wurde außerdem nach einem mRNA kodierenden Gen gesucht. Der Translationsprozess ist bei Hefen ein komplexes Zusammenspiel aus Initiation, Elongation und Termination, das durch eine Vielzahl an Proteinen gesteuert wird (Merrick 1992). Bei der Elongation benötigen Hefen und Schimmelpilze den Elongationsfaktor 3 (EF-3), der bisher nur bei diesen Eukaryoten nachgewiesen wurde, essentiell für das vegetative Wachstum ist und für den bei Prokaryoten kein funktionsgleiches Gegenstück existiert (Dasmahapatra und Chakraburtty 1981, Hutchison et al. 1984, Sandbaken et al. 1990a,b, Skogerson und Wakatama 1976). Diese überraschende Einzigartigkeit des Elongationsfaktors 3 bei Hefen und Schimmelpilzen innerhalb eines ansonsten hoch konservierten, biochemischen Prozesses scheint jedoch nicht uneingeschränkt gültig zu sein. Bei dem Chlorella Virus CVK2 konnte ein mutmaßlich EF-3 kodierendes Gen isoliert werden, dem jedoch eine funktionale Domäne fehlt (Belfield et al. 1995, Yamada et al. 1993). Eine ribosomale ATPase (RbbA) konnte außerdem bei E. coli identifiziert werden, die in der C-terminalen Hälfte der Aminosäuresequenz 40 % Ähnlichkeit mit dem EF-3 Protein von S. cerevisiae aufweist (Kiel et al. 1999). Das 1044 Aminosäuren lange Protein EF-3 wird durch ein „single-copy“ Gen (EF-3) kodiert (Chromosom XII bei S. cerevisiae) und enthält strukturelle Motive, die aufgrund ihrer Homologie zu Proteinen mit bekannten Funktionen auf eine Interaktion des Proteins mit tRNA, rRNA und ATP hinweisen (Qin et al. 1990). Ein 200 Aminosäure langes Motiv am N-terminalen Ende weist 30 % Homologie zu dem ribosomalen Protein S5 von E. coli auf und interagiert mit der 18 S rRNA und den 80 S Ribosomen (Gontarek et al. 1998, Kovalchuke und Chakraburtty 1995). Das 75 4 Diskussion Vorhandensein von zwei ATP-Bindekassetten (oder Walker Boxen), von der die Erste eine intrinsische und die Zweite eine ribosomen-abhängige ATPase Aktivität aufweist, ist ein weiteres Merkmal des Elongationsfaktors 3 (Qin et al. 1990). Außerdem existiert zwischen den beiden Walker Signaturen der zweiten ATP-Bindekassette, die mit 188 Aminosäuren ungewöhnlich weit auseinander liegen, eine hoch konservierte Sequenz (ELVES), die in tRNAbindenden Proteinen zu finden ist (Belfield und Tuite 1993, Belfield et al. 1995, Colthurst et al. 1991a). Diese strukturellen Motive korrelieren mit der etablierten Funktion von EF-3, die in der ATP-abhängigen Stimulation der Bindung des ternären Komplexes aus EF-1α, GTP und Aminoacyl-tRNA an die ribosomale A-Stelle durch Entfernen der deacylierten tRNA von der E-Stelle besteht (Kamath und Chakraburtty 1989, Triana-Alonso et al. 1995, Uritani und Miyazaki 1988). Als Target für die Entwicklung einer Consensus-PCR wurde der 106 Aminosäuren (bzw. 107 Aminosäuren bei Sch. pombe) lange Bereich zwischen den beiden Walker Signaturen der zweiten ATP-Bindekassette ausgewählt, der nicht in anderen Proteinen mit ATPBindekassetten vorkommt und große sequenzielle Übereinstimmung unter den von Hefen bekannten Sequenzen aufweist (Belfield et al. 1995). Bisher waren Sequenzen dieses Bereichs von 9 Ascomyceten (S. cerevisiae, C. albicans, C. maltosa, C. melibiosica, C. zeylanoides, K. lactis, P. pastoris, S. pombe und Y. lipolytica) und von einer Hefe der Unterabteilung der Basidiomycota (C. neoformans) bekannt (Blakely 2001, Di Domenico et al. 1992, Mita et al. 1997, Myers et al. 1992, Qin et al. 1990, Sandbaken et al. 1990a,b, Uritani et al. 1999). Die Übereinstimmung der Aminosäuresequenz des Teilstücks liegt innerhalb dieser Ascomyceten bei mindestens 74 % und ein deutlicher Sequenzunterschied besteht zwischen den Ascomyceten und der Sequenz von C. neoformans (33 % Sequenzähnlichkeit zu S. cerevisiae). Die Sequenzierungen dieses Bereiches von 93 Hefestämmen, von denen zum größten Teil bisher noch keine Informationen vorlagen, und die phylogenetische Untersuchung bestätigten die starke Sequenzhomologie unter den Ascomyceten und gleichzeitig die Distanz zu den Basidiomyceten. Im Gegensatz hierzu ist die Sequenzhomologie zwischen den beiden Unterabteilungen bei dem Elongationsfaktor 1α, der in allen Eukaryoten vorkommt, viel größer, da z. B. S. cerevisiae und C. neoformans eine Sequenzidentität von 84,7 % aufweisen (Thornewell et al. 1997). Die Ergebnisse bestätigen die vermutete, größere evolutionäre Drift des Elongationsfaktors 3 innerhalb des Reichs der Pilze. Außerdem zeigten die neu hinzugekommenen Sequenzen von weiteren Hefen der Unterabteilung der Basidiomyceten, dass die Sequenzübereinstimmung innerhalb dieser Unterabteilung (mindestens 67 %) ähnlich hoch ist wie bei den Ascomyceten (mindestens 68 %). Die phylogenetische Distanz zwischen den Unterabteilungen der Ascomycota und Basidiomycota aufgrund der EF-3 Sequenzen korreliert mit der phylogenetischen Ordnung der He- 76 4 Diskussion fen, die auf Sequenzen der 26 S ribosomalen RNA basiert (Fell et al. 2000, Kurtzman 1994, Kurtzman und Robnett 1998). Weitere Parallelen können zwischen den phylogenetischen Stammbäumen, die mit den EF-3 oder den 18 S rDNA Sequenzen erstellt wurden, in Bezug auf die Gattung Saccharomyces gezogen werden (James et al. 1997). Die Gattung musste aufgrund beider Analysen als polyphyletisch eingestuft werden, da sie mit Arten der Gattungen Zygosaccharomyces, Kluyveromyces und Torulaspora vermischt ist (Abb. 3.12). Viele der zurzeit akzeptierten Hefegattungen wurden nach einem umfangreichen Vergleich der D1/D2 Domäne der 26 S rDNA von Kurtzman und Robnett (1998) als nicht monophyletisch eingestuft. Monophyletische Gruppen bildeten, wie bei dem über die D1/D2 Sequenzen der 26 S rDNA ermittelten Stammbaum, nur die Gattungen Dekkera und Schizosaccharomyces, wobei die Letztere auch zu einer anderen Klasse (Archiascomycetes) als die sonstigen untersuchten Ascomyceten (Hemiascomycetes) gehörte (Kurtzman und Robnett 1998). Der sequenzierte Bereich des EF-3 Gens ist jedoch zu klein, um detaillierte Aussagen über die phylogenetische Verwandtschaft der einzelnen Gattungen und Arten machen zu können. Das EF-3 Gen wurde jedoch von einigen Autoren als möglicher taxonomischer Marker für das Phylum Fungi genannt und für die Identifizierung von Sauerteighefen über RFLP-PCR eingesetzt (Belfield und Tuite 1993, Colthurst et al. 1991b, Mäntynen et al. 1999). Diese RFLP-PCR Analyse von Mäntynen et al. (1999) konnte nicht auf die Hefearten Candida geochares, Cryptococcus laurentii, Rhodosporidium toruloides und Schizosaccharomyces pombe angewendet werden, da keine PCR-Produkte mit den Primern, die über die Sequenzinformationen von S. cerevisiae und C. albicans entwickelt wurden, generiert werden konnten. Der Mikrosatelliten-DNA Polymorphismus in der Promotor Region des EF-3 Gens wurde außerdem als Target zur Typisierung von C. albicans verwendet. (Bretagne et al. 1997, Dalle et al. 2000). Aber auch wenn das EF-3 Gen in seiner Gesamtheit für phylogenetische Analysen geeignet ist, sollte immer davon ausgegangen werden, dass phylogenetische Stammbäume aufbauend auf unterschiedlichen Genen zur Lösung von taxonomischen Problemen auch unterschiedliche Topologien aufweisen können (McCarroll et al. 1983, Seifert et al. 1995). Polyphasische Untersuchungen mit unterschiedlichen, unabhängigen Genen und weitere Merkmale wie z. B. die Morphologie sollten daher zur Bestätigung der Stammbäume herangezogen werden (Valente et al. 1999). Der Elongationsfaktor 1α (EF-1 α) wurde bereits als Target für den Nachweis einiger Hefe(S. cerevisiae, C. albicans) und Schimmelpilzarten (Mucor racemosus, Aureobasidium pullulans) über RT-PCR in Milch, Bier und Joghurt verwendet (Vaitilingom et al. 1998). Versuche, das Consensus-PCR System für Hefen ebenfalls zu einer RT-PCR weiterzuentwickeln, waren nicht erfolgreich, da das Gesamtsystem aufgrund der großen Anzahl an Primern und 77 4 Diskussion Sonden zu komplex war. Durch diese große Anzahl an Primern und Sonden setzte sehr wahrscheinlich schon während der RT-Reaktion eine zu starke Primerdimerbildung ein, die die nachfolgende PCR unmöglich machte. Mit einer reduzierten Anzahl an Primern und nur einem Hybridisierungssondenpaar konnte jedoch die mRNA des EF-3 Gens von S. cerevisiae var. diastaticus in einer Real-Time RT-PCR spezifisch detektiert werden. Die Daten zu diesem Experiment werden im Kapitel 6.3 im Anhang präsentiert. Für die Entwicklung der Real-Time Consensus-PCR für Hefen lieferten die Sequenzergebnisse zwei Notwendigkeiten, zum einen mussten degenerierte Oligonucleotide verwendet werden und zum anderen mussten drei unabhängige PCR-Assays für die Hemiascomyceten, die Gattung Schizosaccharomyces und die Basidiomyceten zu einer Multiplex-PCR kombiniert werden. Diese Kombination machte eine Identifizierung von Arten oder Gattungen mit diesem System unmöglich. 4.2 Spezifität und Sensitivität der Real-Time PCR-Assays Die Spezifität von Real-Time PCR-Assays mit Hybridisierungssonden beruht zum einen wie bei herkömmlichen PCR-Systemen auf den Primern, aber zum anderen auch auf der gleichzeitigen, spezifischen Hybridisierung von zwei fluoreszenzmarkierten Sonden, um die Amplifikate zu detektieren. Bei dem Nachweissystem für S. cerevisiae var. diastaticus konnte durch die Anordnung der vier Oligonucleotide sowohl die PCR als auch die Detektion der PCR-Amplifikate 100-%ig spezifisch gestaltet werden. Dieses Ergebnis stimmt mit Ergebnissen von Yamauchi et al. (1998) überein, die mit einer konventionellen PCR ebenfalls eine 100-%ige Spezifität erreichten. Dagegen konnte das Nachweissystem für alle Hefen durch die Verwendung von degenerierten und vielen unterschiedlichen Primern auf der Ebene der PCR nicht 100-%ig spezifisch gestaltet werden. Die Spezifität wurde jedoch durch die Verwendung von Hybridisierungssonden so weit erhöht, dass keine falsch-positiven Ergebnisse durch bakterielle DNA verursacht wurden. Alle getesteten Hefen waren positiv, aber auch 13 Schimmelpilzarten wurden positiv getestet. Dieses Ergebnis war aufgrund der Heterogenität der EF-3 Zielsequenzen zu erwarten, da die degenerierten Oligonucleotide auch aufgrund der mit berücksichtigten Redundanz des genetischen Codes eine große Sequenzvariabilität abdeckten. Die Unspezifität in Bezug auf einige Schimmelpilze kann jedoch auch als ein Vorteil angesehen werden. Die gemeinsame Erfassung von Hefen und Schimmelpilzen kann von Nutzen sein, da Schimmelpilze ebenfalls zum Verderb von Getränken führen und durch die Bildung von Mycotoxinen gefährlich für die menschliche Gesundheit sein können. Die Ergebnisse zeigten an, dass durch die Sequenzierung des EF-3 Genabschnitts von getränkerelevanten Schimmelpilzen der Assay zu einem Gesamtnachweis für Hefen und Schimmelpilzen erweitert werden könn- 78 4 Diskussion te, wie zurzeit durch die kultivierungsabhängigen Standardmethoden vorgegeben (Anonymus 1987). Auch wenn die ascosporogenen Hefen mit Ausnahme der Gattung Schizosaccharomyces aufgrund der rDNA eine monophyletische Gruppe (Hemiascomycetes) bilden, die sich von filamentösen Arten der Euascomycetes unterscheidet, könnte demnach ein Consensus-System für Hefen und Schimmelpilze möglich sein (Kurtzman 1994). Die Unterschiede in der Komplexität der beiden Assays zeigten sich auch in den Sensitivitätstestungen mit Protein- und RNA-freier, quantifizierter DNA. Die Real-Time PCR für S. c. var. diastaticus ist mit einer Nachweisgrenze zwischen 5 und 10 GÄ pro Probenvolumen von 5 µl sehr sensitiv. Teilweise wurde auch 1 GÄ pro Reaktion nachgewiesen, was einer eingesetzten DNA-Menge von 13,3 fg entspricht. Die theoretisch erreichbare Empfindlichkeit des PCR-Systems konnte demnach auch praktisch realisiert werden, wenn von maximal drei STA Gensequenzen pro Chromosomensatz auszugehen ist und zudem eine Konkurrenz zu der Amplifikation der internen Amplifikationskontrolle besteht. Die Sequenzen der Gene STA1 und STA2 sind bekannt und bis auf eine Base identisch, außerdem besitzen alle STA Gene die gleiche Restriktionskarte, so dass höchstwahrscheinlich auch das noch nicht sequenzierte STA3 Gen ein Target für die PCR darstellt (Lambrechts et al. 1991, Pardo et al. 1986 und Yamashita et al. 1985a,b). Die Real-Time Consensus-PCR für Hefen konnte dagegen nicht so weit optimiert werden, dass die theoretisch mögliche Nachweisgrenze erreicht wurde. Die Empfindlichkeit lag zwischen 10 und 250 GÄ pro Reaktion und war abhängig von der jeweiligen Hefeart. Diese verminderte Sensitivität lässt sich mit der Komplexität der Multiplex-PCR und den notwendigen Degenerierungen der Oligonucleotide erklären. Die Optimierung der Multiplex-PCR wurde besonders durch die sehr unterschiedlichen GC-Gehalte im Target Bereich erschwert, die sich zum einen auf das Design der Primer und zum anderen auf die Annealingtemperatur auswirkten. Beim Einsatz von degenerierten Primern ist es nicht zu vermeiden, dass sehr viele unterschiedliche Primer mit unterschiedlichen Schmelztemperaturen im Reaktionsansatz vorliegen. Die Bildung von Primerdimeren und unspezifischen Amplifikaten mit bakterieller DNA, die den Einsatz von SYBR®-Green I zur Detektion der Amplifikate unmöglich machte, könnte durch den Einsatz dieser degenerierten Primer verstärkt worden sein. Das Primerdesign, für das einige Computerprogramme entwickelt wurden, wird als wichtiger Punkt zur Vermeidung von Primerdimeren angesehen (Abd-Elsalam 2003). Diese Programme und Regeln für das Primerdesign wie z. B. die Vermeidung von Sequenzen, die zu einem Annealing der Primer untereinander oder innerhalb der eigenen Sequenz führen können, sind bei degenerierten Primern schwer anzuwenden. Eine weitere Strategie zur Vermeidung von Primerdimeren, die bei den entwickelten PCR-Systemen zum Einsatz kam, ist die Anwen- 79 4 Diskussion dung einer so genannten „Hot Start“ DNA-Polymerase. Diese Polymerasen können reversibel chemisch wie in der vorliegenden Arbeit, mit Aptameren oder enzymatisch modifiziert sein, sodass sie erst durch den einleitenden Denaturierungschritt bei 95 °C aktiviert werden (Dang und Jayasena 1996, Sharkey et al. 1994). Beim Ansetzen der PCR-Reagenzien besteht daher nicht die Gefahr, dass die Polymerase schon bei niedrigen Temperaturen geringfügig aktiv ist und dadurch unspezifische Amplifikate und Primerdimere bildet. Die unterschiedlichen Sensitivitäten der Real-Time Consensus-PCR für Hefen können zum einen durch die unterschiedliche Effizienz der Primerpaare, aber zum anderen auch durch die unterschiedlichen Effizienzen bei der Synthese der degenerierten Primer entstehen. Bei der normalen Synthese von degenerierten Primern wird nicht jedes Nucleotid mit gleicher Effizienz eingebaut, daher bestehen degenerierte Primer in der Regel nicht zu gleichen Teilen aus allen möglichen Primervarianten, sodass die Primer in sehr unterschiedlichen Konzentrationen vorliegen können. Ein weiterer Punkt, der die PCR-Effizienz herabgesetzt haben könnte, war die notwendige Verringerung der Annealingtemperatur während der Touchdown-PCR auf einen mit 40 °C sehr niedrigen Wert, der für die PCR ungünstig war und normalerweise nur bei der RAPD-PCR eingesetzt wird. Der Einbau von LNA®- („locked nucleic acid“) Nucleotiden in die Sonden, die deren Schelztemperatur erhöhen würden, könnte hier eine Verbesserung darstellen. LNA®-Nucleotide stellen eine neuen, bizyklischen Typ an DNA/RNA-Analoga dar, die eine Methylierung zwischen dem 2´-Sauerstoffatom und dem 4´Kohlenstoffatom der Ribose enthalten und dadurch einem LNA/DNA-Duplex eine höhere Stabilität geben (Koshkin et al. 1998). Die Sonden könnten mit dieser Modifikation kürzer und mit einer höheren Schmelztemperatur konstruiert werden, wodurch die PCR unter stringenteren Bedingungen mit höheren Annealingtemperaturen durchgeführt werden könnte. Das EF-3 Gen kommt einzeln im Genom von S. cerevisiae vor und ist auf dem Chromosom XII lokalisiert (Qin et al. 1990). Im vollständig sequenzierten Genom von S. cerevisiae konnte jedoch eine zu EF-3 homologe Sequenz im Chromosom XIV nachgewiesen werden, die 75 % DNA-Übereinstimmung und 84 % Aminosäure-Übereinstimmung im kodierenden Bereich aufweist. Da dieser Bereich aufgrund fehlender Promotorsequenzen nicht exprimiert werden kann, scheint er nicht essentiell für das vegetative Wachstum zu sein (Sarthy et al. 1998). Für die Sensitivität bedeutet dies, dass maximal zwei Targetsequenzen je haploider Zelle vorliegen. Real-Time PCR Techniken bieten gegenüber konventionellen PCR Methoden nicht nur einen Vorteil in Bezug auf Zeit- und Arbeitsaufwand, sondern auch in Bezug auf die erreichbare Sensitivität. Casey und Dobson (2004) konnten in einem direkten Vergleich zeigen, dass eine Real-Time PCR zum Nachweis des Citratsynthase Gens (cs 1) von C. krusei um zwei 80 4 Diskussion Zehnerpotenzen sensitiver ist als eine konventionelle PCR. Die Sensitivität dieses Systems, das mit SYBR®-Green I zur Detektion der Amplifikate arbeitete, war mit 10 Kopien aufgereinigter Amplifikate oder 120 pg genomischer DNA je Reaktion jedoch nicht im optimalen Bereich. Vergleichbare Systeme für den Nachweis von Hefen über Real-Time PCR beruhen zum größten Teil auf Sequenzen der ribosomalen DNA und deren ITS-Regionen als Target und sind für klinisch relevante Hefen (Candida sp. und Cryptococcus neoformans) entwickelt worden (Bialek et al. 2002, Bu et al. 2005, Hsu et al. 2003, Loeffler et al. 2000, Maaroufi et al. 2003, White et al. 2003). Die Nutzung von rDNA als Target bietet Sensitivitätsvorteile, da je Genom 100 bis 200 Kopien des rDNA Gen-Clusters vorliegen (Kurtzman 1994). 4.3 Anwendbarkeit der Real-Time PCR in Kombination mit der Probenaufarbeitung Ein PCR-basierendes Nachweissystem kann nur Teil eines Qualitätskontrollkonzeptes sein, wenn einige, grundlegende Voraussetzungen erfüllt sind. Hierzu zählen nicht nur die Spezifität und Sensitivität des PCR-Systems, sondern auch eine leichte und sichere Handhabung, die unter anderem eine leichte Interpretation der Ergebnisse beinhaltet, und ein hohes Maß an Robustheit in Bezug auf das eingesetzte Probenmaterial bietet. Das Gesamtkonzept muss außerdem durch eine geeignete Probenvorbehandlung (z. B. Voranreicherung, Membranfiltration) und eine DNA-Extraktionsmethode ergänzt werden. Gegenüber den herkömmlichen Methoden sollten sich möglichst Vorteile zeigen wie z. B. geringerer Zeit- und Arbeitsaufwand. Außerdem sollte die Methode genau und zuverlässig sein, indem das Auftreten von falsch-positiven und falsch-negativen Resultaten möglichst vermieden wird. Mit der optischen Vorrichtung des LightCycler® Gerätes können Fluoreszenzen mit unterschiedlichen Wellenlängen simultan in einer Probe gemessen werden. Dies erlaubt es in jeder Probe eine interne Amplifikationskontrolle (IAK) mitzuführen, deren Amplifikation über eine andere Wellenlänge als bei den positiven Proben und der Positivkontrolle gemessen wird. Für beide Real-Time PCR-Assays wurde eine interne Amplifikationskontrolle durch PCR-Mutagenese entwickelt, die mit der LightCycler®-Red 705 markierten Sonde LMRST1 statt mit den LightCycler®-Red 640 markierten Sonden, die die Wildtypen detektieren, nachgewiesen wurde. Eine IAK sollte idealerweise, um äquivalente Amplifikationseigenschaften aufzuweisen, so wenig Unterschiede zu der eigentlichen Zielsequenz aufweisen wie möglich. Bei den hergestellten internen Amplifikationskontrollen wurde daher nur der Bereich einer Sonde ausgetauscht, die restliche Sequenz entsprach dem Wildtyp. Zu beachten ist jedoch, dass bei der Real-Time Consensus-PCR für Hefen mit vielen, unterschiedlichen Zielsequenzen und den entsprechenden, unterschiedlichen Primern und Sonden die Ähnlichkeit zu der 81 4 Diskussion IAK nicht einheitlich hoch sein konnte. Das Mitführen der internen Amplifikationskontrolle (IAK) bei jeder Reaktion ist für die Anwendung des Systems in der Praxis essentiell, da die PCR durch eine Vielzahl an Substanzen inhibiert werden kann und ohne Kontrolle falschnegative Ergebnisse liefern kann (Rosenstraus et al. 1998). Die IAK wurde bei den beiden Systemen in Form von Plasmid-DNA in einer Konzentration zugegeben, die dem unteren Detektionslimit entspricht, um auch geringe Inhibitionen und Störungen zu detektieren. Ein positives Signal für die Amplifikation der IAK validierte somit negative Ergebnisse bei der Amplifikation des primeren Targets und zeigte, dass auch sehr geringe DNA Mengen in den Proben amplifiziert werden können. Technische Probleme, fehlerhafte Reagenzien oder Fehler beim Handling können durch Mitführen einer Positivkontrolle erkannt werden. Wenn diese Probe negativ ist muss das gesamte Experiment wiederholt werden und mögliche Fehler behoben werden (Burkardt 2000). Für die beiden Systeme wurde je eine Positivkontrolle hergestellt, die sich bei der Real-Time PCR für S. cerevisiae var. diastaticus durch Einfügen einer Punktmutation im Sondenbereich auch von positiven Proben über Schmelzkurvenanalyse unterscheiden ließ, um falschpositive Ergebnisse durch Kontaminationen ausschließen zu können. Für das ConsensusSystem konnte diese zusätzliche Möglichkeit aufgrund der Verwendung von degenerierten Sonden nicht angewendet werden. Falsch-positive Ergebnisse durch Verschleppungen von Amplifikaten in neue Reaktionsansätze können mit der LightCycler® Technologie zum einen vermieden werden, da ein Öffnen der Glaskapillaren für weitere Untersuchungen der Amplifikate nicht notwendig ist, und zum anderen durch den Einsatz eines weiteren Enzyms, der Uracil-N-Glycosylase, gänzlich ausgeschlossen werden (Longo et al. 1990). Die Basis für den Einsatz dieses Enzyms ist eine während der PCR durchgeführte Markierung der generierten Amplifikate, sodass sie sich von der Target-DNA unterscheiden. Dieser Unterschied wird durch die vollständige oder teilweise Substitution der Pyrimidin Base Thymin durch Uracil während der PCR bewerkstelligt. Wenn solche Amplifikate in eine folgende PCR-Reaktion gelangen, werden sie von dem Enzym UNG durch Spaltung der N-glycosidischen Bindung zwischen Uracil und der Desoxyribose abgebaut und können nicht als Vorlage für die PCR dienen. Für die Real-Time PCR für S. c. var. diastaticus wurde der Abbau von zugegebenen Amplifikaten durch die UNG während der einleitenden Inkubation bei 37 °C und die anschließende Inaktivierung des Enzyms durch die folgende Inkubation bei 95 °C erfolgreich getestet. Die Anwendbarkeit und die Robustheit der PCR-Assays wurden mit unterschiedlichen Probenmatrices in Kombination mit der schnellen, 82 mechanisch/thermischen DNA- 4 Diskussion Extraktionsmethode getestet. Diese Testung war wichtig, da ein Nachteil von PCR-Methoden in der Inhibition der DNA-Polymerase durch Substanzen liegen kann, die in der Probe vorhanden sind (Rossen et al. 1992). Der Real-Time PCR-Assay zum Nachweis von S. cerevisiae var. diastaticus stellte sich dabei als ein sehr robustes System dar, da sich nur eine Probenmatrix („Laugetank“) von 66 untersuchten Proben als gänzlich ungeeignet herausstellte und auch nach Verdünnung die Amplifikation der IAK inhibierte. Die Probenmatrix „Laugetank“ inhibiert sehr wahrscheinlich die DNA-Polymerase durch die Erhöhung des pHWertes im Reaktionsansatz. Das in den PCR-Ansätzen als Blocking-Reagenz enthaltene BSA und das während der DNA-Extraktion verwendete Chelex® 100 sind bekannt für ihre positive Eigenschaft, PCRInhibitionen zu vermindern, und könnten zu der hohen Stabilität des Systems beigetragen haben (Al-Soud und Radström 2000, de Lamballerie et al. 1992, Kreader 1996, Mättö et al. 1998, Walsh et al. 1991). Auch eine sehr hohe Hintergrundkonzentration von 108 Zellen/ml S. cerevisiae, die allein aufgrund der großen DNA-Menge oder den auch bei S. cerevisiae vorhandenen Zielsequenzen von Primern und Sonden zur Inhibition der IAK hätten führen können, bereitete keine Probleme. Die Stabilität des PCR-Systems könnte möglicherweise den gänzlichen Verzicht auf eine DNA-Extraktion für einige Proben ermöglichen. Ibeas et al. (1996) konnten z. B. auf eine DNA-Extraktion verzichten, da der Denaturierungsschritt zu Beginn der PCR bei 95 °C ausreichte, um die Zellen zu lysieren und die DNA freizusetzen. Die Real-Time Consensus- PCR für Hefen ist ebenfalls als ein robustes System anzusehen, jedoch führten trübstoffhaltige Säfte und besonders Rotwein zu einer verminderten Sensitivität des Systems, sodass teilweise keine Detektion bei Zellzahlen von weniger als 105 Zellen/ml möglich war. Die Anwendung einer Flüssiganreicherung könnte in diesem Zusammenhang zur Erhöhung der Zellzahlen führen und gleichzeitig auch zur Verdünnung der inhibierenden Substanzen dienen (Hofstra 1994, Swaminathan und Feng 1994). Besonders Rotwein ist bekannt für die inhibierende Wirkung einiger Inhaltsstoffe wie z. B. Polysaccharide, Tannin und Polyphenole (Wilson 1997). Die Inhaltsstoffe des Rotweins könnten möglicherweise als organische Liganden Komplexe mit den Magnesiumionen, die essentiell für die Aktivität der DNA-Polymerase sind, bilden und die PCR dadurch inhibieren. Vergleichbare Verschlechterungen der Sensitivität durch die Probenmatrix Wein konnten bei PCRSystemen beobachtet werden, die für Dekkera/Brettanomyces sp. entwickelt wurden. Ibeas et al. (1996) konnten mit einer konventionellen Nested-PCR ein Detektionslimit von 10 Zellen/Reaktion erreichen, wenn steriles Wasser als Probenmatrix verwendet wurde und die Proben direkt ohne Extraktion in die PCR eingesetzt wurden. Sherrywein inhibierte dagegen die PCR, sodass nur 104 Zellen/ml nachweisbar waren. Eine Zentrifugation der Proben 83 4 Diskussion und die anschließende Aufnahme der sedimentierten Zellen in sterilem Wasser eliminierte die Inhibition. Eine Nested-PCR ist jedoch für die Anwendung in der Praxis nicht nur eine zu umständliche und arbeitsaufwendige Methode, sondern auch aufgrund ihrer hohen Anfälligkeit für falsch-positive Ergebnisse durch Kontaminationen ungeeignet (Burkardt 2000). Jedes erneute Öffnen von Reaktionsgefäßen oder Pipettieren von hohen Amplifikatmengen stellt bei der sehr empfindlichen PCR-Diagnostik ein zu vermeidendes Kontaminationsrisiko dar. Von Cocolin et al. 2004 wurde ebenfalls ein PCR-System zum Nachweis von Dekkera/Brettanomyces bruxellensis und Dekkera/Brettanomyces anomalus entwickelt, das die D1/D2 Domäne der 26S rDNA als Target nutzte. Das System hatte trotz der Verwendung eines „multicopy“ Gens ein hohes Detektionslimit von 104 bis 105 Zellen/ml, wenn DNA oder RNA direkt aus Wein isoliert wurde. Bei einer Konzentration von 105 KBE/ml oder höher macht sich die für Brettanomyces sp. typische und unerwünschte Geschmacksveränderung im Wein bereits bemerkbar (Chatonnet et al. 1992). Quantitative Real-Time PCR-Systeme für Dekkera/Brettanomyces bruxellensis konnten von Delaherche et al. (2004) und Phister und Mills (2003) mit SYBR®-Green I entwickelt werden. Bei Delaherche et al. (2004) wurde ein Detektionslimit von 104 KBE/ml in Wein ermittelt, das gut mit den Ergebnissen der konventionellen Methoden korrelierte. Phister und Mills (2003) konnten dagegen ein für die schwierige Probenmatrix Wein und die Detektion mit SYBR®Green I sehr sensitives System entwickeln, das nach einer 1:10-Verdünnung der Proben ein Detektionslimit von 10 KBE/ml hatte. Diese beiden Einzelnachweise, die nur ein Primerpaar enthielten, sind jedoch nicht direkt mit der entwickelten Real-Time PCR für Hefen zu vergleichen. Die für diese beiden PCR-Systeme verwendeten, kommerziellen DNA- Extraktionsmethoden entsprechen eher der erweiterten, mechanisch/thermischen Methode, mit der wie bei Delaherche et al. (2004) 104 Zellen/ml S. cerevisiae in Rotwein detektiert wurden. Die hohe Sensitivität des Nachweises von Phister und Mills (2003) ist sicher auch auf die Verwendung eines „multi-copy“ Gens (26 S rRNA Gen) zurückzuführen. Die Erweiterung der mechanisch/thermischen Extraktionsmethode um einen enzymatischen Schritt mit Proteinase K und einen Aufreinigungsschritt mit Säulen führte zu einer Verbesserung der Sensitivität. Magnetische Separationstechniken, die zur Trennung von Nucleinsäuren von der Probenmatrix angewendet werden, wie z. B. das MagNA Pure System, das bei einer der Brauereien mit dem S. c. var. diastaticus System erfolgreich getestet wurde, könnten ebenfalls zur Minderung von Inhibitionen bei problematischen Probenmatrices angewendet werden (Loeffler et al. 2002, Safarík et al. 1995). Die Real-Time Consensus-PCR für Hefen unterscheidet sich außerdem von dem Einzelnachweis für S. cerevisiae var. diastaticus in der auf 750 ng/µl verminderten BSA-Konzentration. Diese Reduktion war durch den Ein- 84 4 Diskussion satz einer höheren MgCl2-Konzentration (4,0 mM) bei diesem System notwendig. BSA wird während der PCR durch die wiederholten 95 °C Schritte denaturiert und bildet dann besonders in Gegenwart von bivalenten Ionen wie Mg2+ unlösliche Niederschläge (Teo et al. 2002). Die von Teo et al. (2002) als thermostabile Alternative zu BSA vorgeschlagene Verwendung von RNase A wurde getestet und die Anwendung war für dieses System möglich, jedoch konnten die inhibitionsmindernden Eigenschaften des BSA durch dieses Enzym bei mechanisch/thermisch aufgearbeiteten Proben nicht erreicht werden. (Die Daten hierzu wurden in dieser Arbeit nicht vorgestellt.) Neben Inhibitionen ist die Effizienz des Zellaufschlusses durch die mechanisch/thermischen DNA-Extraktionsmethoden ein weiterer wichtiger Aspekt, der die Sensitivität der Nachweise beeinflusst. Der mechanische Zellaufschluss von Hefen und Schimmelpilzen unter Einbeziehung von Glaskügelchen und einem geeignetem Gerät wurde oft als effiziente, schnelle und günstige Methode beschrieben (Haugland et al. 1999, Müller et al. 1998, van Burik et al. 1998). Eine ähnlich aufgebaute schnelle Extraktionsmethode wie in der vorliegenden Arbeit, die aus der Kombination eines thermischen Schritts mit einem Lysis-Puffer und einem mechanischen Schritt mit Glaskügelchen bestand, wurde von Kuske et al. (1998) zur Extraktion von DNA aus sehr unterschiedlichen Zelltypen (vegetative Bakterien, bakterielle Endosporen und Konidien) und Bodenproben erfolgreich verwendet. In der vorliegenden Arbeit wurde eine 5-%ige Chelex 100 Lösung als Lysis-Puffer verwendet, die durch die Chelatierung von polyvalenten Metallionen und ihre hohe Alkalinität in Kombination mit hohen Temperaturen zur Destabilisierung und Zerstörung der Zellemembranen führt und vermutlich gleichzeitig eine stabilisierende Wirkung auf die DNA hat (de Lamballerie et al. 1992, Walsh et al. 1991). Die Ergebnisse der Sensitivitätstestung des Einzelnachweises für S. c. var. diastaticus zeigten, dass die mechanisch/thermische DNA-Extraktionsmethode sehr effizient war. Eine Ausgangskontamination zwischen 102 und 103 Zellen/ml war nachweisbar, was theoretisch 2,5 bis 25 GÄ pro PCR-Reaktion entspricht. Mit der Real-Time Consensus-PCR für Hefen konnten in Kombination mit der mechanisch/thermischen DNA Extraktionsmethode in trübstofffreien Getränken zwischen 103 und 104 Zellen/ml nachgewiesen werden. Bei der Handhabbarkeit der DNA-Extraktionsmethode wurde außerdem auf die Vermeidung von gesundheitsgefährdenden Stoffen wie Chloroform oder Phenol geachtet. Bei Kontaminationsleveln, die unterhalb des ermittelten Detektionslimits lagen, zeigte sich ein Nachteil von PCR-basierten Methoden, der von van der Vossen und Hofstra (1996) angesprochen wurde und in dem geringen einsetzbaren Probenvolumen von maximal 10 µl bei einem Reaktionsvolumen von 20 µl liegt. Die Sensitivität ist daher auch bei dem sehr empfindlichen PCR-Assay für S. c. var. diastaticus mit einem optimalen Probenvolumen von 5 µl 85 4 Diskussion durch die Probenaufarbeitung limitiert. Die Sensitivität der Nachweise könnte bei filtrierbaren Proben über eine geeignete Membranfiltration erhöht werden, die jedoch auch einen wesentlich höheren Arbeitsaufwand darstellt. Größere Volumina könnten auch nach Zentrifugation und anschließender Aufnahme der sedimentierten Zellen im Lysispuffer aufkonzentriert werden. Anreicherungen stellen wie mit dem Gesamtnachweis für Hefen gezeigt ebenfalls eine Möglichkeit dar, um auch Spurenkontaminationen von weinigen Zellen/ml zu erfassen. Ein Vorteil der Flüssiganreicherung liegt in der Ermittlung signifikant höherer Zellzahlen als bei der direkten Anwendung von Oberflächen- oder Plattenguss-Verfahren, da gestresste Zellen besser wiederbelebt werden (Deák, 1991). Die Kombination aus unspezifischer Flüssiganreicherung mit YM-Medium und anschließender Consensus-PCR stellt einen unselektiven Nachweis für Hefen dar, der Aussagen über die An- und Abwesenheit von Hefen liefert. Ein solcher Nachweis kann z. B. in Brauereien als Indikator für die allgemeine Betriebshygiene und als Endkontrolle dienen. Ein unselektives Medium wurde hierbei zu Gunsten einer hohen Wachstumsgeschwindigkeit ausgewählt, da jedes selektive Reagenz oder jede selektive Bedingung auch Einfluss auf die nachzuweisenden Organismen hat. Die Inhibition einer Begleitflora wie z. B. der Kulturhefe und das Wachstum von Fremdhefen wird unter selektiven Bedingungen von den physiologischen Voraussetzungen der Hefen, der Zellkonzentration und den Inkubationsbedingungen beeinflusst (Fernández et al. 1989). Makdesi und Beuchat (1996) zeigten, dass gegen Benzoat resistente Zygosaccharomyces bailii Stämme nach einem Hitzestress mit pH-neutralem YM-Agar besser als mit saurem YM-Agar (pH 3,8) nachzuweisen waren. Diese Ergebnisse sind besonders interessant im Bereich der nicht karbonathaltigen Getränke, die heiß abgefüllt oder vor dem Abfüllen pasteurisiert werden. Ein weiterer positiver Aspekt des unselektiven YM-Mediums ist die mit 10 g/l niedrige Glucosekonzentration, da hitzegestresste Hefezellen eine erhöhte Sensitivität gegenüber hohen Zuckerkonzentrationen aufweisen können (Golden und Beuchat 1990, Stecchini und Beuchat 1985). Das YM-Medium, das nach den Bestandteilen im Bereich der Brauereien auch MYGP-Medium genannt wird, wurde außerdem ausgewählt, da es als Grundmedium für einige selektive Medien zum Nachweis von Fremdhefen in Brauereien angewandt wird (Jespersen und Jakobsen 1996). Bei einem Vergleichstest unterschiedlicher Medien für den Nachweis von Fremdhefen von van der Aa Kühle und Jespersen (1998) konnten die besten Ergebnisse mit YM-Agar mit dem Zusatz von CuSO4 erzielt werden. Die Anwendung des MYGP-Mediums mit 200 ppm CuSO4 wird außerdem von der American Society of Brewing Chemists empfohlen (Anonymus 1992). 86 4 Diskussion Wie in Brauereien kann es auch in anderen Bereichen der Getränkeindustrie sinnvoll sein nur die relevanten, obligaten Verderbniserreger (z. B. Zygosaccharomyces sp., Dekkera sp. oder Saccharomyces sp.) oder einzelne Gruppen von Hefen (z. B. gärfähige Hefen) nachzuweisen. Eine solche Selektion kann über die Bedingungen der Flüssiganreicherung und die dabei verwendeten Medien erfolgen. Das SSL-Verfahren verbessert z. B. den Nachweis von osmophilen und gärfähigen Hefen in Rohstoffen und Konzentraten, indem zunächst eine Flüssiganreicherung mit SSL-Bouillon für 36 bis 48 Stunden vorgenommen wird, die zur Verkürzung der Lag-Phase führt (Back 1999). Danach werden zwischen 2 und 5 ml der Flüssigkultur im Plattengussverfahren mit Orangenfruchtsaftagar ausgewertet. Das gesamte Verfahren dauert 4 bis 5 Tage und kann sehr geringe Keimzahlen nachweisen. Eine Verkürzung der Detektionszeit um 2 bis 3 Tage, die zur Kultivierung im Orangenfruchtsaftagar nötig sind, könnte durch die Verwendung der wesentlich schnelleren PCR erreicht werden. Quantitative Aussagen über die Grundbelastung können nach einer Flüssiganreicherung nicht gemacht werden. Da es sich hierbei um einen Spurennachweis handelt, ist jedoch die Kenntnis der genauen Keimzahl zweitrangig. Der Nachweis solcher Spurenkontaminationen kann je nach Probe und beteiligtem Mikroorganismus sehr relevant sein. In fruchtfleischhaltigen Säften kann z. B. schon eine Hefezelle pro 10 ml problematisch sein, bei klaren Säften wird dagegen teilweise eine Hefezelle/ml toleriert (Weidenbörner 1998). Für einige Organismen wie z. B. Zygosaccharomyces sp. muss das Qualitätskontrollsystem so ausgelegt werden, dass im Endprodukt keine Zelle vorhanden ist, da auch ein sehr geringer Kontaminationslevel zu Problemen führt (van der Vossen und Hofstra 1996). Die entwickelte Real-Time Consensus-PCR für Hefen in Kombination mit einer Flüssiganreicherung könnte für solche Proben eine Aussage über die An- oder Abwesenheit dieser obligaten Schädlinge in 2 bis 3 Tagen liefern. Die Experimente zur Ermittlung der Detektionszeit zeigten, dass die Anreicherungszeit für langsam wachsende Hefen wie z. B. Brettanomyces sp. oder Schizosaccharomyces pombe entsprechend verlängert werden muss. Falls diese Arten relevant für das Untersuchungsmaterial sind und deren Auftreten zu erwarten ist, muss dies entsprechend berücksichtigt werden. Außerdem sollte auch für geschädigte Zellen, die durch Methoden der Produktstabilisierung nicht vollständig abgetötet wurden, eine verlängerte Anreicherungszeit berücksichtigt werden. Versuche, bei denen vor einer Anreicherung mit Hefezellen dotiert wurde, wurden auch von García et al. (2004) durchgeführt. Die konventionelle PCR mit Nachweis der Amplifikate über Gelelektrophorese hatte ein Detektionslimit für K. marxianus in Milch von 105 KBE/ml. Dieses Detektionslimit konnte bei einer initialen Kontamination von 10 KBE/ml nach 16 Stunden Anreicherung ohne zusätzliches Nährmedium erreicht werden. 87 4 Diskussion Der Nachweis von Hefen über eine Flüssiganreicherung und anschließende Detektion über PCR ist vergleichbar mit der direkten oder indirekten Messung der Leitfähigkeit. Der Detektionsgrenzwert liegt bei der indirekten Messung der Leitfähigkeit zwischen 104 und 105 Zellen/ml (Deák 1995). Wie bei der Messung der Leitfähigkeit könnte auch die Real-Time Consensus-PCR für Hefen in Kombination mit einer Flüssiganreicherung über die Detektionszeit, die von Beginn der Inkubation verstreicht bis eine messbare Veränderung auftritt, gegen eine konventionelle Zellzahlbestimmung kalibriert werden, um Aussagen über die Ausgangspopulation machen zu können. Größere Ausgangspopulationen würden dementsprechend kürzere Detektionszeiten ergeben, die jedoch nicht unabhängig von den unterschiedlichen Wachstumsgeschwindigkeiten der Hefearten sind. Im Gegensatz zu dem Gesamtnachweis für Hefen konnten bei dem Einzelnachweis für S. c. var. diastaticus die gesamten Vorteile der Real-Time PCR ausgenutzt werden, da das System zur sensitiven Detektion und spezifischen Identifikation genutzt werden kann. Ein Vorteil der Real-Time PCR gegenüber anderen PCR-basierten, molekularbiologischen Methoden liegt in der Bündelung der PCR und der Amplifikatdetektion in einem Schritt und der einfachen und objektiven Auswertung der Ergebnisse z. B. mit der LightCycler® Software 4. Besonders wenn sehr geringe Amplifikatmengen detektiert werden müssen, bietet ein numerischer Wert oder eine klare positive oder negative Aussage weniger Interpretationsmöglichkeiten als eine schwache Bande in einem Agarosegel. Damit wird diese Technik nicht nur zu einer schnellen, sondern auch zu einer leicht handhabbaren Methode, wie durch die Testung des S. c. var. diastaticus Nachweises bei vier Brauereien gezeigt wurde. Eine RFLP-PCR von Yamagishi et al. (1999), mit der S. c. var. diastaticus von Brauhefen unterschieden wurde, bestand im Gegensatz dazu aus der PCR mit 5 S rDNA und 26 S rDNA spezifischen Primern, einem anschließendem Restriktionsverdau und einer abschließenden Auftrennung im Agarosegel. Neben dem Nachteil des höheren Arbeitsaufwandes besteht ein weiterer Unterschied dahingehend, dass diese Methode nur zu Identifizierung von Reinkulturen verwendet werden kann. Die gleichen Nachteile und Einschränkungen gelten für einen RAPDPCR-Assay von Tompkins et al. (1996), der ebenfalls zur Unterscheidung von S. cerevisiae var. diastaticus von Brauhefen geeignet war und auch zur Identifizierung von bierschädlichen Bakterien diente. Gegenüber immunologischen Tests besitzt ein Nachweissystem über Nucleinsäuren den Vorteil, dass nicht erst eine phänotypische Expression der Zielantigene stattfinden muss. Sie sind demnach auch weniger abhängig von Wachstumsbedingungen und äußeren Einflüssen. 88 4 Diskussion Der wichtigste Maßstab für die Anwendbarkeit einer auf der Real-Time PCR-basierten Methode besteht jedoch im Vergleich mit den klassischen, mikrobiologischen Methoden. Die Detektion von Fremdhefen wie S. c. var. diastaticus bereitet besonders durch ihre biochemische und physiologische Ähnlichkeit zu den Brauhefen Probleme (Jespersen und Jakobsen 1996), daher ist der Real-Time PCR-Nachweis über das entscheidende, genetische Identifikationsmerkmal von S. c. var. cerevisiae für die Anwendung sehr sinnvoll. Ein weiterer Vorteil des Real-Time LightCycler® Systems zum Nachweis von S. cerevisiae var. diastaticus liegt in der Möglichkeit, geringe Zellzahlen bei einer großen Hintergrundpopulation an S. cerevisiae nachzuweisen. Mit dem System können zwischen 102 und 103 Zellen/ml S. c. var. diastaticus bei einem Hintergrund von 108 Zellen/ml S. cerevisiae identifiziert werden, obwohl die Zielsequenzen in anderer Konstellation auch in der Brauhefe S. cerevisiae vorliegen. Diese Sensitivität entspricht der von Detektionssystemen im Bereich der Brauereien geforderten Nachweisempfindlichkeit von einem verderbniserregenden Organismus in 106 Kulturhefen (Jespersen und Jakobsen 1996). Das System ist demnach geeignet, um S. c. var. diastaticus in schwierigen Proben wie der Anstellhefe und anderen hefehaltigen Proben aus dem gesamten Produktionsbereich nachzuweisen. Der klassische Nachweis von S. c. var. diastaticus und anderen Saccharomyces Fremdhefen kann über Kultivierung mit einer Reihe von unterschiedlichen Medien erfolgen, wobei die Auswahl von der verwendeten Kulturhefe abhängt (Jespersen und Jakobsen 1996). Powell und Smart (2003) verglichen drei unterschiedliche Medien (MYGP mit CuSO4, Lysin und CLEN) mit zwei konventionellen PCR-Methoden (spezifische PCR und RAPD-PCR). Die Ergebnisse zeigten, dass eine Kombination der drei Medien für den Nachweis von 103 Zellen/ml Fremdhefen in Kulturhefen geeignet war und die PCR-basierten Methoden dagegen zur Identifizierung von Hefen geeignet waren. Bei der Verwendung von selektiven Medien besteht jedoch immer die Gefahr, dass auch mögliche Fremdhefen, die sich in einem physiologisch schlechten Zustand bedingt durch z. B. Hitzebehandlung befinden, ebenfalls inhibiert werden und somit unentdeckt bleiben (Jespersen und Jakobsen 1996). Kultivierungsmethoden haben den Nachteil, dass aktive Prozesskontrollen und zeitnahe Qualitätskontrollen der Produkte schwierig sind, da Tage oder sogar Wochen vergehen bis mögliche Kontaminationen erkannt werden. Die Anwendung einer schnellen Methode wie der RealTime PCR zum Nachweis von S. c. var. diastaticus kann hier dazu beitragen, dass Endprodukte schneller ausgeliefert werden können, da die Ergebnisse der Qualitätskontrolle schnell vorliegen. Je schneller eine Methode zum Nachweis von verderbniserregenden Mikroorganismen ist, desto weniger Lagerzeit ist notwendig und somit reduziert sich auch die benötigte Lagerfläche. Die Gesamtzeit, die für die DNA-Extraktion von 30 Proben mit der mecha- 89 4 Diskussion nisch/thermischen Methode und die Durchführung der Real-Time PCR benötigt wird, beträgt für den Einzelnachweis von S. c. var. diastaticus nur 2,5 Stunden. Probleme bei der Anwendung von PCR-Methoden können durch falsch-positive Ergebnisse entstehen, die durch Amplifikation von freier DNA oder DNA von toten Mikroorganismen, deren Zellmembranen noch intakt sind, verursacht werden (van der Vossen und Hofstra 1996). Im Bereich der Getränkeindustrie ist nur der Nachweis von lebenden und damit potentiell schädlichen Mikroorganismen relevant. Für pathogene Bakterien wurde von einigen Autoren gezeigt, dass die DNA von abgetöteten Zellen noch viele Tage als Vorlage für die PCR dienen konnte (Allmann et al. 1995, Josephson et al. 1993, Masters et al. 1994). Bleve et al. (2003) konnte für S. cerevisiae zeigen, dass nach einer Abtötung der Zellen bei 60 °C für 20 min die DNA auch 24 Stunden später nach einer Inkubation bei 25 °C noch amplifiziert werden konnte. In der vorliegenden Arbeit wurde keine undotierte Probe mit oder ohne Anreicherung falsch-positiv getestet. Die bei dem Consensus-System angewandte Voranreicherung könnte bei Untersuchungen von z. B. Säften, bei denen durchaus auch „non-viable“ Targetorganismen zu erwarten wären, die zwar nicht lebensfähig sind, deren DNA aber intakt ist, zur Differenzierung zwischen lebenden und toten Zellen genutzt werden. Rückstellproben, die kühl gelagert wurden, müssten dann bei positiven Ergebnissen ebenfalls getestet werden, um das Ergebnis aufgrund von lebensfähigen Hefen als positiv zu verifizieren. Der Nachweis von Organismen über mRNA als Target kann unter der Voraussetzung, dass die ausgewählte RNA nach dem Tod der Zelle schnell abgebaut wird und eine essentielle Funktion für den Organismus hat, zur Differenzierung zwischen lebenden und toten Zellen eingesetzt werden. Die Anwendbarkeit dieser Methode für Hefen in Lebensmitteln wurde von einigen Autoren für unterschiedliche Targets wie z. B. EF-1α und Actin mRNA gezeigt (Bleve et al. 2003, Vaitilingom et al. 1998). Die Komplexität der Real-Time Consensus-PCR für Hefen verhinderte deren Umstellung zu einer RT-PCR, obwohl Versuche mit einem reduzierten System die Nutzbarkeit der mRNA des EF-3 Proteins anzeigten. Die Daten zu diesem Experiment werden im Anhang im Kapitel 6.3 präsentiert. Für die Anwendbarkeit in der Praxis stellen sich jedoch Fragen, die die Komplexität und damit die Handhabbarkeit der Methode betreffen. Ein zusätzlicher DNase-Verdau mit entsprechenden Kontrollen und möglicherweise einer getrennten Reversen Transkription könnten zu einem erhöhten Arbeitsaufwand führen. Die Inaktivierung der DNase vor der RT-PCR und die Vermeidung von Ribonucleasen sind ebenfalls kritische Punkte, die eine Anwendung als Routineuntersuchung erschweren. Eine Behandlung von Proben, die für eine PCR verwendet werden sollen, mit DNase vor einer DNA-Extraktion könnte auch zur Eliminierung von freier DNA und DNA von toten Zellen verwendet werden (Lyon 2001, Nogva et al. 2000). 90 4 Diskussion Bleve et al. (2003) stellten außerdem nach der Hitzeinaktivierung von S. cerevisiae Zellen ausgehend von einer hohen Zellzahl von 108 Zellen fest, dass die mRNA auch noch nach 24 Stunden Inkubation über RT-PCR nachzuweisen war, da ein Teil der Zellen in ein VBNCStadium übergegangen war. Hefen können wie Bakterien ein so genanntes VBNC-Stadium (viable but nonculturable state) einnehmen, in dem die Zellen zwar metabolisch aktiv sind, aber keine Zellteilung zum Wachstum in flüssigem oder festem Nährmedium durchführen (Oliver 1993). Ausgelöst wird der Übergang in dieses Stadium durch Stressfaktoren wie z. B. Nährstoffmangel oder ungünstige Temperaturen, die neben der Veränderung der Zellmembranen zu einer Verkleinerung der Zellgröße führen (McDougald et al. 1998, Oliver et al. 1995). Divol und LonvaudFunel (2005) konnten den Übergang in ein VBNC-Stadium bei S. cerevisiae, C. stellata und Z. bailii in durch Botrytis cinerea beeinflusstem Wein nach der Zugabe von SO2 beobachten, während dessen keine Kultivierung auf festem Nährmedium möglich war. Nach Verdünnung des Weins und der damit verbundenen Herabsetzung der Stressfaktoren SO2-Konzentration und osmotischer Druck gelangten die Hefen wieder in ein kultivierbares Stadium. Die Detektion von Organismen, die sich in dem VBNC-Stadium befinden, kann besonders dann sinnvoll sein, wenn ein Produkt wie z. B. Wein zur Reifung lange gelagert wird. Das Phänomen einer erneuten Fermentation von in Fässern reifendem oder abgefülltem Wein, in dem zum Zeitpunkt der Einlagerung oder Abfüllung über Kultivierung keine Mikroorganismen nachzuweisen waren, könnte durch z. B Brettanomyces sp. im VBNC-Stadium verursacht werden. Nur direkte Techniken, die keine Kultivierung benötigen, können zur Detektion von Hefen in diesem Stadium angewandt werden. Neben Methoden wie der Durchflusszytometrie und der DEF-Technik (direct epifluorescent filter technique) bietet auch die Real-Time PCR die Möglichkeit, diese Organismen nachzuweisen (Divol und Lonvaud-Funel 2005, Lowder et al. 2000). 91 4 Diskussion 4.4 Ausblick Die entwickelten Real-Time PCR-Assays sind in ihrer jetzigen Form zusammen mit den Probenaufarbeitungsmethoden für den Einsatz in der Getränkeindustrie geeignet. Bei beiden Systemen besteht das Potential, sie durch Einbeziehung weiterer Targetorganismen zu erweitern. Der Einzelnachweis für S. cerevisiae var. diastaticus könnte durch den gleichzeitigen Nachweis von weiteren obligat bierschädlichen Hefen wie z. B. S. bayanus, S. pastorianus und D. bruxellensis ergänzt werden. Der Gesamtnachweis für Hefen könnte nach Generierung von weiteren Sequenzen zu einem Nachweis für Hefen und Schimmelpilze ausgeweitet werden. Der Erweiterung der Komplexität von Real-Time PCR-Assays sind jedoch durch die Anzahl der einsetzbaren Fluoreszenzfarbstoffe Grenzen gesetzt, wenn eine größere Anzahl unterschiedlicher Arten oder Stämme gleichzeitig detektiert und identifiziert werden soll. Die Anwendung der Multiplex-PCR mit anschließender Detektion über Microarrays, die ein hohes Potential zur Differenzierung bieten, wird in Zukunft sicher bei geeigneter Automatisierung für solche Fragestellungen zum Einsatz kommen, um ausgehend von einem einzelnen Assay sehr viele unterschiedliche Targets zu identifizieren. Die Menge an produzierten Daten wird durch die Anwendung solcher immer umfangreicheren Identifizierungsmethoden ansteigen und die Ansprüche an die Auswertungssysteme erhöhen. Jedoch wird auf Einzelnachweise im Real-Time PCR Maßstab für sehr relevante Mikroorganismen, deren An- bzw. Abwesenheit in einer Probe getestet werden muss, nicht verzichtet werden, da die Sensitivität von Multiplex-PCR-Systemen durch Konkurrenzreaktionen herabgesetzt wird. Mit zunehmender Vollautomatisierung im Bereich der Probenaufarbeitung und der anschließenden Detektion wird auch die Möglichkeit der Online-Datenübertragung zwischen unterschiedlichen Produktionsstandorten und der Datenbündelung zur zentralen Auswertung möglich. 92 5 Literatur 5 Literatur Abd-Elsalam, K. A. 2003. Bioinformatic tools and guideline for PCR primer design. African J. Biotech. 2: 91-95. Allmann, M., C. Hofelein, E. Koppel, J. Luthy, R. Meyer, C. Niederhauser, B. Wegmuller, and U. Candrian. 1995. Polymerase chain reaction (PCR) for detection of pathogenic microorganisms in bacteriological monitoring of dairy products. Res. Microbiol. 146: 85-97. Al-Soud, W. A., and P. Radström. 2000. Effects of amplification facilitators on diagnostic PCR in the presence of blood, feces, and meat. J. Clin. Microbiol. 38: 4463-4470. Andrews, J., and R. B. Gilliland. 1952. Super attenuation of beer: a study of three organisms capable of causing abnormal attenuation. J. Inst. Brew. 58: 189-196. Andrews, S., H. De Graaf, H. Stamatin. 1997. Optimization of methodology for enumeration of xerophilic yeasts from foods. Int. J. Food Microbiol. 35: 109-116. Anonymus. 1987. ISO 7954. Microbiology — General guidance for enumeration of yeasts and moulds — Colony count technique at 25 °C. ISO: International Organisation for Standardisation. Anonymus. 1992. Copper media for wild yeast detection. J. Am. Soc. Brew. Chem. 50: 153157. Atkins, S. D., and I. M. Clark. 2004. Fungal molecular diagnostics: a mini review. J. Appl. Genet. 45: 3-15. Back, W. 1987. Nachweis und Identifizierung von Fremdhefen in der Brauerei. Brauwelt 127: 735-737. Back, W. 1994. Farbatlas und Handbuch der Getränkebiologie. Band 1. Fachverlag Hans Carl. Nürnberg. Back, W. 1999. Farbatlas und Handbuch der Getränkebiologie. Band 2. Fachverlag Hans Carl. Nürnberg. Back, W., and S. Anthes. 1979. Taxonomische Untersuchungen an limonadenschädlichen Hefen. Brauwissenschaft. 3236: 145-154. Baleiras Couto, M. M., J. T. W. E. Vogels, H. Hofstra, J. H. J. Huis in `t Veld and J. M. B. M. van der Vossen. 1995. Random amplified polymorphic DNA and restriction enzyme analysis of PCR amplified rDNA in taxonomy: two identification techniques for food-borne yeasts. J. Appl. Bacteriol. 79: 525-535. Baleiras Couto, M. M., B. Eijsma, H. Hofstra, J. H. J. Huis in `t Veld and J. M. B. M. van der Vossen. 1996a. Evaluation of molecular typing techniques to assign genetic diversity among strains of Saccharomyces cerevisiae. Appl. Environ. Microbiol. 62: 41-46. Baleiras Couto, M. M., B. J. Hartog, J. H. J. Huis in `t Veld, H. Hofstra and J. M. B. M. van der Vossen. 1996b. Identification of spoilage yeast in a food production chain by microsatellite PCR fingerprinting. Food Microbiol. 13: 59-67. 93 5 Literatur Banks, J. G., and R. G. Board. 1987. Some factors influencing the recovery of yeasts and moulds from chilled foods. Int. J. Food Microbiol. 4: 197-206. Barnett, J. A., R. W. Payne, and D. Yarrow. 1983. Yeasts: characteristics and identification. Cambridge University Press. Cambridge. Belfield, G. P., and M. F. Tuite. 1993. Translation elongation factor 3: a fungus-specific translation factor? Mol. Microbiol. 9: 411-418. Belfield, G. P., N. J. Ross-Smith, and M. F. Tuite. 1995. Translation elongation factor-3 (EF-3): an evolving eukaryotic ribosomal protein? J. Mol. Evol. 41: 376-387. Belloch, C., E. Barrio, F. Uruburu, M. D. García, and A. Querol. 1997. Characterisation of four species of the genus Kluyveromyces by mitochondrial DNA restriction analysis. Syst. Appl. Microbiol. 20: 397-408. Betts, R. P., P. Bankes, and J. G. Banks. 1989. Rapid enumeration of viable microorganisms by staining and direct microscopy. Lett. Appl. Microbiol. 9: 199-202. Beuchat, L. R. 1979. Comparison of acidified and antibiotic supplemented potato dextrose agar from three manufacturers for its capacity to recover fungi from foods. J. Food Prot. 42: 427-428. Beuchat, L. R., and A. D. Hocking. 1990. Some considerations when analysing foods for the presence of xerophilic fungi. J. Food Prot. 53: 984-989. Beuchat, L. R., B. V. Nail, R. E. Brackett, and T. L. Fox. 1990. Evaluation of a culture film (Petrifilm™YM) method for enumeration yeasts and molds in selected dairy and high-acid foods. J. Food Prot. 53: 869-874. Beuchat, L. R., B. V. Nail, R. E. Brackett, and T. L. Fox. 1991. Comparison of Petrifilm™ yeast and mold culture film method to conventional methods for enumeration yeasts and molds in foods. J. Food Prot. 54: 443-447. Beuchat, L. R., Y. Jung, T. Deák, T. Keffler, D. A. Golden, J. M. Peinado, P. Gonzalo, M. I. De Siloniz, and M. J. Valderrama. 1998. An interlaboratory study on the suitability of diluents and recovery media for enumeration of Zygosaccharomyces rouxii in high sugar foods. J. Food Mycol. 1: 117-130. Bialek, R., M. Weiss, K. Bekure-Nemariam, L. K. Najvar, M. B. Alberdi, J. R. Graybill, and U. Reischl. 2002. Detection of Cryptococcus neoformans DNA in tissue samples by nested and real-time PCR assays. Clin. Diag. Lab. Immun. 9: 461-469. Bignell, G. R., and I. H. Evans. 1990. Localisation of glucoamylase genes of Saccharomyces cerevisiae by pulsed field gel electrophoresis. Antonie van Leeuwenhoek. 58: 49-55. Blakely, G., J. Hekman, K. Chakraburtty, and P. R. Williamson. 2001. Evolutionary divergence of an elongation factor 3 from Cryptococcus neoformans. J. Bacteriol. 183: 22412248. 94 5 Literatur Bleve, G., L. Rizzotti, F. Dellaglio, and S. Torriani. 2003. Development of reverse transcription (RT)-PCR and real-time RT-PCR assays for rapid detection and quantification of viable yeasts and molds contaminating yoghurts and pasteurized food products. Appl. Environ. Microbiol. 69: 4116-4122. Boekhout, T., and H. J. Phaff. 2003. Yeast biodiversity. 1-38. In: Yeasts in food: beneficial and detrimental aspects. Hrsg. Boekhout, T., and V. Robert. Behr’s Verlag. Hamburg. Bretagne, S., J.-M. Costa, C. Besmond, R. Carsique, and R. Calderone. 1997. Microsatellite polymorphism in the promoter sequence of the elongation factor 3 gene of Candida albicans as the basis for a typing system. J. Clin. Microbiol. 35: 1777-1780. Bu, R., R. K. Sathiapalan, M. M. Ibrahim, I. Al-Mohsen, E. Almodavar, M. I. Gutierrez, and K. Bhatia. 2005. Monochrome LightCycler PCR assay for detection and quantification of five common species of Candida and Aspergillus. J. Med. Microbiol. 54: 243-248. Burkardt, H.-J. 2000. Standardization and quality control of PCR analyses. Clin. Chem. Lab. Med. 38: 87-91. Campbell, I. 2002. Wild yeasts in brewing and distilling. 187-205. In: Brewing microbiology. 3. Auflage. Hrsg. Priest, F. G., and I. Campbell. Chapman and Hall. London. Caplin, B. E., R. P. Rasmussen, P. S. Bernard, and C. T. Wittwer. 1999. LightCycler® Hybridisation probes – the most direct way to monitor PCR amplification and mutation detection. Biochemica. 1: 5-8. Casey, G. D., and A. D. W. Dobson. 2004. Potential of using real-time PCR-based detection of spoilage yeast in fruit juice-a preliminary study. Int. J. Food Microbiol. 91: 327-335. Cava, R.R., and P. S. Hernandez. 1994. Comparison of media for enumeration osmotolerant yeasts in orange juice concentrates. Int. J. Food Microbiol. 22: 291-295. Chatonnet, P., D. Dubourdieu, J. N. Boidron, and M. Pons. 1992. The origin of ethylphenols in wines. J. Sci. Food Agric. 60: 165-178. Chen, Y.-C., J. D. Eisner, M. M. Kattar, S. L. Rassoulian-Barrett, K. Lafe, U. Bui, A. P. Limaye, and B. T. Cookson. 2001. Polymorphic internal transcribed spacer region 1 DNA sequences identify medical important yeasts. J. Clin. Microbiol. 39: 4042-4051. Chilvers, K. F., R. H. Reed, and J. D. Perry. 1999. Phototoxicity of rose bengal in mycological media – implications for laboratory practice. Lett. Appl. Microbiol. 28: 103-107. Cocolin, L., K. Rantsiou, L. Iacumin, R. Zironi, and G. Comi. 2004. Molecular detection and identification of Brettanomyces/Dekkera bruxellensis and Brettanomyces/Dekkera anomalus in spoiled wines. Appl. Environ. Microbiol. 70: 1347-1355. Colthurst, D. R., G. P. Belfield, and M. F. Tuite. 1991a. Analysis of a novel elongation factor: EF-3. Biochem. Soc. Trans. 19: 279S. Colthurst, D. R., M. Santos, C. M. Grant, and M. F. Tuite. 1991b. Candida albicans and three other Candida species contain an elongation factor structurally and functionally analogous to elongation factor 3. FEMS Microbiol. Lett. 80: 45-50. 95 5 Literatur Connolly, P., S. J. Lewis, and J. E. L. Corry. 1988. A medium for the detection of yeasts using a conductimetric method. Int. J. Food Microbiol. 7: 31-40. Dalle, F., N. Franco, J. Lopez, O. Vagner, D. Caillot, P. Chavanet, B. Cuisenier, S. Aho, S. Lizard, and A. Bonnin. 2000. Comparative genotyping of Candida albicans bloodstream and nonbloodstream isolates at a polymorphic microsatellite locus. J. Clin. Microbiol. 38: 4554-4559. Dang, C., and S. D. Jayasena. 1996. Oligonucleotide inhibitors of Taq DNA polymerase facilitate detection of low copy number targets by PCR. J. Mol. Biol. 264: 268-78. Dasmahapatra, B., and K. Chakraburtty. 1981. Protein synthesis in yeast: I. Purification and properties of elongation factor 3 from Saccharomyces cerevisiae. J. Biol. Chem. 256: 9999-10004. Davenport, R. R. 1996. Forensic microbiology for the soft drinks business. Soft Drinks Management International. April: 34-35. Deák, T. 1991. Foodborne yeasts. Adv. Appl. Microbiol. 36: 179-278. Deák, T. 1995. Methods for the rapid detection and identification of yeasts in foods. Trends Food Sci. Technol. 6: 287-292. Deák, T. 2003. Detection, enumeration and isolation of yeasts. 39-68. In: Yeasts in food: beneficial and detrimental aspects. Hrsg. Boekhout, T., and V. Robert. Behr’s Verlag. Hamburg. Deák, T., and L. R. Beuchat. 1993. Yeasts associated with fruit juice concentrates. J. Food Prot. 56: 777-782. Deák, T., and L. R. Beuchat. 1994. Use of indirect conductimetry to predict the growth of spoilage yeasts, with special consideration of Zygosaccharomyces bailii. Int. J. Food Microbiol. 23: 405-417. de Barros Lopes, M., A. Soden, A. L. Martens, P. A. Henschke, and P. Langridge. 1998. Differentiation and species identification of yeasts using PCR. Int. J. Syst. Bacteriol. 48: 279286. de Barros Lopes, M., S. Rainieri, P. A. Henschke, and P. Langridge. 1999. AFLP fingerprinting for analysis of yeast genetic variation. Int. J. Syst. Bacteriol. 49: 915-924. Deere, D., J. Shen, G. Vesey, P. Bell, P. Bissinger, and D. Veal. 1998. Flow cytometry and cell sorting for yeast viability assessment and selection. Yeast: 147-160. Delaherche, A., O. Claisse, and A. Lonvaud-Funel. 2004. Detection and quantification of Brettanomyces bruxellensis and “ropy” Pediococcus damnosus strains in wine by real-time polymerase chain reaction. J. Appl. Microbiol. 97: 910-915. de Lamballerie, X., C. Zandotti, C. Vignoli, C. Bollet, and P. de Micco. 1992. A one-step microbial DNA extraction method using “Chelex 100” suitable for gene amplification. Res. Microbiol. 143: 785-790. 96 5 Literatur Dequin, S., J.-M. Salmon, H.-V. Nguyen, and B. Blondin. 2003. Wine yeasts. 389-412. In: Yeasts in food: beneficial and detrimental aspects. Hrsg. Boekhout, T., and V. Robert. Behr’s Verlag. Hamburg. Di Domenico, B. J., J. Lupisella, M. Sandbaken, and K. Chakraburtty. 1992. Isolation and sequence analysis of the gene encoding translation elongation factor 3 from Candida albicans. Yeast. 8: 337-352. Divol, B., and A. Lonvaud-Funel. 2005. Evidence for viable but nonculturable yeasts in botrytis-affected wine. J. Appl. Microbiol. 99: 85-93. Dufour, J.-P., K. Verstrepen, and G. Derdelinckx. 2003. Brewing yeasts. 347-388. In: Yeasts in food: beneficial and detrimental aspects. Hrsg. Boekhout, T., and V. Robert. Behr’s Verlag. Hamburg. Entis, P., and I. Lerner. 1996. Two-day yeast and mold enumeration using the ISO-GRID® Membrane Filtration System in conjugation with YM-11 agar. J. Food Prot. 59: 416-419. Erickson, J. P., and D. N. McKenna. 2000. Zygosaccharomyces. 2359-2365. In: Enzyclopedia of food microbiology. Hrsg. Robinson, R. K., C. A. Batt, and P. D. Patel. Academic Press. Erratt, J. A., and G. G. Stewart. 1978. Genetic and biochemical studies on yeast strains able to utilize dextrins. J. Am. Soc. Brew. Chem. 36: 151-161. Erratt, J. A., and A. Nasim. 1986. Cloning and expression of a Saccharomyces diastaticus glucoamylase gene in Saccharomyces cerevisiae and Schizosaccharomyces pombe. J. Bacteriol. 166: 484-490. Evans, H. A. V. 1982. A note on two uses for impedimetry in brewing microbiology. J. Appl. Bacteriol. 53. 423-426. Ferrati, A. R., P. Tavolaro, M. T. Destro, M. Landgraf, and B. D. G. M. Franco. 2005. A comparison of ready-to-use systems for evaluating the microbiological quality of acidic fruit juices using non-pasteurized orange juice as experimental model. Int. Microbiol. 8: 49-53. Fell, J. W., T. Boekhout, A. Fonseca, G. Scorzetti, and A. Statzell-Tallman. 2000. Biodiversity and systematics of basidiomycetous yeasts as determined by large-subunit rDNA D1/D2 domain sequence analysis. Int. J. Syst. Evol. Microbiol. 50: 1351-1371. Fernández, S., L. M. Almaguer, and J. A. Sierra. 1989. Detection of mixtures of lager strains by the use of selective inhibitors in solid media. J. Am. Soc. Brew. Chem. 47: 73-76. Fleet, G. 1992. Spoilage yeasts. Crit. Rev. Microbiol. 12: 1-44. Fleet, G. H., S. Lafon-Lafourcade, and P. Ribereau-Gayon. 1984. Evolution of yeasts and lactic acid bacteria during fermentation and storage of Bordeaux wines. Appl. Environ. Microbiol. 48: 1034-1038. García, T., B. Mayoral, I. González, I. López-Calleja, A. Sanz, P. E. Hernández, and R. Martín. 2004. Enumeration of yeast in dairy products: a comparison of immunological and genetic techniques. J. Food Prot. 67: 357-364. 97 5 Literatur Golden, D. A., and L. R. Beuchat. 1990. Colony formation of sublethally heat injured Zygosaccharomyces rouxii as affected by solutes in the recovery medium and procedure for sterilizing medium. Appl. Environ. Microbiol. 56: 2319-2326. Gontarek, R. R., H. Li, K. Nurse, and C. D. Prescott. 1998. The N terminus of eukaryotic translation elongation factor 3 interacts with 18 S rRNA and 80 S ribosomes. J. Biol. Chem. 273: 10249-10252. Guillamón, J. M., E. Barrio, T. Huerta, and A. Querol. 1994. Rapid characterization of four species of the Saccharomyces sensu stricto complex according to mitochondrial DNA patterns. Int. J. Syst. Bacteriol. 44: 708-714. Guillamón, J. M., E. Barrio, and A. Querol. 1996. Characterization of wine yeast strains of Saccharomyces genus on the basis of molecular markers: relationships between genetic distance and geographic origin. Syst. Appl. Microbiol. 19: 122-132. Guillamón, J. M., I. Sánchez, and T. Huerta. 1997. Rapid characterization of wild and collection strains of the genus Zygosaccharomyces according to mitochondrial DNA patterns. FEMS Microbiol. Lett. 147: 267-272. Haugland, R. A., J. L. Heckman, and L. J. Wymer. 1999. Evaluation of different methods for the extraction of DNA from fungal conidia by quantitative competitive PCR analysis. J. Microbiol. Methods. 37: 165-176. Hawronskyj, J.-M., and J. Holah. 1997. ATP: a universal hygiene monitor. Trends Food Sci. Technol. 8: 79-84. Heard, G. M., and G. H. Fleet. 1985. Growth of natural yeast flora during the fermentation of inoculated wines. Appl. Environ. Microbiol. 50: 727-728. Henschke, D. A., and D. S. Thomas. 1988. Detection of wine-spoilage yeasts by electrometric methods. J. Appl. Bacteriol. 64: 123-133. Henson, O. E. 1981. Dichloran as an inhibitor of mold spreading in fungal plating media: effects on colony diameter and enumeration. Appl. Environ. Microbiol. 42: 656-660. Heresztyn, T. 1986a. Metabolism of volatile phenolic compounds from hydroxycinnamic acids by Brettanomyces yeast. Arch. Microbiol. 146: 96-98. Heresztyn, T. 1986b. Formation of substituted tetrahydropyrimidines by species of Brettanomyces and Lactobacillus isolated from mousy wines. Am. J. Enol. Vitic. 37: 127-132. Hierro, N., Á. González, A. Mas, and J. M. Guillamón. 2004. New PCR-based methods for yeast identification. J. Appl. Microbiol. 97: 792-801. Higuchi, R., B. Krummel, and R. K. Saiki. 1988. A general method of in vitro preparation and specific mutagenesis of DNA fragments: study of protein and DNA interactions. Nucleic Acids Res. 16: 7351-7367. Hocking, A. D. 1996. Media for preservative resistant yeasts: a collaborative study. Int. J. Food Microbiol. 29: 167-175. Hocking, A. D., and J. I. Pitt. 1980. Dichloran-glycerol medium for enumeration of xerophilic fungi from low-moisture foods. Appl. Environ. Microbiol. 39: 488-492. 98 5 Literatur Hofstra, H., J. M. B. M. van der Vossen, and J. van der Plas. 1994. Microbes in food processing technology. FEMS Microbiol. Rev. 15: 175-183. Holland, P. M., R. D. Abramson, R. Watson, and D. H. Gelfand. 1991. Detection of specific polymerase chain reaction product by utilizing the 5´ → 3´ exonuclease activity of Thermus aquaticus DNA polymerase. Proc. Natl. Acad. Sci. USA. 88: 7276-7280. Hope, C. F. A., and R. S. Tubb. 1985. Approaches to rapid microbial monitoring in brewing. J. Inst. Brew. 91: 12-15. Hsu, M.-C., K.-W. Chen, H.-J. Lo, Y.-C. Chen, M.-H. Liao, Y.-H. Lin, and S.-Y. Li. 2003. Species identification of medically important fungi by use of real-time LightCycler PCR. J. Med. Microbiol. 52: 1071-1076. Hutchison, J. S., B. Feinberg, T. C. Rothwell, and K. Moldave. 1984. Monoclonal antibody specific for yeast elongation factor 3. Biochemistry. 23: 3055-3063. Hysert, D. W., F. Kovecses, and N. M. Morrison. 1976. A firefly bioluminescence ATP assay method for rapid detection and enumeration of brewery microorganisms. J. Am. Soc. Brew. Chem. 34: 145-150. Ibeas, J. I., I. Lozano, F. Perdigones, and J. Jimenez 1996. Detection of DekkeraBrettanomyces strains in sherry by a nested PCR method. Appl. Environ. Microbiol. 62: 9981003. Ikuta, S., K. Takagi, R. B. Wallace, and K. Itakura. 1987. Dissociation kinetics of 19 basepaired oligonucleotide-DNA duplexes containing different single mismatches base pairs. Nucleic Acids Res. 15: 797-811. Ison, R. W., and C. S. Gutteridge. 1987. Determination of carbonation tolerance of yeasts. Lett. Appl. Microbiol. 5: 11-13. James, S. A., J. Cai, I. N. Roberts, and M. D. Collins. 1997. A phylogenetic analysis of the genus Saccharomyces based on 18S rRNA gene sequences: description of Saccharomyces hunashirensis sp. nov. and Saccharomyces martiniae sp. nov. Int. J. Syst. Bacteriol. 47: 453460. James, S. A., and M. Stratford. 2003. Spoilage yeast with emphasis on the genus Zygosaccharomyces. 171-191. In: Yeasts in food: beneficial and detrimental aspects. Hrsg. Boekhout, T., and V. Robert. Behr’s Verlag. Hamburg. Jespersen, L., and M. Jakobsen. 1996. Specific spoilage organisms in breweries and laboratory media for their detection. Int. J. Food Microbiol. 33: 139-155. Jespersen, L., S. Lassen, and M. Jakobsen. 1993. Flow cytometric detection of wild yeast in lager breweries. Int. J. Food Microbiol. 17: 321-328. Josephson, K. L., C. P. Gerba, and I. L. Pepper. 1993. Polymerase chain reaction of nonviable bacterial pathogens. Appl. Environ. Microbiol. 59: 3513-3515. Kato, N. 1981. Antimicrobial activity of fatty acids and their esters against a film-forming yeast in soy sauce. J. Food Safety. 3: 121-126. 99 5 Literatur Kamath, A., K. Chakraburtty. 1989. Role of yeast elongation factor 3 in the elongation cycle. J. Biol. Chem. 264: 15423-15428. Kiel, M. C., H. Aoki, and M. C. Ganoza. 1999. Identification of a ribosomal ATPase in Escherichia coli cells. Biochimie. 81: 1097-1108. King, A. D. Jr., A. D. Hocking, and J. I. Pitt. 1979. Dichloran-rose Bengal medium for enumeration and isolation of molds from foods. Appl. Environ. Microbiol. 37: 959-964. Koshkin, A. A., P. Nielsen, M. Meldgaard, V. K. Rajwanshi, S. K. Singh, and J. Wengel. 1998. LNA (locked nucleic acid): an RNA mimic forming exeedingly stable LNA:LNA duplexes. J. Am. Chem. Soc. 120: 13252-13253. Kosse, D., H. Seiler, R. Amann, W. Ludwig, and S. Scherer. 1997. Identification of yoghurt-spoiling yeasts with 18S rRNA-targeted oligonucleotide probes. Syst. Appl. Microbiol. 20: 468-480. Kovalchuke, O., and K. Chakraburtty. 1995. Interaction of yeast elongation factor 3 with polynucleotides, ribosomal RNA and ribosomal subunits. Ind. J. Biochem. 32: 336-342. Krämer, J. 1997. Lebensmittel-Mikrobiologie. 3. Auflage. Verlag Eugen Ulmer. Stuttgart. Kreader, C. A. 1996. Relief of amplification inhibition in PCR with bovine serum albumin or T4 gene 32 protein. Appl. Environ. Microbiol. 62: 1102-1106. Kuniyuki, A. H., C. Rous, and J. L. Sanderson. 1984. Enzyme-linked immunosorbant assay (ELISA) detection of Brettanomyces contaminations in wine production. Am. J. Enol. Vitic. 35: 143-145. Kurtzman, C. P. 1994. Molecular taxonomy of the yeasts. Yeast. 10:1727-1740. Kurtzman, C. P., and C. J. Robnett. 1998. Identification and phylogeny of ascomycetous yeasts from analysis of nuclear large subunit (26S) ribosomal DNA partial sequences. Antonie van Leeuwenhoek. 73: 331-371. Kuske, C. R., K. L. Banton, D. L. Adorada, P. C. Stark, K. K. Hill, and P. J. Jackson. 1998. Small-scale DNA sample preparation method for field PCR detection of microbial cells and spores in soil. Appl. Environ. Microbiol. 64: 2463-2472. Laluce, C., and J. R. Mattoon. 1984. Development of rapidly fermenting strains of Saccharomyces diastaticus for direct conversion of starch and dextrins to ethanol. Appl. Environ. Microbiol. 48: 17-25. Laluce, C., M. C. Bertolini, J. R. Ernandes, A. Vaughan Martini, and A. Martini. 1988. New amylolytic yeast strains for starch and dextrin fermentation. Appl. Environ. Microbiol. 54: 2447-2451. Lambrechts, M. G., I. S. Pretorius, P. Sollitti, and J. Marmur. 1991. Primary structure and regulation of a glucoamylase-encoding gene (STA2) in Saccharomyces diastaticus. Gene. 100: 95-103. Lambrechts, M. G., I. S. Pretorius, V. S. D`Aguanno, P. Sollitti, and J. Marmur. 1994. Multiple positive and negative cis-acting elements of the STA2 gene regulate glucoamylase synthesis in Saccharomyces cerevisiae. Gene. 146: 137-144. 100 5 Literatur Lambrechts, M. G., I. S. Pretorius, J. Marmur, and P. Sollitti. 1995. The S1, S2 and SGA1 ancestral genes for STA glucoamylase genes all map to chromosome IX in Saccharomyces cerevisiae. Yeast. 11: 783-787. Lambrechts, M. G., F. F. Bauer, J. Marmur, and I. S. Pretorius. 1996. Muc1, a mucin-like protein that is regulated by Mss10, is critical for pseudohyphal differentiation in yeast. Proc. Natl. Acad. Sci. USA. 93: 8419-8424. La Rocco, K. A., K. A. Galligan, K. J. Little, and A. Spurgash. 1985. A rapid, bioluminescent ATP method for determining yeast contamination in a carbonated beverage. Food Technol. 39: 49-52. Lavallee, F., Y. Salva, S. Lamy, D. Y. Thomas, R. Degre, and L. Dulau. 1994. PCR and DNA fingerprinting used as quality control in the production of wine yeast strains. Am. J. Enol. Vitic. 45: 86-91. Lee, L.G., C. R. Connell and W. Bloch 1993. Allelic discrimination by nick-translation PCR with fluorogenic probes. Nucleic Acids Res. 21: 3761-3766. Lieckfieldt, E., W. Meyer, and T. Borner. 1993. Rapid identification and differentiation of yeast by DNA and PCR fingerprinting. J. Basic Microbiol. 33: 413-426. Lindsley, M. D., S. F. Hurst, N. J. Iqbal, and C. I. Morrison. 2001. Rapid identification of dimorphic and yeast-like fungal pathogens using specific DNA probes. J. Clin. Microbiol. 39: 3505-3511. Loeffler, J., N. Henke, H. Hebart, D. Schmidt, L. Hagmeyer, U. Schumacher, and H. Einsele. 2000. Quantification of fungal DNA by using fluorescence resonance energy transfer and the Light Cycler System. J. Clin. Microbiol. 38: 586-590. Loeffler, J., K. Schmidt, H. Hebart, U. Schumacher, and H. Einsele. 2002. Automated extraction of genomic DNA from medically important yeast species and filamentous fungi by using the MagNA Pure LC System. J. Clin. Microbiol. 40: 2240-2243. Longo, M. C., M. S. Berninger, and J. L. Hartley. 1990. Use of uracil DNA glycosylase to control carry-over contamination in polymerase chain reactions. Gene. 93: 125-128. Loureiro, V., and M. Malfeito-Ferreira. 2003. Spoilage yeasts in the wine industry. Int. J. Food Microbiol. 86: 23-50. Lowder, M., A. Unge, N. Maraha, J. K. Jansson, J. Swiggett, and J. D. Oliver. 2000. Effect of starvation and the viable but nonculturable state on green fluorescent protein fluorescence in GFP tagged Pseudomonas fluorescens A506. Appl. Environ. Microbiol. 66: 31603165. Lyon, W. J. 2001. TaqMan PCR for detection of Vibrio cholerae O1, O139, non-O1, and non-O139 in pure cultures, raw oysters, and synthetic seawater. Appl. Environ. Microbiol. 67: 4685-4693. Maaroufi, Y., C. Heymans, J.-M. De Bruyne, V. Duchateau, H. Rodriguez-Villalobos, M. Aoun, and F. Crokaert. 2003. Rapid detection of Candida albicans in clinical blood samples by using a TaqMan-based PCR assay. J. Clin. Microbiol. 41: 3293-3298. 101 5 Literatur Makdesi, A. K., and L. R. Beuchat. 1996. Evaluation of media for enumeration heatstressed, benzoate-resistant Zygosaccharomyces bailii. Int. J. Food. Microbiol. 33: 169-181. Mäntynen, V. H., M. Korhola, H. Gudmundsson, H. Turakainen, G. A. Alfredsson, H. Salovaara, and K. Lindström. 1999. A polyphasic study on the taxonomic position of industrial sour dough yeasts. System. Appl. Microbiol. 22: 87-96. Marcilla, A., C. Monteagudo, S. Mormeneo, and R. Sentandreu. 1999. Monoclonal antibody 3H8: a useful tool in the diagnosis of candidiasis. Microbiol. 145: 695-701. Masters, C. I., J. A. Shallcross, and B. M. Mackey. 1994. Effect of stress treatment on the detection of Listeria monocytogenes and enterotoxigenic Escherichia coli by the polymerase chain reaction. J. Appl. Bacteriol. 77: 73-79. Mättö, J., M. Saarela, S. Alaluusua, V. Oja, H. Jousimies-Somer, and S. Asikainen. 1998. Detection of Porphyromonas gingivalis from saliva by PCR by using a simple sampleprocessing method. J. Clin. Microbiol. 36: 157-160. McCarroll, R., G. J. Olsen, Y. D. Stahl, C. R. Woese, and M. L. Sogin. 1983. Nucleotide sequence of Dictyostelium discoideum small-subunit ribosomal ribonucleic acid inferred from the gene sequence: evolutionary implications. Biochemistry. 22: 5858-5868. McDougald, D., S. A. Rice, D. Weichart, and S. Kjellberg. 1998. Nonculturable: adaptation or debilitation. FEMS Microbiol. Ecol. 25: 1-9. Merrick, W. C. 1992. Mechanism and regulation of eukaryotic protein synthesis. Microbiol. Rev. 56: 291-315. Meyer, W., T. G. Mitchell, E. Freedman, and R. Vilgalys. 1993. Hybridization probes for conventional DNA fingerprinting used as single primers in the polymerase chain reaction to distinguish strains of Cryptococcus neoformans. J. Clin. Microbiol. 31: 2274-2280. Middelhoven, W., J., and S. Notermans. 1988. Species-specific extracellular antigen production by ascomycetous yeasts, detected by ELISA. J. Gen. Appl. Microbiol. 34: 15-26. Middelhoven, W., J., and S. Notermans. 1993. Immuno-assay techniques for detecting yeasts in food. Int. J. Food Microbiol. 19: 53-62. Millard, P. L., B. L. Roth, H.-P. Truong Thi, S. T. Yue, and R. P. Haugland. 1997. Development of the FUN-1 family of fluorescent probes for vacuole labelling and viability testing of yeasts. Appl. Environ. Microbiol. 63: 2897-2905. Millet, V., and A. Lonvaud-Funel. 2000. The viable but non-culturable state of wine microorganisms during storage. Lett. Appl. Microbiol. 30: 136-141. Miller, M. W. 1979. Yeasts in food spoilage: an update. Fd. Technol. 33: 76-80. Miller, R., and G. Galston. 1989. Rapid methods for the detection of yeast and Lactobacillus by ATP bioluminescence. J. Inst. Brew. 95: 317-320. Minárik, E. 1981. Zur Ökologie von Hefen und hefeartigen Mikroorganismen abgefüllter Weine. Wein-Wissenschaft. 36: 280-285. 102 5 Literatur Mita, K., M. Morimyo, K. Ito, K. Sugaya, K. Ebihara, E. Hongo, T. Higashi, Y. Hirayama, and Y. Nakamura. 1997. Comprehensive cloning of Schizosaccharomyces pombe genes encoding translation elongation factors. Gene. 187: 259-266. Molina, F. I., S.-C. Jong, and J. L. Huffman. 1993. PCR amplification of the 3` external transcribed and intergenic spacer of the ribosomal DNA repeat unit in three species of Saccharomyces. FEMS Microbiol. Lett. 108: 259-264. Mortimer, R., and M. Polsinelli. 1999. On the origins of wine yeasts. Res. Microbiol. 150: 199-204. Müller, F.-M. C., K. E. Werner, M. Kasai, A. Francesconi, S. J. Chanock, and T. J. Walsh. 1998. Rapid extraction of genomic DNA from medically important yeasts and filamentous fungi from high-speed cell disruption. J. Clin. Microbiol. 36: 1625-1629. Myers, K. K., W. A. Fonzi, and P. S. Sypherd. 1992. Isolation and sequence analysis of the gene for translation elongation factor 3 from Candida albicans. Nucleic Acids Res. 20: 17051710. Naumov, G. I., I. Masneuf, E. S. Naumova, M. Aigle, and D. Durbourdieu. 2000. Association of Saccharomyces bayanus var. uvarum with some French wines: genetic analysis of yeast populations. Res. Microbiol. 151: 683-691. Needleman, S. B., and C. D. Wunsch. 1970. A general method applicable to the search for similarities in the amino acid sequence of two proteins. Mol. Biol. 48: 443-453. Niesters, H. G. M., W. H. F. Goessens, J. F. M. G. Meis, and W. G. V. Quint. 1993. Rapid, polymerase chain reaction-based identification assays for Candida species. J. Clin. Microbiol. 31: 904-910. Nogva, H. K., A. Bergh, A. Holck, and K. Rudi. 2000. Application of the 5´-nuclease PCR assay in evaluation and development of methods for quantitative detection of Campylobacter jejuni. Appl. Environ. Microbiol. 66: 4029-4036. Oliver, J. D. 1993. Formation of viable but non culturable cells. 239-271. In: Starvation in Bacteria. Hrsg. Kjellberg, S. Plenum Press. New York. Oliver, J. D., F. Hite, D. McDougald, M. L. Andon, and L. M. Simpson. 1995. Entry into and resuscitation from the viable but non culturable state by Vibrio vulnificus in an etuarine environment. Appl. Environ. Microbiol. 61: 2624-2630. Pardo, J. M., J. Polaina, and A. Jiménez. 1986. Cloning of the STA2 and SGA genes encoding glucoamylases in yeasts and regulation of their expression by the STA10 gene of Saccharomyces cerevisiae. Nucleic Acids Res. 14: 4701-4718. Parish, M. E., D. P. Higgins. 1989. Yeasts and molds isolated from spoilage citrus products and by-products. J. Food Prot. 52: 261-263. Pearson, G. A., and R. A. McKee. 1992. Rapid identification of Saccharomyces cerevisiae, Zygosaccharomyces bailii, and Zygosaccharomyces rouxii. J. Food Microbiol. 16: 63-67. Perpète, P., P. van Cutsem, C. Boutte, A. M. Colson-Corbisier, and S. Collin. 2001. Amplified fragment-length polymorphism, a new method for the analysis of brewer`s yeast DNA polymorphism. J. Am. Soc. Brew. Chem. 59: 195-200. 103 5 Literatur Pettipher, G. L., Y. B. Watts, S. A. Langford, and R. G. Kroll. 1992. Preliminary evaluation of COBRA, an automated DEFT instrument, for the rapid enumeration of micro-organisms in cultures, raw milk, meat and fish. Lett. Appl. Microbiol. 14: 206-209. Phister, T. G., and D. A. Mills. 2003. Real-time PCR assay for detection and enumeration of Dekkera bruxellensis in wine. Appl. Environ. Microbiol. 69: 7430-7434. Pitt, J. I., and A. D. Hocking. 1997. Fungi and food spoilage. Second Edition. Blackie Academic & Professional. London. Powell, C, and K. Smart. 2003. A comparison of new and traditional methods for the detection of brewery contaminants. In: Proceedings of the 29th European Brewery Convention Congress. Dublin. 2003. Pretorius, I. S., T. Chow, and J. Marmur. 1986. Identification and physical characterization of yeast glucoamylase structural genes. Mol. Gen. Genet. 203: 36-41. Pretorius, I. S., and J. Marmur. 1988. Localization of yeast glucoamylase genes by PFGE and OFAGE. Curr. Genet. 14: 9-13. Qin, S., A. Xie, C. M. Bonato, and C. S. McLaughlin. 1990. Sequence analysis of the translational elongation factor 3 from Saccharomyces cerevisiae. J. Biol. Chem. 265: 1903-1912. Rodrigues, U. M., and R. G. Kroll. 1986. Use of the direct epifluorescent filter technique for the enumeration of yeasts. J. Appl. Bacteriol. 61: 139-144 Rodrigues, N., G. Goncalves, M. Malfeito-Ferreira, and V. Loureiro. 2001. Development and use of a differential medium to detect yeasts of the genera Dekkera/Brettanomyces. Int. J. Food Microbiol. 90: 588-599. Rosenstraus, M., Z. Wang, S.-Y. Chang, D. DeBonville, and J. P. Spadoro. 1998. An internal control for routine diagnostic PCR: design, properties, and effect on clinical performance. J. Clin. Microbiol. 36: 191-197. Rossen, L., P. Norskov, K. Holmstrom, and O. F. Rasmussen. 1992. Inhibition of PCR by components of food samples, microbial diagnostic assays, and DNA-extraction solutions. Int. J. Food Microbiol. 17: 37-45. Safarík, I., M. Safaríková, and S. J. Forsythe. 1995. The application of magnetic separations in applied microbiology. J. Appl. Bacteriol. 78: 575-585. Saiki, R. K., S. Scharf, F. Faloona, K. B. Mullis, G. T. Horn, H. A. Erlich, and N. Arnheim. 1985. Enzymatic amplification of beta-globin genomic sequences and restriction site analysis for diagnosis of sickle cell anemia. Science. 230: 1350-1354. Saiki, R. K., D. H. Gelfand, S. Stoffel, S. J. Scharf, R. Higuchi, G. T. Horn, K.B. Mullis, and H. A. Ehrlich. 1988. Primer-directed enzymatic amplification of DNA with a thermostable DNA polymerase. Science. 239: 487-491. Saitou, N., and M. Nei. 1987. The neighbour-joining method: a new method for reconstructing phylogenetic trees. Mol. Biol. Evol. 4: 406-425. Sambrook, J., E. F. Fritsch, and T. Maniatis. 1989. Molecular cloning. A laboratory manual. Second Edition. Cold Spring Harbour Laboratory Press. New York. 104 5 Literatur Sand, F. E. M. J., and A. M. van Grinsven. 1976. Investigation of yeast strains isolated from Scandinavian soft drinks. Brauwissenschaften. 29: 353-355. Sandbaken, M., J. A. Lupisella, B. Di Domenico, and K. Chakraburtty. 1990a. Isolation and characterization of the structural gene encoding elongation factor 3. Biochim. Biophys. Acta. 1050: 230-234. Sandbaken, M., J. A. Lupisella, B. Di Domenico, and K. Chakraburtty. 1990b. Protein synthesis in yeast: Structural and functional analysis of the gene encoding elongation factor 3. J. Biol. Chem. 1990:15838-15844. Sarthy, A. V., T. Mcgonigal, J. O. Capobianco, M. Schmidt, S. R. Green, C. M. Moehle, and R. C. Goldman. 1998. Identification and kinetic analysis of a functional homolog of elongation factor 3, YEF3 in Saccharomyces cerevisiae. Yeast. 14: 239-253. Schaertel, B. J., N. Tsang, and R. Firstenberg-Eden. 1987. Impedimetric detection of yeast and mold. Food Microbiol. 4: 155-163. Scheda, R., and D. Yarrow. 1966. The instability of physiological properties used as criteria in the taxonomy of yeast. Arch. Microbiol. 55: 209-225. Schütz, E., and N. von Ahsen. 1999. Spreadsheet software for thermodynamic melting point prediction of oligonucleotide hybridization with and without mismatches. Biotechniques. 27: 1218-1224. Scorzetti, G., J. W. Fell, A. Fonseca, and A. Statzell-Tallman. 2002. Systematics of basidiomycetous yeasts: a comparison of large subunit D1/D2 and internal transcribed spacer rDNA regions. FEMS Yeast Res. 2: 495-517. Seifert, K. A., B. D. Wingfield, and M. J. Wingfield. 1995. A critique of DNA sequence analysis in the taxonomy of filamentous ascomycetes and ascomycetous anamorphs. Can. J. Bot. 73: S760-S767. Sharkey, D. J., E. R. Scalice, K. G. Christy Jr., S. M. Atwood and J. L. Daiss. 1994. Antibodies as thermolabile switches: high temperature triggering for the polymerase chain reaction. Bio/Technology 12: 506-509. Sheridan, G. E. C., C. I. Masters, J. A. Shallcross, and B. M. Mackey. 1998. Detection of mRNA by reverse transcription-PCR as an indicator of viability in Escherichia coli cells. Appl. Environ. Microbiol. 64: 1313-1318. Skogerson, L., and E. Wakatama. 1976. A ribosome-dependent GTPase from yeast distinct from elongation factor 2. Proc. Nat. Acad. Sci. USA. 73: 73-76. Smart, K. A., K. M. Chambers, I. Lambert, and C. Jenkins. 1999. Use of methylene violet staining procedures to determine yeast viability and vitality. J. Am. Soc. Brew. Chem. 57: 1823. Stecchini, M., and L. R. Beuchat. 1985. Effects of sugars in growth media, diluents and enumeration media on survival and recovery of Saccharomyces cerevisiae heated in peach puree. Food Microbiol. 2: 85-95. 105 5 Literatur Steels, H., S. A. James, I. N. Roberts, and M. Stratford. 1999a. Zygosaccharomyces lentus: a significant new osmophilic, preservative-resistant spoilage yeast, capable of growth at low temperature. J. Appl. Microbiol. 87: 520-527. Steels, H., C. J. Bond, M. D. Collins, I. N. Roberts, M. Stratford, and S. A. James. 1999b. Zygosaccharomyces lentus sp. nov., a new member of the yeast genus Zygosaccharomyces Barker. Int. J. Syst. Bacteriol. 49: 319-327. Steels, H., S. A. James, I. N. Roberts, and M. Stratford. 2000. Sorbic acid resistance: the inoculum effect. Yeast. 16: 1173-1183. Stender, H., C. Kurtzman, J. J. Hyldig-Nielsen, D. Sørensen, A. Broomer, K. Oliveira, H. Perry-O`Keefe, A. Sage, B. Young, and J. Coull. 2001. Identification of Dekkera bruxellensis (Brettanomyces) from wine by fluorescence in situ hybridization using peptide nucleic acid probes. Appl. Environ. Microbiol. 67: 938-941. Stratford, M., and S. A. James. 2003. Non-alcoholic beverages and yeasts. 309-345. In: Yeasts in food: beneficial and detrimental aspects. Hrsg. Boekhout, T., and V. Robert. Behr`s Verlag. Hamburg. Swaminathan, B., and P. Feng. 1994. Rapid detection of food-borne pathogenic bacteria. Annu. Rev. Microbiol. 48: 401-426. Takahashi, T., Y. Nakakita, J. Watari and K. Shinotsuka. 2000. Application of a bioluminescence method for the beer industry: sensitivity of MicroStar™-RMDS for detecting beerspoilage bacteria. Biosci. Biotechnol. Biochem. 64: 1032-1037. Tamaki, H. 1978. Genetic studies of ability to ferment starch in Saccharomyces: gene polymorphism. Mol. Gen. Genet. 164: 205-209. Teo, I. A., J. W. Choi, J. Morlese, G. Taylor, and S. Shaunak. 2002. LightCycler qPCR optimisation for low copy number target DNA. J. Immun. Methods. 270: 119-133. Thompson, J. D., D. G. Higgins, and T. J. Gibson. 1994. CLUSTAL W: improving the sensitivity of progressive multiple sequence alignment through sequence weighting, positionspecific gap penalties and weight matrix choice. Nucleic Acids Res. 22: 4673-4680. Thornewell, S. J., R. B. Peery, and P. L. Skatrund. 1997. Cloning and molecular characterization of CnTEF1 which encodes translation elongation factor 1 alpha in Cryptococcus neoformans. Fungal Genet. 22: 84-91. Tompkins, T. A., R. Stewart, L. Savard, I. Russell, and T. M. Dowhanick. 1996. RAPDPCR characterization of brewery yeast and beer spoilage bacteria. J. Am. Soc. Brew. Chem. 54: 91-96. Torriani, S., G. Zapparoli, P. Malacrino, G. Suzzi, and F. Dellaglio. 2004. Rapid identification and differentiation of Saccharomyces cerevisiae, Saccharomyces bayanus and their hybrids by multiplex PCR. Lett. Appl. Microbiol. 38: 239-244. Török, T., and A. D. King Jr. 1991. Comparative study on the identification of food-borne yeasts. Appl. Environ. Microbiol. 57: 1207-1212. Török, T., D. Rockhold, and A. D. King. 1993. Use of electrophoretic karyotyping and DNADNA hybridization in yeast identification. Int. J. Food Microbiol. 19: 63-80. 106 5 Literatur Triana-Alonso, F. J., K. Chakraburtty, and K. H. Nierhaus. 1995. The elongation factor 3 unique in higher fungi and essential for protein biosynthesis is an E site factor. J. Biol. Chem. 270: 20473-20478. Turenne, C. Y., S. E. Sanche, D. J. Hoban, J. A. Karlowsky, and A. M. Kabani. 1999. Rapid identification of fungi by using the ITS2 genetic region and an automated fluorescent capillary electrophoresis system. J. Clin. Microbiol. 37: 1846-1851. Tyagi, S., and F. R. Kramer. 1996. Molecular beacons: probes that fluoresce upon hybridization. Nat. Biotechnol. 14: 303-308. Uritani, M., and M. Miyazaki. 1988. Role of yeast peptide elongation factor 3 (EF-3) at the AA-tRNA binding step. J. Biochem. 104: 118-126. Uritani, M., Y. Shoumuru, and S. Yamada. 1999. Detection and analysis of translation elongation factor 3 genes from various yeasts. Biosci. Biotechnol. Biochem. 63: 769-772. Vaitilingom, M., F. Gendre, and P. Brignon. 1998. Direct detection of viable bacteria, molds and yeasts by reverse transcriptase PCR in contaminated milk samples after heat treatment. Appl. Environ. Microbiol. 64: 1157-1160. Valente, P., J. P. Ramos, and O. Leoncini. 1999. Sequencing as a tool in yeast molecular taxonomy. Can. J. Microbiol. 45: 949-958. van Burik, J.-A. H., R. W. Schreckhise, T. C. White, R. A. Bowden, and D. Myerson. 1998. Comparison of six extraction techniques for isolation of DNA from filamentous fungi. Med. Mycol. 36: 299-303. van der Aa Kühle, A., and L. Jespersen. 1998. Detection and identification of wild yeasts in lager breweries. Int. J. Food Microbiol. 43: 205-213. van der Vossen, J. M. B. M., and H. Hofstra. 1996. DNA based typing, identification and detection systems for food spoilage microorganisms: development and implementation. Int. J. Food Microbiol. 33: 35-49. Vaughan Martini, A., and A. Martini. 1987a. Three newly delimited species of Saccharomyces sensu stricto. Antonie van Leeuwenhoek. 53: 77-84. Vaughan Martini, A., and A. Martini. 1987b. Taxonomic revision of yeast genus Kluyveromyces by nuclear deoxyribonucleic acid reassociation. Int. J. Syst. Bacteriol. 37: 380-385. Vaughan Martini, A. 1989. Saccharomyces paradoxus comb. nov., a newly separated species of the Saccharomyces sensu stricto complex based upon nDNA/nDNA homologies. Syst. Appl. Microbiol. 12: 179-182. Versavaud, A., and J. N. Hallet. 1995. Pulsed-field gel electrophoresis combined with rarecutting endonucleases for strain identification of Candida famata, Kloeckera apiculata and Schizosaccharomyces pombe with chromosome number and size estimation of the two former. Syst. Appl. Microbiol. 18: 303-309. Vezinhet, F., B. Blondin, and J. N. Hallet. 1990. Chromosomal DNA patterns and mitochondrial DNA polymorphism as tools for identification if enological strains of Saccharomyces cerevisiae. Appl. Microbiol. Biotechnol. 32: 568-571. 107 5 Literatur Vilgalys, R., and M. Hester. 1990. Rapid genetic identification and mapping of enzymatically amplified ribosomal DNA from several Cryptococcus species. J. Bacteriol. 172: 4238-4246. Vivier, M. A., M. G. Lambrechts, and I. S. Pretorius. 1997. Coregulation of starch degradation and dimorphism in the yeast Saccharomyces cerevisiae. Crit. Rev. Biochem. Mol. Biol. 32: 405-435. Vivier, M. A., P. Sollitti, and I. S. Pretorius. 1999. Functional analysis of multiple AUG codons in the transcripts of the STA2 glucoamylase gene from Saccharomyces cerevisiae. Mol. Gen. Genet. 261: 11-20. Vlaemynck, G. M. 1994. Comparison of Petrifilm™ and plate count methods for enumerating molds and yeasts in cheese and yoghurt. J. Food Prot. 57: 913-914. von Ahsen, N., M. Oellerich, V. W. Armstrong, and E. Schütz. 1999. Application of a thermodynamic nearest-neighbour model to estimate nucleic acid stability and optimize probe design: Prediction of melting points of different mutations of apolipoprotein B 3500 and factor V Leiden with a hybridization probe genotyping assey on the LightCycler. Clin. Chem. 45: 2094-2101. Vos, P., R. Hogers, M. Bleeker, M. Reijans, T. van de Lee, M. Hornes, A. Frijters, J. Pot, J. Peleman, M. Kuiper and M. Zabeau. 1995. AFLP: a new technique for DNA fingerprinting. Nucleic Acids Res. 23: 4407-4414. Walsh, P. S., D. A. Metzger, and R. Higuchi. 1991. Chelex 100 as a medium for simple extraction of DNA for PCR-based typing from forensic material. Biotechniques. 10: 506-513. Watson-Craik, I. A., K. E. Aidoo, and J. G. Anderson. 1990. Development and evaluation of a medium for the monitoring of food-borne moulds by capacitance changes. Food Microbiol. 7: 129-145. Weidenbörner, M. 1998. Lebensmittel-Mykologie. B. Behr`s Verlag, Hamburg. Weidenbörner, M. 2000. Lexikon der Lebensmittelmykologie. Springer-Verlag, Berlin Heidelberg. Weihe, J. L., S. L. Seist, and W. S. Hatcher. 1984. Estimation of microbial populations in frozen concentrated orange juice using automated impedance measurements. J. Food Sci. 49: 243-245. Whitcombe, D., J. Theaker, S. P. Guy, T. Brown, and S. Little. 1999. Detection of PCR products using self-probing amplicons and fluorescence. Nat. Biotechnol. 17: 804-807. White, P. L., A. Shetty, and R. A. Barnes. 2003. Detection of seven Candida species using the Light-Cycler system. J. Med. Microbiol. 52: 229-238. White, T. J., T. Bruns, S. Lee, and J. Taylor. 1990. Amplification and direct sequencing of fungal ribosomal RNA genes for phylogenetics, p. 315-322. In M. A. Innis, D. H. Gelfand, J. J, Sninsky, and T. J. White (ed.), PCR protocols: A guide to methods and applications. Academic Press, San Diego, Calif. Wilson, I. G. 1997. Inhibition and facilitation of nucleic acid amplification. Appl. Environ. Microbiol. 63: 3741-3751. 108 5 Literatur Xufre, A., F. Simões, F. Girio, A. Clemente, and M. T. Amaral-Collaço. 2000. Use of RAPD analysis for differentiation among six enological Saccharomyces spp. strains. Food Technol. Biotechnol. 38: 53-58. Yamada, T., T. Fukuda, K. Tamura, S. Furukawa, and P. Songsri. 1993. Expression of the gene encoding a translational elongation factor 3 homolog of Chlorella virus CVK2. Virology. 197: 742-750. Yamagishi, H., Y. Otsuta, W. Funahashi, T. Ogata, and K. Sakai. 1999. Differentiation between brewing and non-brewing yeasts using a combination of PCR and RFLP. J. Appl. Microbiol. 86: 505-513. Yamashita, I., and S. Fukui. 1985. Transcriptional control of the sporulation-specific glucoamylase gene in the yeast Saccharomyces cerevisiae. Mol. Cell. Biol. 5: 3069-3073. Yamashita, I., K. Suzuki, and S. Fukui. 1985a. Nucleotide sequence of the extracellular glucoamylase gene STA1 in the yeast Saccharomyces diastaticus. J. Bacteriol. 161: 567573. Yamashita, I., T. Maemura, T. Hatamo, and S. Fukui. 1985b. Polymorphic extracellular glucoamylase genes and their evolutionary origin in the yeast Saccharomyces diastaticus. J. Bacteriol. 161: 574-582. Yamashita, I., M. Nakamura, and S. Fukui. 1987. Gene fusion is a possible mechanism underlying the evolution of STA1. J. Bacteriol. 169: 2142-2149. Yamauchi, H., H. Yamamoto, Y. Shibano, N. Amaya, and T. Saeki. 1998. Rapid methods for detection Saccharomyces diastaticus, a beer spoilage yeast, using the polymerase chain reaction. J. Am. Soc. Brew. Chem. 56: 58-63. Yoshida, M., H. Maeda, and Y. Ifuku. 1991. Rapid detection of yeast in orange juice by enzyme-linked immunosorbent assay. Agric. Biol. Chem. 55: 2951-2957. Ypma-Wong, M. F., W. A. Fonzi, and P. S. Sypherd. 1992. Fungus-specific translation elongation factor 3 gene present in Pneumocystis carinii. Inf. Immun. 60: 4140-4145. Zindulis, J. 1984. A medium for the impedimetric detection of yeasts in food. Food Microbiol. 1: 159-167. 109 6 Anhang 6 Anhang 6.1 Getestete Mikroorganismen Tab. 6.1: Stämme für die Spezifitätstestung der Real-Time PCR für S. cerevisiae var. diastaticus Spezies Candida boidinii Candida magnoliae Candida sake Candida tropicalis Cryptococcus albidus Debaryomyces hansenii Dekkera anomala Dekkera anomala Dekkera bruxellensis Dekkera bruxellensis Dekkera custersiana E. coli E. coli Serovar O157:H7 Hanseniaspora uvarum Issatchenkia orientalis Kazachstania unispora Kluyveromyces marxianus Kluyveromyces marxianus Lactobacillus brevis Lactobacillus casei Lactobacillus collinoides Lactobacillus coryniformis Lactobacillus lindneri Lactobacillus parabuchneri Lactobacillus plantarum Lactobacillus perolens Megasphaera cerevisiae Pectinatus cerevisiiphilus Pectinatus frisingensis Pediococcus damnosus Pediococcus inopinatus Pediococcus parvulus Pediococcus claussenii Pediococcus pentosaceus Pichia anomala Pichia anomala Pichia membranaefaciens Rhodotorula sp. Rhodotorula glutinis Rhodotorula rubra S. bayanus S. bayanus S. bayanus S. carlsbergensis (=S. past.) S. carlsbergensis (=S. past.) S. carlsbergensis (=S. past.) S. carlsbergensis (=S. past.) S. carlsbergensis (=S. past.) S. pastorianus S. pastorianus Stamm/Herkunft DSM 70024 DSM 70638 CBS 2920 ATCC 20247 DSM 70197 BCD 3512 DSM 70727 DSM 70732 DSM 3429 DSM 70726 DSM 70736 DSM 30083 BCD 5579 ATCC 9774 CBS 5147 BCD 877 DSM 70106 BCD 5186 DSM 20054 DSM 20011 DSM 20515 DSM 20001 DSM 20690 DSM 5707 DSM 20174 DSM 12744 DSM 20462 DSM 20467 DSM 6306 DSM 20331 DSM 20285 DSM 20332 DSM 14800 DSM 20336 BCD 1082 DSM 70783 DSM 70178 ATCC 20254 BCD 3530 BCD 4081 BCD 1256 BCD 1392 DSM 70412 BCD 2573 BCD 2574 BCD 2581 ATCC 9080 BCD 728 NCYC 73 DSM 6580 Spezies S. cerevisiae S. cerevisiae S. cerevisiae S. cerevisiae S. cerevisiae S. cerevisiae S. cerevisiae S. cerevisiae S. cerevisiae S. cerevisiae S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. cerevisiae var. diastaticus S. exiguus S. exiguus S. exiguus S. kluyveri Saccharomycopsis fibuligera Schizosaccharomyces pombe Torulaspora delbrueckii Z. bailii Z. bisporus Z. cidri Z. fermentati Z. lentus Z. rouxii Z. rouxii 110 Stamm/Herkunft ATCC 44075 CBS 6503 ATCC 12341 ATCC 18790 ATCC 28383 DSM 70452 DSM 1333 DSM 70416 Brauerei E Brauerei D BCD 1257 BCD 1432 BCD 1433 BCD 1499 BCD 1501 BCD 13974 BCD 13980 DSM 70487 VTT C-68059 VTT C-70060 VTT C-82101 Brauerei A Brauerei A Brauerei A Brauerei A Brauerei A Brauerei A Brauerei B Brauerei B Brauerei C Brauerei C Brauerei D Brauerei D Brauerei D Brauerei E BCD 1491 BCD 1493 MUCL 29838 DSM 70517 ATCC 9947 BCD 773 CBS 5636 MUCL 28823 DSM 70415 MUCL 31280 MUCL 27824 CBS 8516 DSM 70835 ATCC 48230 6 Anhang 6.2 Sequenzauswertung Abb. 6.1: Alignment der Nucleinsäuresequenzen des EF-3 Sequenzabschnitts (Position 2272-2637) mit Angabe der Primerpositionen. HS10 HS11/I-IV Ha1f-5f Yfa1-2,Yfs1 Ca AF038153 Ca ATCC 10231 Cb DSM 70034 Cc DSM 70136 Cd DSM 70042 Ce DSM70858 Cg BCD 8932 Cglae CBS 5691 Ch DSM 70624 Cim BCD 1062 Cint BCD 685 Ck BCD 689 Cll DSM 70102 Cm DSM 70638 Cmal AB018532 Cmal BCD 806 Cmel AB018533 Cmu DSM 70862 Cp ATCC 20384 Cr BCD 814 Cs BCD 1054 Csan CBS 4261 Cso BCD 818 Ct BCD 819 Ctr ATCC 20326 Cv DSM 6956 Cvi DSM 70184 Cz AB018534 Cz BCD 690 De ATCC 20126 Dekb DSM 3429 Dekb DSM 70726 Dekc DSM 70736 Dh BCD 3512 Dh BCD 589 Dm ATCC 11627 Ef BCD 3514 Ef DSM 70554 Gs DSM 3431 Hb BCD 859 Hb DSM 3505 Hg DSM 70285 Hu ATCC 9774 Hu BCD 3526 Hv DSM 70283 Io CBS 5147 Kl AB018535 Km BCD 2563 Km BCD 5186 Km BCD 811 Km DSM 70106 Km DSM 70792 Ku BCD 877 Le DSM 70320 Lt CBS 6340 Mp DSM 70321 Pa DSM 70277 Pan BCD 1082 Pan DSM 70783 Pc CBS 601 Pcar DSM 70392 Pf BCD 861 Pfe BCD 711 Pfe DSM 70090 Pg BCD 804 Pm DSM 70178 1 10 20 30 40 50 60 70 75 |--------|---------|---------|---------|---------|---------|---------|----||-------------------| |--------------------| |-----------------------| |-------------------| TGGAGATTCCAAACTGGTGAAGATAGAGAAACCATGGATAGAGCCTCTAGACAAATCAATGAAGAAGATGAACAAA TGGAGGTTCCAGTCTGGTGAAGATAGAGAAACCATGGATAGAGCTTCTAGACAAATCAATGAAGAAGATGAACAAA TGGCGGTACCAGACTGGTGAAGATCGTGAAACTATGGGTAGGGCTTCTAGACAAATTAACGAAAATGATGAAGAAG TGGAGGTTCCAGACTGGTGAGGACAGAGAAACCATGGACCGTGCTTCCAGACAGGTTACCGAGGAAGACGAGAACA TGGAGGTACCAAACTGGTGAAGATCGAGAGACTATGGATCGAGCCAATCGACAGATCGATGAAAATGATGAGGAAG --------------------AGATAGAGAAACCATGGACAGAGCTTCAAGACAAATCAATGAAAATGATGAAGAAA TGGAGGTACCAAACCGGTGAAGATAGAGAAACTATGGACAGAGCTAACAGACAAATCAACGAAGATGATGAAGCTG TGGCGGTACCAGACTGGTGAAGATAGAGAAACCATGGACAGAGCCAACAGACAAGTTACTGAAAAGGATGAAGAAA TGGCGGTACCACACTGGTGAGGACAGAGAGACCATGGACAGAGCCAACAGACAGATCAACGAAGCTGATGAGAACG TGGCGGTACCAGACCGGTGAGGATCGTGAAACCATGGACCGTGCCTCTCGTCAAATCAACGAGGACGATGAAACCT TGGAGGTTCCATACCGGTGAGGACAGAGAGACCATGGACAGAGCCAACAGACAGATTAACGAGGACGATGAGAACG TGGAGGTACCAGACCGGTGAGGACAGAGAGACCATGGACAGAGCTTCTAGACAAATCAACGAGAGCGATGAGAACG TGGCGGTTCCAGACCGGTGAGGACAGAGAGACCATGGACAGAGCCAACAGACAAATCAACGAGGATGACGAGAACG --------------------GATATGAGAGACCATGGACCGTGCTAGCCGCCAGATCGACGAGAACGACGAGCAGG TGGAGATTCCAAACTGGTGAAGATAGAGAAACCATGGACAGAGCTTCTAGACAAATCAACGAAGAAGATGAACAAA TGGCGGTTCCAATCTGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGAGTTATCAACGAAAACGATGCTGAAG TGGAGATTCCACACTGGTGAAGACAGAGAGACCATGGACAGAGCCTCTAGACAAATCAACGAGAGTGATGAGAACG TGGCGGTACCAGACCGGTGAAGATAGAGAAACCATGGATAGAGCTTCAAGACAAATTAACGAACAAGATGAACAAT TGGAGGTTCCAGTCCGGTGAAGATAGAGAAACCATGGACAGAGCTTCTAGACAAATTAACGAAGAAGATGAACAAA TGGCGGTACCAGTCTGGTGAGGACCGTGAGACCATGGACCGTGCCAACCGTCAGATCGATGAGAACGATGAGGCTG TGGCGGTACCAGTCCGGTGAAGATAGAGAAACCATGGACAGAGCTTCTAGACAAATCAACGAAAACGATGAAAACG TGGAGGTTCCACACTGGTGAAGATAGAGAAACCATGGACAGAGCTTCTAGACAAATTAACGAAAACGATGAAAACG TGGAGGTACCAATTCGGTGAAGATAGAGAAACTATGGTTCGTGCTTCAAGACAAATTAATGAAAATGATGAAGAAG TGGCGGTTCCACACTGGTGAAGATAGAGAAACCATGGACAGAGCTTCTAGACAGATCAACGAAGATGATGAAAAGG TGGAGGTTCCACACTGGTGAAGATAGAGAAACCATGGACAGAGCTTCTAGACAAATCAACGAAGAAGATGAACAAA TGGCGGTTCCAGTCTGGTGAGGACCGTGAGACTATGGACCGTGCCAACCGTCAAATCGATGAGAATGACGAGAAGG TGGCGATACCAAACCGGTGAAGATAGAGAAACTATGGATAGAGCTTCTAGACAAATTAACGAAAATGATGAACAGG TGGAGATTCCACACTGGTGAAGACAGAGAGACCATGGACAGAGCCTCTAGACAAATCAACGAGAGTGACGAGAACG TGGAGGTTCCACACTGGTGAAGACAGAGAGACAATGGACAGAGCCTCTAGACAAATCAACGAGAGTGACGAGAACG TGGAGGTACCAGACCGGTGAAGATAGAGAAACTATGGATAGAGCATCTAGACAAATCAACGAAGATGATGAGAATG TGGAGGTACCAATCCGGTGAAGATCGTGAGACTATGGACCGTGCTAACAGGAAGATTAACGAAGAGGACAAGCAGG TGGCGGTACCAGACTGGTGAAGATCGTGAGACTATGGACCGTGCTAACAGGAAGATTAACGAAGAGGACAAGCAGG TGGCGGTACCAGACTGGTGAAGATCGTGAAACCATGGACCGTGCCAACAGAAAGATCAATGAATCTGATAAGCAGG TGGAGGTACCAATCTGGTGAAGATAGAGAAACTATGGACAGAGCCTCCAGACAAATCAACGAAGATGATGAAACTT TGGAGGTACCAAACCGGTGAAGATAGAGAAACTATGGACAGAGCCTCCAGACAAATCAACGAAGATGATGAAACTT TGGAGGTTCCAAACTGGTGAAGATAGAGAAACTATGGACAGAGCTTCTAGACAAATCAACGAAGATGATGAAACTT TGGAGGTTCCAGACTGGTGAAGATAGAGAAACCATGGATAGAGCTTCTAGACAAGTTAACGAACAAGATGAAAACT TGGAGGTACCAGTCTGGTGAAGATAGAGAAACCATGGACAGAGCTTCTAGACAAATCAATGAAAGTGATGAAGAAG TGGAGGTTCCAAACCGGTGAAGATAGAGAAACTATGGACAGAGCTTCCAGACAAATCAACGAAAATGATGAACAAG TGGCGGTACCAGTCTGGTGAAGATAGAGAAACCATGGACAGAGCTTCCAGACAAGTTAACGAACAAGATGAAAACT TGGCGGTACCAATCTGGTGAAGATAGAGAAACCATGGATAGAGCTTCTAGACAAGTTAACGAACAAGATGAAAACT TGGCGGTTCCATTCTGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGACAAATCAACGAAGATGATGAAGCTG TGGAGGTTCCAAACTGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGACAAATCAACGAAGATGATGAAGCTG -GAAGGTTCCATTCCGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGACAAATCAACGAAGATGATGAAGCTG TGGAGGTTCCACACCGGTGAAGATAGAGAAACCATGGACAGAGCCAACAGACAAATCAACGAAGATGATGCTCAAG TGGAGGTTCCAGACCGGTGAAGATAGAGAAACTATGGATAGAGCTTCCAGACAAATCAACGAAAACGATGAACAAG TGGAGATTCCAAACTGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGAGTTATCAACGAAGATGATGCTGAAG TGGCGGTTCCAGACCGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGAGTTATCAACGAAAACGATGCTGAAG TGGAGGTACCAGACTGGTGAAGATAGAGAAACCATGGACAGGGCTAACAGAGTTATCAACGAAAACGATGCTGAAG TGGAGGTTCCAGACCGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGAGTTATCAACGAAAACGATGCTGAAG TGGCGGTTCCATACCGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGAGTTATCAACGAAAACGATGCTGAAG TGGAGGTACCAGTCTGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGAGTTATCAACGAAAACGATGCTGAAG TGGAGGTTCCAGACTGGTGAAGATAGAGAAACCATGGATAGAGCTAACAGACAAATTAATGAAAATGATGCTGAAG TGGCGGTTCCAGTCCGGTGAAGATAGAGAAACCATGGACAGAGCTTCAAGACAAATCAACGAGGCTGATGAGCAAA TGGAGGTTCCAGTCTGGTGAAGACAGAGAGACCATGGACAGAGCCAACAGAGTCATCAACGAGGAGGATGCTGAGT TGGCGGTTCCAGTCTGGTGAGGACAGAGAGACCATGGACAGAGCTAACAGAGTCATCAACGAGGGCGATGAGAATG TGGAGGTACCAAACCGGTGAAGACAGAGAAACCATGGACAGAGCTTCTAGACAAATCAACGAGAACGATGAGCAGG TGGAGGTTCCAAACTGGTGAAGATAGAGAAACTATGGATCGTGCTTCAAGACAAATTAATGAAAATGATGAAGAAG TGGCGGTTCCACACTGGTGAAGATAGAGAAACTATGGATCGTGCTTCAAGACAAATTAATGAAAATGATGAAGAAG TGGAGGTTCCAAACTGGTGAAGATAGAGAAACCATGGATCGTGCTTCCAGACAAATCAATGAAAATGATGAACAAG TGGAGGTTCCAGACTGGTGAAGATAGAGAAACCATGGATAGAGCATCTAGACAAATCAACGAAGATGATCAAAAAG TGGCGGTTCCAGACTGGTGAAGATAGAGAGACTATGGATAGAGCTTCTAGACAAATCAACGAGGAGGACGAGAGTG TGGAGGTTCCAAACTGGTGAAGATAGAGAAACCATGGACAGAGCTTCTAGACAAATCAACGAAAACGATGAAGAAG TGGAGGTTCCAATCCGGTGAAGATAGAGAAACCATGGACAGAGCTTCCAGACAAATTAACGAAAACGATGAACAAG TGGAGGTACCAGACTGGTGAGGACAGAGAGACCATGGACAGAGCTTCTAGACAAATCAACGAGAGCGATGAGAACG TGGAGGTTCCACTCTGGTGAAGATAGAGAAACCATGGACAGAGCTTCCAGACAAATCAACGAAAATGATGAAGAAG 111 6 Anhang Po BCD 862 Pp AB018536 Sb BCD 1256 Sb BCD 1392 Sb DSM 70412 Sc AB018539 Sc DSM 1333 Sd BCD 1257 Sd DSM 70487 Se MUCL 29838 Sp DSM 6580 Sp BCD 728 Td DSM 70607 Yl AB018537 Yl BCD 2003 Yl BCD 2556 Zb BCD 1424 Zbi DSM 70415 Zf DSM 70506 Zm DSM 6959 Zr ATCC 48230 Scho DSM 70573 Schp AB018538 Schp BCD 773 HS12/IV-IX Hb1f-5f Hb6f Hb7f Bd DSM 70745 Cra DSM 70197 Crc BCD 2578 Crc DSM 70022 Crf BCD 823 Crh DSM 70067 Crl BCD 824 Fn AF316889 Rg BCD 3530 Rm DSM 70408 Spj BCD 4982 Spj BCD 778 Spj DSM 70847 Trc DSM 70684 TGGAGGTTCCAGACTGGTGAGGACAGAGGGACCATGGACAGAGCTTCCAGACAGGTCACCGAGGAGGACGAGCAGA TGGAGATTCCAAACCGGTGAGGACCGTGAGACCATGGACCGTGCATCTAGACAAATCAACGAGAACGATGAGGAGG TGGAGGTTCCAAACTGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGACAAATTAACGAAGACGATGCTCAAG TGGCGGTTCCATACCGGTGAAGACAGAAAAACCATGGACAGAGCTAACAGAGTTATCAACGAAGATGATGCTGAAG TGGCGGTACCAGACTGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGACAAATTAACGAAGACGATGCTCAAG TGGAGATTCCAAACCGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGACAAATCAACGAAAACGATGCTGAAG TGGAGGTTCCAGTCCGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGACAAATCAACGAAAATGATGCTGAAG TGGCGGTACCAGTCCGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGACAAATCAACGAAAACGATGCTGAAG TGGAGGTTCCAGACTGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGACAAATCAACGAAAACGATGCTGAAG TGGAGGTTCCAGTCCGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGACAAATCAACGAAAACGATGCTGAAG TGGAGGTTCCAGACCGGTGAAGATAGAGAAACCATGGATAGAGCTAATAGGCAAATAAATGAAAATGATGCGGAAG TGGAGGTACCAGTCTGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGACAAATTAATGAAGACGATGCTCAAG TGGAGGTACCAGACCGGTGAAGACAGAGAAACCATGGACAGAGCTAACAGAGTTATCAACGAAGATGATGCTGAAG TGGCGATTCCAGACCGGTGAGGATCGAGAGACCATGGACCGAGCCAACCGACAGATCACCGACTCCGATGAGGCTG TGGCGGTACCAGACTGGTGAAGATCGAGAGACTATGGATCGAGCCAATCGACAGATCGATGAAAATGATGAGGAAG TGGCGGTACCAGACCGGTGAGGATCGAGAGACCATGGACCGAGCCAACCGACAGATCACCGACTCCGATGAGGCTG TGGCGGTACCAGACCGGTGAGGACAGAGAGACCATGGACAGAGCTAACAGACAAATCAACGAGAGTGATGAGCGGG TGGAGGTTCCAGACCGGTGAAGACAGAGAAACCATGGATAGAGCTAACAGACAGATTAATGAGAGTGACGAACAGG TGGCGGTTCCAGTCTGGTGAAGACAGAGAAACCATGGACAGAGCTAACAGACAAATCAACGAAAACGATGCTGAAG TGGAGGTTCCATACTGGTGAAGATAGAGAAACTATGGACAGAGCCAACAGACAAATCAACGAAGATGATGCTCAAG TGGAGGTTCCAGACTGGTGAAGATAGAGAAACCATGGACAGAGCTAACAGACAAATTAACGAAGATGATGCTCAAG TGGCGGTTCCACTCTGGTGAAGATTTGGAAGCTATGGACAAGGCCTCTCGTGTCATTAACGAAGCTGATGAGGAAG TGGCGTTTCCAATCTGGTGAAGATTTGGAGGCTATGGATAAGGCTTCTCGTGTCATCAGCGAGGCTGATGAGGAGG TGGCGGTACCACACTGGTGAAGATTTGGAGGCTATGGATAAGGCTTCTCGTGTCATCAGCGAGGCTGATGAGGAGG |--------------------| |-------------------|----------------------| |------------------| TGGCGATACCAAACCGGTGAAGATTTGGAAGAAATGAACAAAGCTACCCGAGTCATGACCGAAGAAGAGAAACAAA TGGCGATACCAGACCGGTGAGGATTTGGAGGAACTGCAAAAGGCGAACCGACAGTTGACCGAGGAAGAGATGCAAA TGGCGGTTCCATACCGGTGAGGACATTGAGGAGCTCTCCAAGGCCAACCGTGTCCTCTCCGAGGAGGAGAAGAAGA TGGCGATACCAGACGGGTGAGGACCTCGAGGAGCTCAACAAGGCCAACCGTGTCATGTCCGAGGAGGAGAAGAAGA TGGCGATACCAGACCGGTGAGGATCTCGAGGAGATGCACAAGGCCAACCGAGTCATGACCGAGGAGGAGAAGAAGA TGGCGATACCAGACCGGTGAGGACCTCGAGGAGGTGAACAAGGCCACCCGTGTCATGACCGAGGAGGAGAAGAAGA TGGCGATACCAGACTGGTGAGGATCTTGAGGAACTACACAAGGCCAACCGAACCATGTCTGCCGAGGAAGAGGCCA TGGCGATACCAGACCGGTGAGGACTTGGAGGAAATGCACAAGGCTAACCGGGTCATGACCGAGGCCGAGCTTGCCA TGGAGGTTCCAGACCGGTGAGGACATTGAGGAGCTCGCCAAGGCCAACCGCAAGCTCAGCGAGGAGGAGGAGAAGA TGGAGATACCAGACCGGTGAGGATCTCGAGGAGCTCAACAAGGAAGGCCGACAGATCACCGATGCCGAAAAGGAGA TGGCGATAC-AGACTGGTGAGGACCTCGAAGAGCTCGCGAAGGCCAACCGCACCCTCTCTGAGGAGGAGGAGAAGA TGGAGGTTCCAGACCGGTGAGGACATTGAGGAGCTCCACAAGGCCAACCGTGTCCTGTCCGAGGAGGAGGAGAAGA TGGAGGTTCCAGACCGGTGAGGACATTGAGGAGCTCCACAAGGCCAACCGTGTCCTGTCCGAGGAGGAGGAGAAGA TGGAGGTTCCAGACCGGTGAGGACCTCGAGGAGCTGAACAAGGCTACTCGTGTCCTTACCGAGGAGGAGAAGAAGA 77 80 | | Yff1-4,6,8 Ca AF038153 Ca ATCC 10231 Cb DSM 70034 Cc DSM 70136 Cd DSM 70042 Ce DSM70858 Cg BCD 8932 Cglae CBS 5691 Ch DSM 70624 Cim BCD 1062 Cint BCD 685 Ck BCD 689 Cll DSM 70102 Cm DSM 70638 Cmal AB018532 Cmal BCD 806 Cmel AB018533 Cmu DSM 70862 Cp ATCC 20384 Cr BCD 814 Cs BCD1054 Csan CBS 4261 Cso BCD 818 Ct BCD 819 Ctr ATCC 20326 Cv DSM 6956 Cvi DSM 70184 Cz AB018534 Cz BCD 690 De ATCC 20126 Dekb DSM 3429 90 | 100 | 110 | 130 140 150 | | | |-----------------------------ACATGAA------CAAGATTTTCAAAATTGAAGGTACACCAAGAAGAATTGCTGGTATTCACGCCAGAAGAAAGTT ACATGAA------CAAGATTTTCAAAATTGAAGGTACACCAAGAAGAATTGCTGGTATTCACGCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATTGAAGGTACTCCAAGAAGAATTGCCGGTATTCACTCCAGAAGAAAGTT ACATGAA------CAAGATCTTCAAGGTTGAGGGTTCCGAGCGTAGAATTGCCGGTACCCACGCCAGAAGAAAGTT CCATGAA------CAAGATATATAAGATTGAAGGCACTCAGCGACGTGTGGCCGGTGTTCATGCTCGAAGGAAGTT ACATGAA------GAAAATCTTCAAAGTTGAAGGTACACCAAGAAGAATTAAAGACATTATTGCCCGAAGAAAATT GTATGAA------GAAGATTTTCGAAATTGAAAACACTCCAAGAAGAGTTCAAGAAATCCATGCCAGAAGAAAATT ACATGAA------CAAGGTTTTCAAGATCGAAGGTACTCCAAGAAGAGTCCAAGGTATCCACGCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGGTCGAGGGTACCCCAAGAAGAGTTGCTGGTGTCCACTCTAGAAGAAAGTT CCATGAA------CAAAATCTTCAAGATTGAGGGTACCCCAAGAAGAATTCAAGGTATCCACGCCAGAAGAAAGTT CCATGAA------CAAGATCTTCAAGATTGAGGGTACCCCAAGAAGAATTGCTGGTATTCACGCTAGAAGAAAGTT CCATGAA------CAAGATCTTCAAGATTGAAGGTACCCCAAGAAGAGTTGCTGGTATTCACGCTAGAAGAAAGTT CCATGAA------CAAGATCTTCAAGATCGAGGGTACCCCAAGAAGAATTGCTGGTATTCACGGTAGAAGAAAGTT CCAAGAA------CAAGGTCTACAAGGTCGAGGGCACCTACCGCCGTGTGAACGAGGTTCTGTCCCGCCGTAAGTT ACATGAA------CAAAATCTTCAAAGTTGAAGGTACTCCAAGAAGAGTTGCTGGTATCCACGCCAGAAGAAAGTT CTGTGAA------CAAGATCTTCAAGATCGATGGTACCCCAAGAAGAATCGCTGGTATCCACGCTAGAAGAAAGTT CCATGAA------CAAGATCTTCAAGATCGAGGGTACTCCCAGAAGAATCCAAGGTATTCACGCCAGAAGAAAGTT CTATGAA------CAAGATCTTCTCAGTTGAAGGATCACCAAGAAAGATTGCTGGTATTCACTCTAGAAGAAAATT ATATGAA------CAAGATTTTCAAGATTGAAGGTACCCCAAGAAGAGTTGTTGGTATCCATTCTAGAAGAAAGTT CCATGAA------CAAGATCTACAAGATTGAGGGAACTCCCCGCTGTGTTGCCGGTGTTCATGCTCGTCGTAAGTT CTATGAA------CAAGATCTTCAAGGTTGAAGGTACCCCAAGAAGAGTCCAAGGTATTCACGCTAGAAGAAAGTT CTATGAA------CAAGATTTTCAAGGTTGAAGGTACTCCAAGAAGAATCCAAGGTATCCATGCTAGAAGAAAGTT GTATGAA------GAAAATCTTCAAAATTGAAGGTACTCCAAGACGTATTCATGAAATTCATGCTAGAAGGAAATT GAATGGA------AAAGATCTTCAAGATTGAAGGTTCTCCAAGAAGAGTTGCTGGCATTCACGCTAGAAGAAAATT ACATGAA------CAAGATCTTCAAAGTTGAAGGTACACCAAGAAGAGTTGCTGGTATCCACGCCAGAAGAAAGTT CTATGAA------CAAGATCTACAAGATCGAAGGTACTGAGCGTCGTGTGCAAGGTGTTCACTCTCGCCGGAAGTT CTATGAA------CAAAATTTTCAAGATTGAAGGCACTCCAAGAAGAATTCAAGGTATTCATTCTAGAAGAAAGTT CCATGAA------CAAGATCTTCAAGATCGAGGGTACTCCCAGAAGAATCCAAGGTATTCACGCCAGAAGAAAGTT CCATGAA------CAAGATTTTCAAGATCGAGGGTACTCCCAGAAGAATTCAAGGTATTCACGCCAGAAGAAAGTT CTATGAA------CAAAATCTTCAAGATTGAGGGTACCCCAAGAAGAGTCGCTGGTATCCATGCCAGAAGAAAGTT GTATGAA------CAAGATTTTCCACATTGAAGGTACCTCAAGGAGAATTGCCGGTATCCACTCTAGAAGAAAGTT 112 120 | 6 Anhang Dekb DSM 70726 Dekc DSM 70736 Dh BCD 3512 Dh BCD 589 Dm ATCC 11627 Ef BCD 3514 Ef DSM 70554 Gs DSM 3431 Hb BCD 859 Hb DSM 3505 Hg DSM 70285 Hu ATCC 9774 Hu BCD 3526 Hv DSM 70283 Io CBS 5147 Kl AB018535 Km BCD 2563 Km BCD 5186 Km BCD 811 Km DSM 70106 Km DSM 70792 Ku BCD 877 Le DSM 70320 Lt CBS 6340 Mp DSM 70321 Pa DSM 70277 Pan BCD 1082 Pan DSM 70783 Pc CBS 601 Pcar DSM 70392 Pf BCD 861 Pfe BCD 711 Pfe DSM 70090 Pg BCD 804 Pm DSM 70178 Po BCD 862 Pp AB018536 Sb BCD 1256 Sb BCD 1392 Sb DSM 70412 Sc AB018539 Sc DSM 1333 Sd BCD 1257 Sd DSM 70487 Se MUCL 29838 Sp DSM 6580 Sp BCD 728 Td DSM 70607 Yl AB018537 Yl BCD 2003 Yl BCD 2556 Zb BCD 1424 Zbi DSM 70415 Zf DSM 70506 Zm DSM 6959 Zr ATCC 48230 Scho DSM 70573 Schp AB018538 Schp BCD 773 Hb1f-5f Yff5 Bd DSM70745 Cra DSM70197 Crc BCD 2578 Crc DSM 70022 Crf BCD 823 Crh DSM 70067 Crl BCD 824 Fn AF316889 Rg BCD 3530 Rm DSM 70408 Spj BCD 4982 Spj BCD 778 Spj DSM 70847 Trc DSM 70684 GTATGAA------CAAGATTTTCCACATTGAAGGTACTTCAAGGAGAATTGCCGGTATCCACTCTAGAAGAAAGTT GTATGAA------TAAGATTTTCCATATTGAAGGTACTCCAAGAAGGATTGCTTCTATCAACTCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATTGAAGGTACTCCAAGAAGAATCGCTGGTATCCACGCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATTGAAGGTACTCCAAGAAGAATCGCTGGTATCCACGCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATTGAAGGTACTCCAAGAAGAATTGCTGGTATCCACGCTAGAAGAAAGTT CTATGAA------AAAGATTTTCAATGTTGAAGGTACCCCAAGAAGAATTGCCGGTATTCACTCCAGAAGAAAGTT GTATGAA------GAAACTTTTCAAGGTTGAAGGTACCGCTAGAAGAATTAAGGAAATCTTGGCTAGAAGAAAGTT GTATGAA------GAAGATCTTCAAGGTTGATTCTACTACCAGAAGAGTTAAAGAAATTTAGCCCAGAAGAAAATT CTATGAA------GAAGATTTTCACTGTTGAAGGTACCCCAAGAAGAATTGCTGGTATTCACTCCAGAAGAAAGTT CTATGAA------AAAGATTTTCAATGTTGAAGGTACCCCAAGAAGAATTGCCGGTATTCACTCCAGAAGAAAGTT GTATGAA------GAAGATCTTCGAAATTGAAAACACTCCAAGAAGAATTCAAGAAATTCACGCTAGAAGAAAATT GTATGAA------GAAGATCTTTGAAATTGAAAACACTCCAAGAAGAATTCAAGAAATTCACGCTAGAAGAAAATT GTATGAA------GAAGATCTTCGAAATTGAAAACACTCCAAGAAGAATTCAAGAAATTCACGCTAGAAGAAAATT GTATGCA------AAAAATTTTCAAGATTGAAGGTACTCCAAGAAGAATCAACGAAATTTTGGCCAGAAGAAAATT CTATGAA------CAAGATTTTCAAGATTGAAGGTACTCCAAGAAGAATTGCAGGTATTCACTCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATCGACGGTACTCCAAGAAGAATTGCTGGTATCCACGCTAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATCGATGGTACCCCAAGAAGAATCGCTGGTATCCACGCTAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATCGATGGTACCCCAAGAAGAGTCGCTGGTATCCACGCTAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATCGAAGGTACCCCAAGAAGAATCGCTGGTATCCACGCTAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATCGATGGTACCCCAAGAAGAATCGCTGGTATCCACGCTAGAAGAAGGTT CTATGAA------CAAGATCTTCAAGATCGATGGTACCCCAAGAAGAATCGCTGGTATCCACGCTAGAAGAAAGTT TTATGAA------CAAGATCTTCAAGATTGAAGGTACTCCAAGAAGAATTCAAGAAATTTTAGCTAGAAGAAAGTT ACATGAA------CAAGATCTTCAAGGTTGAAGGTACCCCAAGAAGAATTGCTGGTATTCACGCAAGAAGAAAGTT CCATGAA------CAAGATCTTCAAGATCGAGGGTACCCCAAGAAGAATTCAGGGCATCCACGCCAGAAGAAAGTT CTATGAA------CAAAATTTTCAAGATCGAGGGCACTCCAAGAAGAATTGCTGGTATCCACTCTAGAAGAAAGTT CCATGAA------CAAGATCTTCAAGATTGATGGTACCCCAAGAAGAATTCAAGGTATTCACGCTAGACGGAAGTT GTATGAA------GAAAATCTTCAAAATTGAAGGTACTCCAAGACGTATTCATGAAATTCATGCTAGAAGAAAATT GTATGAA------GAAAATCTTCAAAATTGAAGGTACTCCAAGACGTATTCATGAAATTCATGCTAGAAGAAAATT CTATGAA------CAAAATTTTCAAGATTGAAGGTACCCCAAGACGTATTGCTGGTATCCACGCTAGAAGAAAATT ATATGAA------TAAGATTTTCAAGGTTGAGGGTACCGAAAGAAGAATTGCCGGAATTCATGCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATTGAAGGTACTCCAAGAAGAATCGCTGGTATTCACGCTAGAAGAAAGTT CTATGAA------CAAGATCTATAAGATCGAAGGTACTCCAAGAAGAATTGCAGGTATTCACGCTAGACGGAAGTT CTATGAA------CAAGATCTTCAGGATTGAAGGTTCTCCAAGAAGAATTGCTGGTATCCACTCCAGAAGAAAGTT CCATGAA------CAAGATCTTCAAGATTGAAGGTACCCCAAGAAGAGTTGCTGGTATTCACGCTAGAAGAAAGTT CTATGAA------CAAGATCTATAAGATCGAAGGTACCCCAAGAAGAATTAATGGTATTCACGCTAGACGGAAGTT ACATGAA------CAAGATCTTCAAGATCGAGGGTACCCCAAGAAGAGTTGTTGGTATCCACGCCAGAAGAAAGTT CCATGAA------CAAGATCTTCAAGATCGATGGTACTCCAAGAAGAATCGCTGAGATTCACTCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATCGAAGGTACCCCAAGAAGAATCGCTGGTATCCACTCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATCGAAGGTACTCCAAGAAGAATCCAAGAGATTCACGCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATCGAAGGTACCCCAAGAAGAATCGCTGGTATCCACTCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATTGAAGGTACCCCTAGAAGAATTGCCGGTATCCACTCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATTGAAGGTACCCCTAGAAGAATTGCCGGTATCCACTCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATTGAAGGTACCCCTAGAAGAATTGCCGGTATCCACTCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATTGAAGGTACCCCTAGAAGAATTGCCGGTATCCACTCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATTGAAGGTACCCCTAGAAGAATTGCCGGTATCCACTCCAGAAGAAAGTT CCATGAA------CAAAATCTTCAAAATCGAAGGAACTCCACGAAGGATTGCAGGAGTTCACTCAAGAAGAAAATT CTATGAA------CAAGATCTTCAAGATCGAAGGTACTCCAAGAAGAATCGCTGGTATCCACTCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATCGGAGGTACTCCAAGAAGAATCCAAGAGATTCACGCCAGAAGAAAGTT CCATGAA------CAAGATCTACAAGATCGAGGGCACTCCCCGACGAGTTGCTGAGGTCCACGCCCGACGAAAGTT CCATGAA------CAAGATATATAAGATTGGAGGCACTCAGCGACGTGTGGCCGGTGTTCATGCTCGAAGGAAGTT CCATGAA------CAAGATCTGCAAGATCGAGGGCGCCCCCCGACGAGTTGCTGGTGTTCACGCCCGACGAAAGTT CCATGAA------CAAGATCTTCAAGATCGATGGTACTCCAAGAAGAATTGCTGGTATTCACTCCAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATCGACGGTACTCCAAGAAGAATCGCTGGTATCCACTCTAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATTGACGGTACCCCAAGAAGAATTGCTGGTATCCACGCTAGAAGAAAGTT CTATGAA------CAAAATCTTCAAGATTGAAGGTACTCCAAGAAGAATTGCTGGTATTCACTCTAGAAGAAAGTT CTATGAA------CAAGATCTTCAAGATCGATGGTACCCCAAGAAGAATTGCTGGTATCCACTCCAGAAGAAAGTT CCATGAAGAA---CAAGATCTTCAAGATTGAGGGTACTCCTCGTAAGATTTTGGGTATTCACAGCCGTAGAAAGCT CTATGAAGAA---CAAGATCTTCAAGATTGAGGGAACTCAACGTAAGATTTTGGGTATCCACAGCCGTCGTAAGCT CTATGAAGAA---CAAGATCTTCAAGATTGAGGGAACTCAACGTAAGATTTTGGGTATCCACAGCCGTCGTAAGCT ----| |------------------------AGATGAAGGAAGGTGCCGTCGTTGTCAAAGAAGGTGTCAAACGATTGATAGACGAACTTGTTGCCAGAAAGAAATT AGATGAAGGAAGGAGGCAACGTCATCATTGAAGGTGCCAAGCGAGTCATTGACGAACTTGTCGCCCGAAAGAAGCT AGATGGCCGAGGGTGCCACCGTCGTCGTTGAGGGTGTGAAGCGCATCATTGACGAGCTCGTTGCCCGTAAGAAGCT AGATGGCCGAGGGAGCAAACGTCATCAAGGACGGCGTGAAGCGTATCATTGACGAGCTTGTCGCACGTAAGAAGCT AGATGGCCGAGGGTGCCACCTTCATGAAGGAGGGTGTCAAGCGAATCATCGACGAGATTGTTGCCCGAAAGAAGCT AGATGGCCGAGGGTGCCACCTTTGTCAAGGAGGGCGTCAAGCGCATCATTGACGAGCTTGTCGGCCGTAAGAAGCT AGATGAAGGAAGGAGCCAACGTTATCAAGGAAGGTGTCAAGCGAATCATTGATGAGCTTATCGCCCGAAAGAAGCT AGATGAAGGAGGGTGCCACCGTTATCAAGGACGGTGTCAAGCGAATCATCGATGAGCTTGTTGCTAGAAAGAAGCT GGATGAAGGACGGCGCCAACGTCGTCGTCGAGGGCGTCAAGCGCACCATCGACGACATTGTCGCCCGCAAGAAGCT AGATGAAGCAGGGTGAAGTCGTCCTCGTTGAAGGTGTCAAGCGCATCATCGATGAGATCGTTGGACGAAAGAAGCT AGATGAAGGAGGATTCGACCGTCGTCGTTGAGGGCGTCAAGCGCACCATCGACGAGGTTATCAACCGCAAGAAGCT AGATGAAAGAGGGTGCGACCGTTGTCGTTGAGGGTGTCAAGCGCACCATTGACGAGATCATCAGCCGCAAGAAGCT AGATGAAAGAGGGTGCGACCGTTGTCGTCGAGGGTGTCAAGCGCACCATTGACGAGATCATCAACCGTAAGAAGCT AGATGGCCGAGGGTGCTATCGTCGTCAAGGAGGGCGTCAAGCGCACCATTGACGAGCTCGTTGCCCGTAAGAAGCT 113 6 Anhang Yff1-4,6,8 Yfr1-4,8 Ca AF038153 Ca ATCC 10231 Cb DSM 70034 Cc DSM 70136 Cd DSM 70042 Ce DSM70858 Cg BCD 8932 Cglae CBS 5691 Ch DSM 70624 Cim BCD 1062 Cint BCD 685 Ck BCD 689 Cll DSM 70102 Cm DSM 70638 Cmal AB018532 Cmal BCD 806 Cmel AB018533 Cmu DSM 70862 Cp ATCC 20384 Cr BCD 814 Cs BCD1054 Csan CBS 4261 Cso BCD 818 Ct BCD 819 Ctr ATCC 20326 Cv DSM 6956 Cvi DSM 70184 Cz AB018534 Cz BCD 690 De ATCC 20126 Dekb DSM 3429 Dekb DSM 70726 Dekc DSM 70736 Dh BCD 3512 Dh BCD 589 Dm ATCC 11627 Ef BCD 3514 Ef DSM 70554 Gs DSM 3431 Hb BCD 859 Hb DSM 3505 Hg DSM 70285 Hu ATCC 9774 Hu BCD 3526 Hv DSM 70283 Io CBS 5147 Kl AB018535 Km BCD 2563 Km BCD 5186 Km BCD 811 Km DSM 70106 Km DSM 70792 Ku BCD 877 Le DSM 70320 Lt CBS 6340 Mp DSM 70321 Pa DSM 70277 Pan BCD 1082 Pan DSM 70783 Pc CBS 601 Pcar DSM 70392 Pf BCD 861 Pfe BCD 711 Pfe DSM 70090 Pg BCD 804 Pm DSM 70178 Po BCD 862 Pp AB018536 Sb BCD 1256 Sb BCD 1392 Sb DSM 70412 Sc AB018539 Sc DSM 1333 Sd BCD 1257 153 160 170 180 190 200 210 220 228 |------|---------|---------|---------|---------|---------|---------|-------| ------| |------------------------------------| CAAGAACTCTTATGAATATGAAATTTCTTGGATGTTGGGTGAAAACATTGGTATGAAGAATGAAAGATGGGTACCA CAAGAACTCTTATGAATATGAAATTTCTTGGATGTTGGGTGAAAACATTGGTATGAAGAATGAAAGATGGGTACCA CAAGAACACCTACGAATATGAATGTTCTTTTACTTTAGGTGAAAACATTGGTATGAAATCTGAAAGATGGGTCCCA CAAGAACTCTTACGAGTACGAGATCTCCTGGATGTTGGGTGAGAACGTCGGCATGAAGTCCGAGAGATGGGTCCCC CAAGAACTCTTATGAATACGAATGTTCATTCTTGCTTGGTGAAAACCTTGGCATGAAATCTGAGCGATGGATTCAA CAAGAATTCTTATGAATATGAAATTGAATGGTCTTTAGGTGAAAACATTGGTATGAAGAATGAAAGATGGATTAAC CAAGAACTCTTATGAATATGAATGTTCTTTCTTATTAGGTGAAAACATTGGTATGAAATCTGAAAGATGGGTTCCA CAAGAACTCTTACGAATATGAAATTTCTTGGATATCGGGAGACAATGTTGGTATGAAATCTGAAAGATGGGTACCA CAAGAACACTTACGAGTACGAGGTTTCTTGGAACCTTGGTGAGAACATTGGCATGAAGAACGAGAGATGGGTTCCA CAAGAACACCTACGAGTACGAGTGTTCTTTCATGCTTGGAGAGAACATCGGTATGAAGAACGAGAGATGGGTTCCT CAAGAACTCTTACGAGTACGAGTGTTCTTTCACCTTGGGTGAGAACATTGGTATGAAGAACGAGAGATGGGTTCCA CAAGAACTCTTACGAGTACGAATGTTCTTGGCTCTTGGGTGAGAACATTGGCATGAAGAACGAGAGATGGGTTCCT CAAGAACACTTACGAGTACGAGTGTTCTTTCTTGTTGGGAGAGAACATCGGCATGAAGAACGAGAGATGGGTTCCA CAAGAACTCTTACGAGTACGAGGTCTCGTACCTGCTCGGAGACAACATTGGTCTCAAGAGCGAGCGCTGGGTCCCC CAAGAACTCTTACGAGTATGAAATTTCTTGGTTGTTGGGTGAAAACATTGGTATGAAGAACGAAAGATGGGTCCCA CAAGAACACCTACGAGTACGAATGTTCCTTCCTGTTGGGTGAAAACATCGGTATGAAGTCTGAAAGATGGGTTCCA CAAGAACTCTTACGAGTACGAATGTTCTTGGATGTTGGGTGAGAACATTGGCATGAAGAATGAGAGATGGGTTCCT CAAAAATTCTTATGAATATGAAATTTCATGGATGTTGGGTGACAACATTGGTATGAAATCTGAAAGATGGGTTGCT TAAGAACTCTTATGAGTATGAAGTTTCATGGTCTTTGGGTGAAAACGTTGGTATGAAGAATGAAAGATGGGTCCCA CAAGAACTCCTACGAGTACGAGTGTTCTTTCCTGCTCGGTGAGAACATTGGTCTCAAGTCTGAGCGCTGGATTCCC CAAGAACTCTTACGAATACGAATGTTCTTGGATGTTGGGTGAAAACATTGGTATGAAGAACGAAAGATGGGTCCCA CAAGAACTCTTACGAATACGAATGTTCTTGGATGTTAGGTGAAAACATTGGTATGAAGAACGAAAGATGGGTTGCT CAAGAACTCTTATGAATATGAATGTTCTTCCTTATTAGGTGAAAATGTTGGTATGAGGAATGAAAGATGGGTTCCA CAAGAACTCTTACGAGTATGAATGTTCTTGGACTTTGGGTGAAAACTTGGGTATGAAATCTGAAAGATGGGTTCCA CAAGAACTCTTACGAGTATGAAATTCCTTGGTTGTTGGGTGAAAACATTGGTATGAAGAACGAAAGATGGGTCCCA CAAGAACTCTTATGAGTACGAGTGCTCATTCTATCTAGGTGAGAACGTTGGTCTGAAGAGCGAGCGCTGGACGCCC TAAAAACACTTATGAATATGAATGTTCTTTCACATTAGGTGAAAACATCGGTATGAAATCTGAAAGATGGGTTCCA CAAGAACTCTTACGAGTACGAATGTTCTTGGATGTTGGGTGAGAACATTGGCATGAAGAATGAGAGATGGGTTCCT CAAGAACTCTTACGAGTACGAATGTTCTTGGATGTTGGGTGAGAACATTGGCATGAAGAACGAGAGATGGGTTCCT TAAGAACACCTACGAGTACGAATGTTCTTGGTTATTAGGTGAAAACATTGGAATGAAGAATGAAAGATGGGTTCCA CAAGAACACGTACGAGTACGAGTGTTCGTTCTTGCTTGGTGAGAACGTTGGTATGAAGAGTGAGAGATGGACTCCA CAAGAACACGTATGAGTACGAGTGTTCGTTCTTGCTTGGTGAGAACGTTGGTATGAAGAGTGAGAGATGGACTCCA CAAGAACACTTACGAATACGAGTGTTCGTTCTTGCTTGGTGAAAATGTTGGTATGAAGAAGGAGAAGTGGACTCCA CAAGAACTCTTACGAGTATGAATGTTCTTGGATGTTGGGTGAAAACATCGGTATGAAGAACGAAAGATGGGTCCCA CAAGAACTCTTACGAGTATGAATGTTCTTGGATGTTGGGTGAAAACATCGGTATGAAGAACGAAAGATGGGTCCCA CAAGAACTCTTACGAATATGAATGTTCTTGGTTCTTAGGTGAAAACATCGGTATGAAAAACGAAAGATGGGTTCCA CAAAAACTCTTATGAATATGAAATTTCTTGGTTATTAGGTGATAACGTTGGTATGAAGAACGAAAGATGGGTTCCA CAAGAACTCTTACGAATATGAAATCAGTTGGTACTTGGTTGACAACCCAGGTATGAAGAACGAAAGACAAGTTCCA CAAGAACTCTTATGAATATGAAATTAGTTGGTATTTAGTTGAAAACCCAGGTATGAAGAATGAAAGAGAAGTTCCA CAAAAACTCTTACGAATATGAAATTTCTTGGATGTTGGGCGACAATGTCGGTATGAAATCTGAAAGATGGGTCCCA CAAAAACTCTTATGAATATGAAATTTCTTGGTTATTAGGTGATAACGTTGGTATGAAGAACGAAAGATGGGTTCCA CAAGAACTCTTACGAATACGAATGTTCTTTCTTATTAGGTGAAAACATCGGTATGAAATCTGAAAGATGGGTCCCA CAAGAACTCTTACGAATACGAATGTTCTTTCTTATTAGGTGAAAACATCGGTATGAAATCTGAAAGATGGGTCCCA CAAGAACTCTTACGAATACGAATGTTCTTTCTTATTAGGTGAAAACATCGGTATGAAATCTGAAAGATGGGTCCCA CAAAAACTCTTACGAATATGAATGTTCCTTCTTCTTGGGTGAAAACATCGGTATGAAATCTGAAAGATGGGTTCCA CAAGAACACTTACGAATATGAATGTTCTTTCTTATTAGGTGAAAACATTGGTATGAAGTCTGAAAGATGGGTTCCA CAAGAACACCTACGAATACGAATGTTCCTTCTTGTTAGGTGAAAACATCGGTATGAAGTCTGAAAGATGGGTTCCA CAAGAACACCTACGAGTACGAATGTTCCTTCTTGTTGGGTGAAAACATCGGTATGAAGTCTGAAAGATGGGTTCCA CAAGAACATCTACGAGTACGAATGTTCCTTCTTGTTGGGTGAAAACATCGGTATGAAGTCTGAAAGATGGGTTCCA CAAGAACACCTACGAGTACGAATGTTCCTTCTTGTTGGGTGAAAACATCGGTATGAAGTCTGAAAGATGGGTTCCA CAAGAACACCTACGAGTACGAATGTTCCTTCTTGTTGGGTGAAAACATCGGTATGAAGTCTGAAAGATGGGTTCCA CAAGAACACCTACGAGTACGAATGTTCCTTCTTGTTGGGTGAAAACATCGGTATGAAGTCTGAAAGATGGGTTCCA TAAGAATACTTATGAATATGAATGTTCTTTCTACTTAGGTGAAAACATTGGTATGAAATCTGAAAGATGGGTTCCA TAAGAACTCTTATGAGTATGAGATTTCATGGACTTTGGGTGAAAACGTTGGTATGAAGAATGAGAGATGGGTTCCA CAAGAACTCTTACGAGTACGAGTGTTCTTTCTTGTTGGGTGAGAACATTGGTATGAAGTCTGAGAGATGGGTTCCA CAAGAACTCTTATGAGTACGAGTGTTCTTTCACCTTGGGTGAGAACATTGGCATGAAGAATGGGAGATGGGTCCAG CAAGAACACTTATGAGTATGAGTGTTCTTTCCTGTTGGGTGAGAACGTTGGTATGAAATCCGAGAGATGGGTTCCA CAAGAACTCTTATGAATATGAATGTTCTTTCTTATTAGGTGAAAATGTTGGTATGAAGAATGAAAGATGGGTTCCA CAAGAACTCTTATGAATATGAATGTTCTTTCTTATTAGGTGAAAATGTTGGTATGAAGAATGAAAGATGGGTTCCA CAAAAACACTTACGAATATGAATGTTCTTTCACTTTAGGTGAAAACATTGGTATGAAGAATGGAAGATGGGTTCCA TAAAAACTCTTACGAATATGAAATCTCCTGGATGTTGGGAGAAAACATTGGTATGAAGAATGAAAGATGGGTTGCA CAAGAACTCTTACGAGTACGAATGTTCTTGGTTATTGGGTGAGAACATCGACATGAAGAACGAGAGATGGGTTCCA CAAGAACACATACGAATATGAATGTTCCTTCTTGTTGGGTGAAAACATTGGTATGAAGTCTGAAAGATGGGTTCCA CAAGAACACCTACGAATATGGATGTTCTTTCCTTTTGGGTGACAACATCGGTATGAAGTCTGAAAGATGGGTTCCT CAAGAACTCTTACGAGTACGAATGTTCTTGGCTCTTGGGTGAGAACATTGGCATGAAGAACGAGAGATGGGTTCCT CAAGAACACTTACGAGTATGAATGTTCTTTCTTCTTAGGTGAAAACATTGGTATGAAGTCTGAAAGATGGGTTCCA CAAGAACTCTTACGAGTACGAAGTCTCCTGGGCTTTGGGTGAGAACATCGGCATGAAGAACGAGAGATGGGTTAAC CAAGAACTCTTACGAGTACGAGTGTTCGTTCTTGCTGGGTGAGAACATTGGTATGAAGTCTGAGAGATGGGTTCCA CAAGAACACTTACGAATATGAATGTTCTTTCATGTTGGGTGAAAACATTGGTATGAAATCTGAAAGATGGGTTCCA CAAGAACACCTACGAATACGAATGTTCTTTCCTATTGGGTGAAAACATCGGTATGAAATCCGAGAGATGGGTTCCA CAAGAACACTTACGAATATGAATGTTCTTTCATGTTGGGTGAAAACATTGGTATGAAATCTGAAAGATGGGTTCCA CAAGAACACTTACGAATATGAATGTTCTTTCTTATTGGGTGAAAACATTGGTATGAAATCTGAAAGATGGGTTCCA CAAGAACACTTACGAATATGAATGTTCTTTCTTATTGGGTGAAAACATTGGTATGAAATCTGAAAGATGGGTTCCA CAAGAACACTTACGAATATGAATGTTCTTTCTTATTGGGTGAAAACATTGGTATGAAATCTGAAAGATGGGTTCCA 114 6 Anhang Sd DSM 70487 Se MUCL 29838 Sp DSM 6580 Sp BCD 728 Td DSM 70607 Yl AB018537 Yl BCD 2003 Yl BCD 2556 Zb BCD 1424 Zbi DSM 70415 Zf DSM 70506 Zm DSM 6959 Zr ATCC 48230 Scho DSM 70573 Schp AB018538 Schp BCD 773 Yff5 Yfr5,7 Bd DSM70745 Cra DSM70197 Crc BCD 2578 Crc DSM 70022 Crf BCD 823 Crh DSM 70067 Crl BCD 824 Fn AF316889 Rg BCD 3530 Rm DSM 70408 Spj BCD 4982 Spj BCD 778 Spj DSM 70847 Trc DSM 70684 CAAGAACACTTACGAATATGAATGTTCTTTCTTATTGGGTGAAAACATTGGTATGAAATCTGAAAGATGGGTTCCA CAAGAACACTTACGAATATGAATGTTCTTTCTTATTGGGTGAAAACATTGGTATGAAATCTGAAAGATGGGTTCCA CAAGAACACATACGAATACGAGTGCTCTTTCTTCTTAGGCGAAAACATTGGCATGAAGTCCGAGAGATGGGTCCCG CAAGAACACTTACGAATATGAATGTTCTTTCATGTTGGGTGAAAACATTGGTATGAAATCTGAAAGATGGGTTCCA CAAGAACACCTACGAATACGAATGTTCTTTCCTATTGGGTGAAAACATTGGTATGAAATCCGAGAGATGGGTTCCA CAAGAACTCTTACGAGTACGAGTGTTCTTTCCTGCTCGGAGAGAACCTGGGCATGAAGTCCGAGAAGTGGATCCCC CAAGAACTCTTATGAATACGAATGTTCATTCTTGCTTGGTGAAAACCTTGGCATGAAATCTGAGCGATGGATTCAA CAAGAACTCTTACGAGTACGAGTGTTCTTTCCTGCTCGGTGAGAACCCTGGCATGAAGTCCGAGAAGTGGATCCCC CAAGAACACTTACGAATACGAATGTTCTTTCTTGCTAGGTGAGAACATTGGTATGAAATCCGAGAGATGGGTGCCT CAAGAACACTTACGAGTACGAATGTTCCTTCTTGCTAGGTGAGAACATCGGTATGAAATCCGAGAGATGGGTTCCA CAAGAACACTTACGAATATGAATGTTCTTTCTTATTAGGTGAAAACATCGGCATGAAATCAGAAAGATGGGTTCCA CAAGAACACTTACGAATATGAATGTTCCTTTTTATTAGGTGAAAACATCGGTATGAAATCTGAAAGATGGGTTCCA CAAGAACTCTTACGAGTACGAATGTTCTTTCTTGTTGGGTGAAAACATCGGTATGAAATCTGAAAGATGGGTTCCA TAAGAACTCTTACGAGTATGAATGTTCTTTCACTGTTGGTGAGAACATTGGTATGAAGAGTGAACGCTGGGTTCCC CAAGAACTCTTATGAGTATGAGTGCTCTTTCCTCGTCGGTGAGAACATTGGCATGAAGAGTGAGCGCTGGGTTCCT CAAGAACTCTTATGAGTATGAGTGCTCTTTCCTCGTCGGTGAGAACATTGGCATGAAGAGTGAGCGCTGGGTTCCT --------| |-----------------------GAAGCAATCGTACGAGTACGAAGTTTCATTC------------------------------AA-----AGGT---CAAGCAGTCGTACGAGTACGAAATCTCGTTC------------------------------AA-----GGGC---CAAGCAGTCTTACGAGTACGAGGTCTCGTTC------------------------------AA-----GGGC---CAAGCAGTCGTACGAGTACGAGGTGTCCTTC------------------------------AA-----GGGC---GAAGCAATCTTACGAGTACGAGGTTTCGTTC------------------------------AA-----GGGA---GAAGCAGTCTTACGAGTACGAGGTCTCGTTC------------------------------AA-----GGGC---CAAGCAGTCTTACGAATACGAAATCTCTTTC------------------------------AA-----GGGT---CAAGCAGTCCTACGAGTACGAGGTATCCTTC------------------------------AA-----GGGT---CAAGCAGTCGTTCGAGTACGAGGTCACCTTC------------------------------AA-----GGGC---GAAGCAATCTTACGAGTACGAGCTATCCTTC------------------------------AA-----GGCT---CAAGCAGTCGTTCGAGTACGAGGTCTCGTTC------------------------------AA-----GGGT---CAAGCAGTCGTTCGAGTACGAGACTACCTTC------------------------------AA-----GGGT---CAAGCAGTCGTTCGAGTACGAGACTACCTTC------------------------------AA-----GGGT---CAAGCAGTCTTACGAGTACGAGGTTTCGTTC------------------------------AA-----GGGC---- Ca AF038153 Ca ATCC 10231 Cb DSM 70034 Cc DSM 70136 Cd DSM 70042 Ce DSM70858 Cg BCD 8932 Cglae CBS 5691 Ch DSM 70624 Cim BCD 1062 Cint BCD 685 Ck BCD 689 Cll DSM 70102 Cm DSM 70638 Cmal AB018532 Cmal BCD 806 Cmel AB018533 Cmu DSM 70862 Cp ATCC 20384 Cr BCD 814 Cs BCD1054 Csan CBS 4261 Cso BCD 818 Ct BCD 819 Ctr ATCC 20326 Cv DSM 6956 Cvi DSM 70184 Cz AB018534 Cz BCD 690 De ATCC 20126 Dekb DSM 3429 Dekb DSM 70726 Dekc DSM 70736 Dh BCD 3512 Dh BCD 589 Dm ATCC 11627 Ef BCD 3514 Ef DSM 70554 Gs DSM 3431 Hb BCD 859 Hb DSM 3505 Hg DSM 70285 229 240 250 260 270 280 290 300 304 |----------|---------|---------|---------|---------|---------|---------|---| ATGATGTCTGTTGACAACACTTGGTTGCCAAGAGGTGAATTGATGGAAACTCACGCC---AAGTTGGTTGCTGAAG ATGATGTCTGTTGACAACACTTGGTTGCCAAGAGGTGAATTGATGGAAACTCACGCC---AAGTTGGTTGCTGAAG ATGATGTCTGTTGATAACGCTTGGTTACCAAGAGGTGAATTAGTTGAATCACATTCC---AAGATGGTTGCTGAAG ATGATGTCTGTTGACAACACCTGGTTGCCCAGAGGTGAGTTGATGGAGACTCACGCC---AAGTTGGTCGCCGAGG ATGTCCTCTGTTGACAATGCATGGATTTCGCGATCTGAGTTGGTTGAATCTCACGCC---AAGTTGGTTGCTGAGG ATGATGTCTGCTGATAACACATGGTTACCAAGAGGTGAATTAGTTGAAACTCACTCC---AAGATGGTTAGTGAAG ATGTCTTCTGTTGACAATGCTTGGATTCCAAGAAGTGAATTAGTTGAATCTCATGCT---AAGTTGGTTGCTGAAG ATGATGTCTGTCGACAACACTTGGTTGCCAAGAGGTGAATTGATGGAAACCCACGCC---AAGATGGTTGCTGAAG ATGATGTCTGTTGACAACACCTGGTTGCCAAGAGGTGAGTTGATCGAGACTCACTCC---AAGTTGGTCGCTGAGG ATGATGTCTGTCGACAACGCTTGGTTGCCACGTGGTGAAATCACTGAATCTCACGGT---AAGATGGTTGCTGAGG ATGATGTCCGTTGACAACGCTTGGTTGCCAAGAGGTGAGTTGATCGAGACTCACTCC---AAGTTGGTTGCTGAGG ATGATGTCTGTTGACAACGCTTGGTTGCCAAGAGGTGAATTGATGGAGACCCACTCC---AAGATGGTTGCTGAGG ATGATGTCTGTTGACAACGCTTGGTTGCCAAGAGGTGAGTTGGTTGAGACTCACTCC---AAGATGGTTGCTGAAG ATGTCGTCTGTCGACAACGGCTGGATCCCGCGTAACGAGCTTATGGAGTCGCACGCC---AAGGACATTGCTGAGG ATGATGTCTGTTGACAACACTTGGTTGCCAAGAGGTGAATTGATGGAAACTCACGCC---AAATTGGTTGCTGAAG ATGATGTCTGTTGACAACGCTTGGTTGCCAAGAGGTGAATTGGTCGAATCTCACTCT---AAGATGGTTGCTGAAG ATGATGTCCGTCGACAACACTTGGTTGCCAAGAAGTGAGTTGATGGAGACCCACTCC---AAGTTGGTTGCTGAGG ATGATGTCAGTTGACAACACTTGGTTACCAAGAGGTGAATTAATGGAAACTCACTCC---AAGATGGTTGCTGAAG ATGATGTCTGTTGATAACACCTGGTTGCCAAGAGGTGAATTGATGGAAACTCATGCT---AAATTGGTTGCTGAAG ATGTCCTCTGTCGACAACGCATGGATTCCTCGTTCTGAGCTTGTTGAGTCTCATGCC---AAGCTGGTTGCTGTGG ATGATGTCTGTTGACAACACTTGGTTGCCAAGAGGTGAATTAATGGAAACCCACTCT---AAGTTGGTTGCTGAAG ATGATGTCTGTTGATAACACTTGGTTACCAAGAGGTGAATTAATGGAAACTCACTCT---AAGTTAGTCGCTGAAG ATGATGTCTGTTGATAACGCTTGGTTACCAAGAGGTGAATTGGTTGAAACTCATTCC---AAATTGGTTGCTGAAG ATGATGTCTGTTGACAACGCTTGGTTGCCAAGAGGTGAATTAATGGAAACTCACTCC---AAGATGGTTGCCTAAG ATGATGTCTGTTGACAACACTTGGTTGCCAAGAGGTGAATTGATGGAAACTCACGCC---AAATTGGTTGCTGAAG ATGTCTTCGGTTGACAATGCTTGGATCCCTCGTAGCGAGCTTATGGAATCGCACGCT---AAGCTTGTCTCAGAGG ATGCTTTCTGTTGATAACGCTTGGTTACCAAGAGGTGAATTGGTTGAATCTCATTCC---AAGATGGTTGCCGAAG ATGATGTCCGTCGACAACACTTGGTTGCCAAGAGGTGAGTTGATGGAGACCCACTCC---AAGTTGGTTGCTGAGG ATGATGTCCGTCGACAACGCTTGGTTGCCAAGAGGTGAGTTGATGGAGACCCACTCC---AAGTTGGTTGCCGAGG ATGATGTCCGTTGATAACACTTGGTTACCAAGAGGTGAGCTCATGGAAACACACTCC---AAGATGGTTGCTGAAG ATGTCTTCGGTCGACAACGCATGGATTCCAAGAGGTGAATTGGTTGAGAGTCACTCC---AAGATGGTTGCTGAAG ATGTCTTCGGTCGACAACGCATGGATTCCAAGAGGTGAATTGGTTGAGAGTCACTCC---AAGATGGTTGCTGAAG ATGTCTTCTGTTGACAATGCTTGGATTCCAAGAGGTGACTTGATTGAGACTCACGGT---AAGATGGTCGCTGAGG ATGATGTCTGTTGATAACGCTTGGTTACCAAGAGGTGAAATCATGGAAACTCACTCC---AAGTTAGTCGCCGAAG ATGATGTCTGTTGATAACGCTTGGTTACCAAGAGGTGAAATCATGGAAACTCACTCC---AAGTTAGTCGCCGAAG ATGATGTCTGTTGATAACGCTTGGTTACCAAGAGGTGAAATTATGGAATCTCACTCC---AAGTTGGTTGCTGAAG ATGATGTCTGTTGATGACACTTGGTTACCAAGAGGTGAATTAATGGAAACTCACTCT---AAGATGGTTGCTGAAG ATGATGTCCGTCGACAACACCTGGTTACCAAGAGGTGAATTGGTTGAAACTCACTCC---AAGATGGTTGCTGAAG ATGATGTCTGTTGATAACACTTGGTTACCAAGAGGTGAATTAGTTGAAACTCACTCT---AAATTAGTCGCCGAAG ATGATGTCTGTTGACAACACTTGGTTGCCAAGAGGTGAATTAATGGAAACTCACTCC---AAGATGGTTGCTGAAG ATGATGTCTGTTGATAACACTTGGTTACCAAGAGGTGAATTAATGGAAGCTCACTCT---AAGATGGTTGCTGAAG ATGTCCTCTGTTGACAATGCTTGGATTCCAAGAAGTGAATTAGTTGACTCCCACTCT---AAGTTAGTTGCTGAAG 115 6 Anhang Hu ATCC 9774 Hu BCD 3526 Hv DSM 70283 Io CBS 5147 Kl AB018535 Km BCD 2563 Km BCD 5186 Km BCD 811 Km DSM 70106 Km DSM 70792 Ku BCD 877 Le DSM 70320 Lt CBS 6340 Mp DSM 70321 Pa DSM 70277 Pan BCD 1082 Pan DSM 70783 Pc CBS 601 Pcar DSM 70392 Pf BCD 861 Pfe BCD 711 Pfe DSM 70090 Pg BCD 804 Pm DSM 70178 Po BCD 862 Pp AB018536 Sb BCD 1256 Sb BCD 1392 Sb DSM 70412 Sc AB018539 Sc DSM 1333 Sd BCD 1257 Sd DSM 70487 Se MUCL 29838 Sp DSM 6580 Sp BCD 728 Td DSM 70607 Yl AB018537 Yl BCD 2003 Yl BCD 2556 Zb BCD 1424 Zbi DSM 70415 Zf DSM 70506 Zm DSM 6959 Zr ATCC 48230 Scho DSM 70573 Schp AB018538 Schp BCD 773 HS14/III-VIII Hb1r-3r HT5r-6r Yfr5,7 Bd DSM70745 Cra DSM70197 Crc BCD 2578 Crc DSM 70022 Crf BCD 823 Crh DSM 70067 Crl BCD 824 Fn AF316889 Rg BCD 3530 Rm DSM 70408 Spj BCD 4982 Spj BCD 778 Spj DSM 70847 Trc DSM 70684 ATGTCTTCTGTTGACAATGCTTGGATTCCAAGAAGTGAATTAGTTGACTCCCACTCT---AAGTTAGTTGCTGAAG ATGTCCTCTGTTGACAATGCTTGGATTCCAAGAAGTGAATTAGTTGACTCCCACTCT---AAGTTAGTTGCTGAAG ATGTCCTCTGTTGACAACGCCTGGATTCCAAGAGGTGAATTGGTTGAAACTCACTCC---AAACTGGTTGCTGAAG ATGTTATCTGTTGATAACGCTTGGTTACCAAGAGGTGAATTAGTTGAATCTCACTCT---AAGATGGTTGCTGAAG ATGATGTCTGTTGACAACGCTTGGTTGCCAAGAGGTGAGTTGGTCGAATCTCACTCT---AAGATGGTTGCTGAAG ATGATGTCTGTTGACAACGCTTGGTTGCCAAGAGGTGAATTGATCGAATCTCACTCT---AAGATGGTTGCTGAAG ATGATGTCTGTTGACAACGCTTGGTTGCCAAGAGGTGAATTGGTCGAATCTCACTCT---AAGATGGTTGCTGAAG ATGATGTCTGTTGACAACGCTTGGTTGCCAAGAGGTGAATTGGTCGAATCTCACTCT---AAGATGGTTGCTGAAG ATGATGTCTGTTGACAACGCTTGGTTGCCAAGAGGTGAATTGATCGAATCTCACTCT---AAGATGGTTGCTGAAG ATGATGTCTGTTGACAACGCTTGGTTGCCAAGAGGTGAATTGATCGAATCTCACTCT---AAGATGGTTGCTGAAG ATGATGTCTGTTGACAATGCTTGGATTCCAAGAGGTGAATTAGTTGAATCTCATTCT---AAGATGGTTGCTGAAG ATGATGTCCGTTGACAACACTTGGTTGCCAAGAGGTGAATTGATGGAGACTCATGCC---AAGATGGTTGCTGAAG ATGATGTCCGTTGACAACGCCTGGATTCCAAGAGGTGAGTTGGTCGAGTCTCACTCT---AAGATGGTTGCTGAGG ATGATGTCCGTTGACAACGCCTGGTTGCCAAGAGGTGAGTTGATCGAGTCTCACGGT---AAGATGGTCGCCGAGG ATGATGTCTGTTGACAACGCTTGGTTGCCAAGAGGTGAGCTCATTGAATCCCACGCT---AAGATGGTTGCTGAGG ATGATGTCTGTTGATAACGCTTGGTTACCAAGAGGTGAATTGGTTGAAACTCATTCC---AAATTGGTTGCTGAAG ATGATGTCTGTTGATAACGCTTGGTTACCAAGAGGTGAATTGGTTGAAACTCATTCC---AAATTGGTTGCTGAAG ATGATGTCTGTTGACAGTGCTTGGTTACCAAGAGGTGAATTGGTTGAATCTCATTCT---AAATTGGTTGCTGAAG ATGATGTCTGTTGATAACACTTGGTTGCCAAGAGGTGAATTGATGGAAACCCACTCT---AAGATGGTTGCTGAAG ATGATGTCCGTTGACAACGCCTGGTTGCCAAGAGGTGAGCTTATGGCAAGTCACGCC---AAGATGGTCTCTGAAG ATGTTGTCTGTCGATAACGCTTGGTTGCCAAGAGGTGAATTGATTGAATCCCACTCC---AAGATGGTTGCTGAAG ATGTTATCCGTCGACAATGCTTGGTTACCAAGAGGTGAATTGGTTGAATCTCACTCC---AAGATGGTTGCTGAAG ATGATGTCTGTTGACAACGCTTGGTTGCCAAGAGGTGAATTGATGGAGACCCACTCC---AAGATGGTTGCTGAGG ATGTTGTCTGTTGATAACGCTTGGTTGCCAAGAGGTGAAGTGATTGAATCCCACTCC---AAGATGGTTGCTGAAG ATGATGTCTGTTGACAACACCTGGTTGCCAAGAGGTGAGTTGATGGAGACCCACGCC---AAGATGGTTGCCGAGA ATGATGTCTGTTGACAACGCTTGGTTGCCAAGAGGAGAGTTGGTAGAGTCCCACTCC---AAGATGGTTGCTGAGG ATGATGTCCGTCGACAACGCTTGGTTGCCAAGAGGTGAATTGGTCGAATCCCACTCC---AAGATGGTCGCTGAAG ATGATGTCTGTCGACAACGCTTGGATTCCAAGAGGTGAATTGGTTGAGTCTCACGCC---AAGATGGTCGCTGAAG ATGATGTCCGTCGACAACGCTTGGTTGCCAAGAGGTGAATTGGTCGAATCCCACTCC---AAGATGGTCGCTGAAG ATGATGTCCGTCGACAACGCTTGGATTCCAAGAGGTGAATTGGTTGAATCTCACTCT---AAGATGGTTGCTGAAG ATGATGTCCGTCGACAACGCTTGGATTCCAAGAGGTGAATTGGTTGAATCTCACTCT---AAGATGGTTGCTGAAG ATGATGTCCGTCGACAACGCTTGGATTCCAAGAGGTGAATTGGTTGAATCTCACTCT---AAGATGGTTGCTGAAG ATGATGTCCGTCGACAACGCTTGGATTCCAAGAGGTGAATTGGTTGAATCTCACTCT---AAGATGGTTGCTGAAG ATGATGTCCGTCGACAACGCTTGGATTCCAAGAGGTGAATTGGTTGAATCTCACTCT---AAGATGGTTGCTGAAG ATGATGTCTGTTGATAACGCTTGGCTACCAAGAGGCGAACTAATTGAATCGCACACT---AAACTCGTTGCAGAAG ATGATGTCCGTCAACAACGCTTGGTTGCCAAGAGGTGAATTGGTCGAATCTCACTCC---AAGATGGTCGCTGAAG ATGATGTCCGTCGACAACGCTTGGATTCCAAGAGGTGAATTGGTTGAATCTCACGCC---AAGATGGTCGCTGAAG ATGGGCTCCGTCGACAACGCCTGGATCCCCCGATCCGAGCTCATGGAGTCTCACTCC---AAGCAGGTTGCCGAGG ATGTCCTCTGTTGACAATGCATGGATTTCGCGATCTGAGTTGGTTGAATCTCACGCC---AAGTTGGTTGCTGAGG ATGGGTTCCGTCGACAACGCCTGGATCCCCCGATCCGAGCTCATGGAGTCCCACTCC---AAGCTGGTTGCTGAGG ATGATGTCTGTGGACAACGCTTGGTTGCCAAGAGGTGAATTGGCCGAATCTCACTCT---AAGATGGTTGCCGAGG ATGATGTCGGTTGACAACGCTTGGTTGCCAAGAGGTGAGTTGGCCGAGTCCCACTCT---AAGATGGTCGCCGAAG ATGATGTCTGTTGACAACGCTTGGTTACCAAGAGGTGAATTGGTCGAATCTCACTCC---AAATTGGTGGCTGAAG ATGATGTCTGTTGACAATGCTTGGTTACCAAGAGGTGAATTAGTCGAATCTCACGCT---AAAATGGTCGCTGAAG ATGATGTCTGTTGACAACGCTTGGTTGCCAAGAGGTGAAGTTATTGAATCTCACGGT---AAGATGGTTGCTGAAG ATGATGTCTTCCGACAACGCTTGGTTGCCTCGTGGTGAGCTTATGGAAAGCCACGCC---AAGATGGTTGCTGAAG ATGATGTCTTCCGACAATGCTTGGTTACCTCGTGGTGAACTTATGGAGACTCACGCT---AAGATGGTTGCTGAAG ATGATGTCTTCCGACAATGCTTGGTTACCTCGTGGTGAACTTATGGAGACTCACGCT---AAGATGGTTGCTGAAG |-----------------------| |-------------------------|------------------| ----------| CTTTCATCCGCTGAAAACATGTGGTTATCAAGAGATGAATTGGTTGCCAGAGGTTTCGAAAAGAAAGTCATGGAAC ATGTCCTCGACCGAGAACATCTGGATGTCCCGAGACGAGTTGATCAGCCGAGGTTTCGAAAAGAAGGTTCTTG--CAGTCTTCCGCCGACAACATCTGGATGTCGCGTGACGAGCTCGTCACCCGTGGTTTCGAGAAGAAGATTCTCGAGC CAGTCCTCTGCCGAGAACATCTGGATGTCCCGTGACGAGCTCATCACCCGTGGGTTCGAGAAGAAGGTCCTCG--ATGTCCTCCGCCGAGAACGTCTGGATCTCCCGAGACGAGCCCATCACCCGTGGGTTCGAGAAGAAGGTCCTCG--ATGTCGTCTGCCGAGAACGTCTGGCTCTCGCGTGACGAGCTCATTGCCCGTGGTTTCGAGAAGAAGGTCCTCG--CTATCTTCTGCCGAAAACATGTGGATGTCCCGAGACGAGCTCATTACTCGAGGTTTCGAAAAGAAGGTTCTTGAAC ATGTCCTCTGCCGAAAACATCTGGATTTCTCGAGACGAACTTGTTGCCCGTGGTTTCGAGAAGAAGGTTATGGAGC CTCTCGTCGTCCGAGAACATGTGGCTCCCGCGTGACGAGCTCGTCCGCCGTGGTTTCGAGAAGAAGGTCCTCG--CTCTCATCATCTGAAAACATCTGGATGTCTCGAGATGAGCTCATCTCACGTGGTTTCGAGAAGAAGGTCCTCGAGG CTTTCTTCGTCGGAGAACCTCTGGATTCCGCGTGACGAGCTCATCCGTCGTGGTTTCGAGAAGAAGGTCCTCG--CTCTCGTCGTCTGAGAACATGTGGCTCCCGCGTGACGAGCTCATCCGTCGTGGGTTCGAGAAGAAGGTCCTCG--CTCTCGTCGTCTGAGAACATGTGGCTCCCGCGTGACGAGCTCATCCGTCGTGGTTTCGAGAAGAAGGTCCTCG--CAGTCGTCGGCCGAGAACATCTGGATGTCGCGTGACGAGCTTATCTCGCGTGGCTTCGAGAAGAAGGTCCTCGAGC 116 6 Anhang HS09 Ha1r-8r HT1r-4r Ca AF038153 Ca ATCC 10231 Cb DSM 70034 Cc DSM 70136 Cd DSM 70042 Ce DSM70858 Cg BCD 8932 Cglae CBS 5691 Ch DSM 70624 Cim BCD 1062 Cint BCD 685 Ck BCD 689 Cll DSM 70102 Cm DSM 70638 Cmal AB018532 Cmal BCD 806 Cmel AB018533 Cmu DSM 70862 Cp ATCC 20384 Cr BCD 814 Cs BCD1054 Csan CBS 4261 Cso BCD 818 Ct BCD 819 Ctr ATCC 20326 Cv DSM 6956 Cvi DSM 70184 Cz AB018534 Cz BCD 690 De ATCC 20126 Dekb DSM 3429 Dekb DSM 70726 Dekc DSM 70736 Dh BCD 3512 Dh BCD 589 Dm ATCC 11627 Ef BCD 3514 Ef DSM 70554 Gs DSM 3431 Hb BCD 859 Hb DSM 3505 Hg DSM 70285 Hu ATCC 9774 Hu BCD 3526 Hv DSM 70283 Io CBS 5147 Kl AB018535 Km BCD 2563 Km BCD 5186 Km BCD 811 Km DSM 70106 Km DSM 70792 Ku BCD 877 Le DSM 70320 Lt CBS 6340 Mp DSM 70321 Pa DSM 70277 Pan BCD 1082 Pan DSM 70783 Pc CBS 601 Pcar DSM 70392 Pf BCD 861 Pfe BCD 711 Pfe DSM 70090 Pg BCD 804 Pm DSM 70178 Po BCD 862 Pp AB018536 Sb BCD 1256 Sb BCD 1392 Sb DSM 70412 Sc AB018539 Sc DSM 1333 305 310 320 330 340 350 360 370 376 |----|---------|---------|---------|---------|---------|---------|----| |---------------| |--------------------------| |---------------------| TTGATATGAAAGAAGCTTTGGCTTCTGGTCAATTCAGACCATTAACCAGAAAAGAAATTGAAGAACATTG TTGATATGAAAGAAGCTTTGGCTTCTGGTCAATTCAGACCATTAACCAGAAAAGAAATTGAAGAACATTG TTGATATGAAAGAAGCTTTAGCTTCTGGTCAATTCAGACCATTAACCAGAAAGGAAATTGAAGCTCATTG TCGACATGAAGGAGGCTCTTGCTTCCGGTCAGTTCCGTGCCCTTACCAGAAAGGAGATTGAGGAGCACTG TTGATATGAAGGAAGCTTTGGCATCTGGACAGTTCCGACCTTTGACCAGAAAGGAAATTGAAGCCCACTG TTGATATGAAAGAAGCCTTAGCTTCAGGTCAATTCAGACCTTTAGTTAGAAAGGAAATTGAAGCTCATTG TTGATATGAAGGAAGCTTTAGCTTCTGGTCAATTCAGAGCTTTAACCAGAAAGGAAATTGAATCTCATTG TTGATATGAAAGAAGCTTTAGCCTCCGGTCAATTCAGACCATTGACTAGAAAAGAAATCGAACAACACTG TTGATATGAAGGAGGCTTTGGCTTCCGGTCAGTTCAGACCATTGACCAGAAAGGAGATCGAGGACCACTG TTGATATGAAGGAGGCTCTTGCATCCGGTCAATTCCGTCCTCTTACCCGTAAGGAGATCGAGAAGCACTG TTGACATGAAGGAAGCTTTGGCTTCCGGTCAGTTCAGACCATTGACCAGAAAGGAGATCGAGAAACACTG TTGATATGAAGGAGGCTTTGGCTTCTGGACAATTCAGACCTTTGACCAGAAAGGAGATTGAGCAGCACTG TCGACATGAAGGAGGCTTTGGCTTCCGGTCAATTCAGACCATTGACCAGAAAGGAGATCGAACAACACTG TTGACATGAAGGAAGCTCTCGCCTCACC-----------------------------------------TTGATATGAAAGAAGCTTTGGCTTCCGGTCAATTCAGACCATTAACCAGAAAAGAAATCGAAGAACATTG TTGATATGAAGGAAGCTTTGGCTTCCGGTCAATTCAGACCTTTGACCAGAAAGGAAATCGAACAACACTG TTGACATGAAGGAGGCCTTGGCTTCTGGTCAATTTAGACCTTTGACCAGAAAGGAGATTGAGGAGCATTG TTGATATGAAAGAAGCTTTAGCATCTGGTCAATTCAGACCTTTAACTAGAAAAGAAATTGAAGAACATTG TTGATATGAAAGAAGCTTTGGCTTCAGGTCAATTCAGACCATTGACTAGAAAGGAAATCGAGAAACACTG TCGATATGAAGGAGGCTCTTGCTTCTGGTCAGTTCCGTCCTCTTACCCGTAAGGAGATAGAACAACACTG TTGATATGAAGGAAGCTTTGGCTTCTGGTCAATTCAGACCATTAACTAGAAAGGAAATCGAAAAACACTG TTGATATGAAGGAAGCTTTAGCTTCTGGTCAATTCAGACCATTAACCAGAAAGGAAATTGAAGAACACTG TTGATATGAAAGAAGCTTTAGCCTCAGGTCAATTCCGTGCTTTAACCAGAAAAGAAATTGAATCTCACTG TTGATATGAAGGAAGCTTTGGCTTCTGGTCAATTCAGACCTTTAACCAGAAAGGAAATCGAAAAACACTG TTGATATGAAAGAAGCTTTGGCTTCCGGTCAATTCAGACCATTAACCAGAAGAGAAATCGAACAACACTG TTGATATGAAGGAAGCATTGGCTTCTGGTCAGTTCCGCCCTCTTACCAGAAAGGAGATTGAGCAACACTG TTGATATGAAGGAAGCTTTAGCTTCTGGTCAATTTAGACCATTAACCAGAAAAGAAATCGAAGAACACTG TTGACATGAAGGAGGCCTTGGCTTCTGGTCAATTTAGACCTTTGACCAGAAAGGAGATTGAGGAGCATTG TTGACATGAAGGAGGCCTTGGCTTCTGGTCAATTTAGACCTTTGACCAGAAAGGAGATAGAGAAACACTG TTGATATGAAGGAAGCTTTAGCATCTGGTCAATTCAGACCATTAACTAGAAAGGAGATCGAGAAGCACTG TTGATATGAAGGAAGCTCTTGCCAACGGTCAGTATAGAGCTTTGACCAGAAAGGAGATCGAGGCGCACTG TTGATATGAAGGAAGCTCTTGCCAACGGTCAGTATAGAGCTTTGACCAGAAAGGAGATCGAGGCCCATTG TCGATATGAAGGAAGCTCTTGCCAACGGTCAGTACAGACCATTGACTAGAAAGAACATCGAAGAGCACTG TCGATATGAAGGAAGCTTTAGCCTCTGGTCAATTCAGACCATTAACCAGAAAAGAGATCGAACAACACTG TCGATATGAAGGAAGCTTTAGCCTCTGGTCAATTCAGACCATTAACCAGAAAAGAAATCGAAAAACACTG TTGATATGAAGGAAGCTTTAGCCTCTGGTCAATTTAGACCATTAACCAGAAAGGAAATCGAAGAACACTG TTGATATGAAAGAAGCTTTAGCTTCCGGTCAATTCAGACCATTAACCAGAAAAGAAATCGAAAAACACTG TTGATATGAAGGAAGCTTTGGCTTCTGGTCAATTCAGACCATTGACCAGAAAAGAAATCGAAGATCATTG TTGATATGAAGGAAGCTTTAGCTTCTGGTCAATTCAGAGCTTTAACCAGAAAGGAAATAGAAAAGCACTG TTGATATGAAGGAAGCTTTGGCTTCTGGTCAACTCAGACCTTTAACCAGAAAGGAAATCGAAAAACACTG TTGATATGAAAGAAGCTTTAGCTTCCGGTCAATTCAGACCATTAACCAGAAAAGAAATCGAAAAACACTG TTGATATGAAGGAAGCTTTAGCTTCTGGTCAATTCAGAGCTTTAACCAGAAAGGAAATTGAATCCCACTG TTGATATGAAGGAAGCTTTAGCTTCTGGTCAATTCAGAGCTTTAACCAGAAAGGAAATTGAATCCCACTG TTGATATGAAGGAAGCTTTAGCTTCTGGTCAATTCAGAGCTTTAACCAGAAAGGAAATTGAATCCCACTG TTGATATGAAAGAAGCTTTGGCTTCTGGTCAATTCAGAGCTTTGACCAGAAAAGAAATTGAATCTCACTG TTGATATGAAGGAAGCTTTAGCTTCTGGTCAATTCAGACCATTGACTAGAAAGGAAATCGAAAAACACTG TTGATATGAAGGAAGCTTTGGCTTCTGGTCAATTCAGACCTTTGACTAGAAAGGAAATCGAAGAGCACTG TTGATATGAAGGAAGCTTTGGCTTCCGGTCAATTCAGACCTTTGACCAGAAAGGAAATCGAAAAACACTG TTGATATGAAGGAAGCTTTGGCTTCCGGTCAATTCAGACCTTTGACCAGAAAGGAGATCGAACAACACTG TTGATATGAAGGAAGCTTTGGCTTCCGGTCAATTCAGACCTTTGACCAGAAAGGAAATCGAAAAACACTG TTGATATGAAGGAAGCTTTGGCTTCCGGTCAATTCAGACCTTCGACCAGAAAGGAAATCGAACAGCACTG TTGATATGAAGGAAGCTTTGGCTTCCGGTCAATTCAGACCTTTGACCAGAAAGGAAATCGAAAAACACTG TTGATATGAAGGAAGCTTTAGCTTCTGGTCAATTCAGACCATTAACTAGAAAGGAAATCGAAAAACACTG TTGATATGAAGGAAGCTTTGGCTTCAGGTCAATTCAGACCATTGACCAGAAAGGAAATCGAGCAACACTG TTGACATGAAGGAGGCTTTGGCTTCCGGTCAGTTCCGTCCTTTGACCAGAAAGGAGATCGAGGAGCACTG TTGACATGAAGGAGGCTTTGGCTTCCGGTCAGTTCAGACCATTGACCAGGAAGGAGATCGAAAAGCACTG TTGACATGAAGGAAGCTTTGGCTTCCGGTCAATTCAGACCTTTGACTAGAAAGGAGATCGAGCAGCACTG TTGATATGAAAGAAGCTTTAGCTTCAGGTCAATTCCGTGCTTTAACCAGAAAAGAAATTGAATCTCACTG TTGATATGAAAGAAGCTTTAGCTTCAGGTCAATTCCGTGCTTTAACCAGAAAAGAAATTGAATCTCACTG TTGATATGAAAGAAGCTTTAGCTTCTGGTCAATTCCGTCCATTAACCAGAAAAGAAATTGAACAACATTG TGGATATGAAAGAAGCCTTAGCATCTGGTCAATTTAGACCATTAACTAGAAAGGAAATTGAAGAACATTG TCGATATGAAGGAGGCTTTGGCTTCTGGTCAATTCAGACCTTTGACTAGAAAGGAAATCGAAAAACACTG TTGATATGAAGGAAGCTTTGGCTTCTGGTCAATTCAGACCATTAACCAGAAAGGAAATCGAAAAACACTG TTGATATGAAGGAAGCTTTAGCATCTGGTCAATTCAGACCATTAACCAGAAAGGAGATCGAAAAGCACTG TTGATATGAAGGAGGCTTTGGCTTCTGGACAATTCAGACCTTTGACCAGAAAGGAGATCGAAAAGCATTG TTGATATGAAGGAAGCTTTAGCATCTGGTCAATTCAGACCATTAACCAGAAAGGAAATCGAAGACCATTG TCGACATGAAGGAGGCTCTTGCCTCTGGTCAGTTTAGACCATTGACCAGAAAGGAGATCGAACAACACTG TCGATATGAAGGAGGCTTTGGCTTCCGGTCAATTCCGTCCTTTGACCAGAAAAGAAATCGAGGAGCACTG TTGATATGAAGGAAGCTTTGGCTTCCGGTCAATTCCGTCCATTAACTAGAAAGGAAATCGAAAAACACTG TCGATATGAAGGAAGCTTTGGCTTCCGGTCAATTCCGTCCATTGACCAGAAAGGAAATAGAAAAGCACTG TTGATATGAAGGAAGCTTTGGCTTCCGGTCAATTCCGTCCATTAACCAGAAAGGAAATTGAAGAACATTG TTGATATGAAGGAAGCTTTGGCTTCTGGTCAATTCCGTCCATTAACCAGAAAAGAAATTGAAGAACATTG TTGATATGAAGGAAGCTTTGGCTTCTGGTCAATTCCGTCCATTAACCAGAAAAGAGATCGAAAAACACTG 117 6 Anhang Sd BCD 1257 Sd DSM 70487 Se MUCL 29838 Sp DSM 6580 Sp BCD 728 Td DSM 70607 Yl AB018537 Yl BCD 2003 Yl BCD 2556 Zb BCD 1424 Zbi DSM 70415 Zf DSM 70506 Zm DSM 6959 Zr ATCC 48230 Scho DSM 70573 Schp AB018538 Schp BCD 773 Hb1r-3r Bd DSM70745 Cra DSM70197 Crc BCD 2578 Crc DSM 70022 Crf BCD 823 Crh DSM 70067 Crl BCD 824 Fn AF316889 Rg BCD 3530 Rm DSM 70408 Spj BCD 4982 Spj BCD 778 Spj DSM 70847 Trc DSM 70684 TTGATATGAAGGAAGCTTTGGCTTCTGGTCAATTCCGTCCATTAACCAGAAAAGAAATCGAAAAACACTG TTGATATGAAGGAAGCTTTGGCTTCTGGTCAATTCCGTCCATTAACCGGAAAAGAAATTGAAGAACATTG TTGATATGAAGGAAGCTTTGGCTTCTGGTCAACTCCGTCCATTAACCAGAAAAGAAATTGAAGAACATTG TTGATATGAGGGAAGCACTTGCCTCCGGTCAATTTAGAGCCTTAACTAGAAAAGAGATTGAGTCTCATTG TTGATATGAAGGAAGCTTTGGCTTCTGGTCAATTCCGTCCATTAACCAGAAAGGAGATCGAAAAAC---TTGATATGAAGGAAGCTTTGGCTTCCGGTCAATTCCGTCCATTGACCAGAAAGGAAATCGAAAAACACTG TTGATATGAAGGAGGCTCTTGCTTCCGGACAGTTCCGACCTCTTACCAAGAAGGAGATTGAGCAGCATTG TTGATATGAAGGAAGCTTTGGCATCTGGACAGTTCCGACCTTTGACCAGAAAGGAAATTGAAGCCCACTG TTGATATGAAGGAGGCCCTTGCTTCCGGACAGTTCCGACCTCTTACCAAGAAGGAGATTGAGGCCCACTG TTGACATGAAGGAGGCCTTGGCTTCCGGTCAGTTCCGTGCGTTGACCAGAAAGGAAATCGAAAAACACTG TCGACATGAAGGAAGCTTTGGCTTCCGGTCAGTTCCGTGCGTTGACTAGAAAGGAGATTGAAGAGCACTG TTGATATGAAGGAGGCTTTGGCTTCTGGTCAATTCCGTCCATTAACCAGAAAGGAAATCGAAGAACACTG TTGATATGAAAGAAGCTTTGGCTTCCGGTCAATTCCGTCCTCTAACCAGAAAGGAAATCGAAGAACACTG TTGATATGAAGGAAGCTTTGGCTTCCGGTCAATTCCGTCCATTGACCAGAAAGGAAATAGAAGAGCACTG TTGACCGTGCTGAAGCTTTGAAGAGTGGTCAATTCCGTCCCTTGGTCCGTAAGGAAATTGAAGAACACTG TTGACCGTGCTGAGGCCTTGAAGAGTGGTCAATTCCGTCCCTTGGTCCGTAAGGAGATTGAGGAGCACTG TTGACCGTGCTGAGGCCTTGAAGAGTGGTCAATTCCGTCCCTTGGTCCGTAAGGAGATCGAAAAGCACTG --| TTGATACCCGAGAAGCTCAACGATTAGGTTTAATGAGACCTTTAGTCCGAAGAGAAATCGAAAAACATTT ---------------------------------------------------------------------TCGACACCCGTGAGGCCCAGCGTCTTGGTCTCATGCGCCCCCTTGTCCGTCGCGAGATCGAAAAACACTG ---------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------TCGACACCAAGGAGGCTCAGCGATTGGGTCTCATGCGACCTTTGGTTCGACGAGAAATCGAAAAGCACTT TCGACACCAGGGAGGCTCAGCGATTGGGTCTCATGAGGCCCTTGGTCAGGAGGGAAATCGAAAAGCACTT ---------------------------------------------------------------------TTGATACTCGTGAAGCTCAACGTCTTGGTTTAATGAGACCTCTAGTCCGAAAGGAAATCGAGAAGCACAT ---------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------TCGACACCCGTGAGGCTCAGCGTCTTGGTCTCATGCGCCCCCTCGTCCGTCGCGAGATCGAAAAGCACTG Bd: Bullera dendrophila; Ca: Candida albicans; Cb: Candida boidinii; Cc: Candida catenulata; Cd: Candida diddensiae; Ce: Candida ernobii; Cg: Candida glabrata; Cglae: Candida glaebosa; Ch: Candida haemulonii; Cim: Citeromyces matritensis; Cint: Candida intermedia; Ck: Candida krusei; Cll: Clavispora lusitaniae; Cm: Candida magnoliae; Cmal: Candida maltosa; Cmel: Candida melibiosica; Cmu: Candida multigemmis; Cp: Candida parapsilosis; Cr: Candida rugosa; Cra: Cryptococcus albidus; Crc: Cryptococcus curvatus; Crf: Cryptococcus flavus; Crh: Cryptococcus humicola; Crl: Cryptococcus laurentii; Cs: Candida sake; Csan: Candida santamariae; Cso: Candida solani; Ct: Candida tenuis; Ctr: Candida tropicalis; Cv: Candida versatilis; Cvi: Candida vini; Cz: Candida zeylanoides; De: Debaryomyces etchelsii; Dekb: Dekkera bruxellensis; Dekc: Dekkera custersiana; Dh: Debaryomyces hansenii; Dm: Debaryomyces marama; Ef: Endomyces fibuliger; Fn: Filobasidiella neoformans; Gs: Guilliermondella selenospora; Hb: Hyphopichia burtonii; Hg: Hanseniaspora guilliermondii; Hu: Hanseniaspora uvarum; Hv: Hanseniaspora vineae; Io: Issatchenkia orientalis; Kl: Kluyveromyces lactis; Km: Kluyveromyces marxianus; Ku: Kazachstania unispora; Le: Lodderomyces elongisporus; Lt: Lachancea thermotolerans; Mp: Metschnikowia pulcherrima; Pa: Pichia angusta; Pan: Pichia anomala; Pc: Pichia canadensis; Pcar: Pichia carsonii; Pf: Pichia farinosa; Pfe: Pichia fermentans; Pg: Pichia guilliermondii; Pm: Pichia membranaefaciens; Po: Pichia ohmeri; Pp: Pichia pastoris; Rg: Rhodotorula glutinis; Rm: Rhodotorula minuta; Sb: Saccharomyces bayanus; Sc: Saccharomyces cerevisiae; Scho: Schizosaccharomyces octosporus; Schp: Schizosaccharomyces pombe; Sd: Saccharomyces cerevisiae var. diastaticus; Se: Saccharomyces exiguus; Sp: Saccharomyces pastorianus; Spj: Sporidiobolus johnsonii; Td: Torulaspora delbrueckii; Trc: Trichosporon cutaneum; Yl: Yarrowia lipolytica; Zb: Zygosaccharomyces bailii; Zbi: Zygosaccharomyces bisporus; Zf: Zygosaccharomyces florentinus; Zm: Zygosaccharomyces microellipsoides; Zr: Zygosaccharomyces rouxii 118 6 Anhang Hg DSM 70285 Hu ATCC 9774 Hu BCD 3526 Hv DSM 70283 Csan CBS 4261 Hb DSM 3505 94 94 88 87 79 84 82 85 90 90 94 95 91 64 92 85 99 87 91 80 97 97 94 94 89 86 80 83 83 84 89 91 94 96 92 64 91 86 98 86 90 81 96 96 92 92 90 84 80 83 82 85 92 90 93 97 94 65 93 88 94 86 90 81 94 93 78 78 84 75 79 70 82 74 77 80 81 80 84 62 77 84 76 76 78 78 75 75 78 78 84 75 79 70 82 74 77 80 81 80 84 62 77 84 76 76 78 78 75 75 76 76 79 70 74 69 76 72 76 78 80 79 82 58 75 79 75 74 76 74 74 74 94 94 88 85 79 82 82 83 87 94 94 94 91 63 91 85 94 87 89 80 93 93 94 94 88 85 79 82 82 83 87 94 94 94 91 63 91 85 94 87 89 80 93 93 92 92 89 84 80 81 83 82 86 94 93 93 90 64 90 86 92 85 88 81 91 91 87 87 83 85 72 82 75 84 85 82 84 88 85 63 88 79 86 90 86 72 87 87 84 84 80 79 71 84 75 81 80 79 81 84 81 63 84 77 84 82 81 69 84 84 83 83 77 79 71 81 78 75 81 75 79 81 78 62 84 75 81 78 83 70 84 83 87 87 84 87 72 81 75 85 84 82 84 86 84 64 86 79 86 92 85 72 87 87 87 87 84 85 73 82 76 84 85 83 84 88 85 64 88 80 86 90 86 73 87 87 80 80 83 75 82 74 97 75 77 83 85 82 84 64 79 83 84 75 77 84 81 81 80 80 83 75 82 74 97 75 77 83 85 82 84 64 79 83 84 75 77 84 81 81 80 80 83 75 82 74 97 75 77 83 85 82 84 64 79 83 84 75 77 84 81 81 84 84 84 78 80 77 89 77 80 83 88 84 86 66 82 84 84 78 81 81 83 83 Die verwendeten Abkürzungen entsprechen den Abkürzungen in der Abbildung 6.1. 119 80 80 83 75 93 72 86 76 80 79 84 83 83 71 81 83 81 74 78 100 Cs BCD 1054 Hb BCD 859 86 86 96 79 82 80 84 81 85 91 90 89 92 67 84 91 88 84 85 83 88 88 84 84 93 77 83 78 82 80 84 87 89 88 92 63 83 100 Cr BCD 814 Gs DSM 3431 Cp ATCC 20384 Ef DSM 70554 Cmu DSM 70862 Ef BCD 3514 Cmel AB018533 Dm ATCC 11627 78 78 81 77 89 70 83 78 79 78 81 80 79 72 78 78 81 73 81 90 81 79 92 92 90 84 82 83 83 85 90 89 94 100 Cmal BCD 806 Dh BCD 589 Cmal AB018532 Dh BCD 3512 Cm DSM 70638 Dekc DSM 70736 Cll DSM 70102 Dekb DSM 70726 95 95 83 88 78 84 80 85 88 84 87 91 85 67 98 81 89 86 93 79 92 90 91 91 91 84 83 81 84 83 91 90 100 Ck BCD 689 Dekb DSM 3429 87 87 87 84 79 79 82 84 84 85 89 92 87 62 87 84 87 85 86 79 88 86 Cint BCD 685 De ATCC 20126 Cim BCD 1062 Cz BCD 690 Ch DSM 70624 Ce DSM 70858 Cz AB018534 Cglae CBS 5691 Cd DSM 70042 Cvi DSM 70184 85 85 86 81 78 82 84 79 81 84 87 87 86 62 84 84 86 78 84 77 86 86 Cg BCD 8932 Cc DSM 70136 94 94 84 87 78 82 80 87 89 84 87 90 85 67 94 80 90 85 100 Cv DSM 6956 89 89 84 85 73 81 74 83 84 83 84 86 84 64 88 80 86 100 Ca AF038153 Ca ATCC 10231 Cb DSM 70034 Cc DSM 70136 Cd DSM 70042 Ce DSM 70858 Cg BCD 8932 Cglae CBS 5691 Ch DSM 70624 Cim BCD 1062 Cint BCD 685 Ck BCD 689 Cll DSM 70102 Cm DSM 70638 Cmal AB018532 Cmal BCD 806 Cmel AB018533 Cmu DSM 70862 Cp ATCC 20384 Cr BCD 814 Cs BCD 1054 Csan CBS 4261 Ca AF038153 Cb DSM 70034 94 94 87 86 80 83 83 84 89 89 93 94 90 64 91 84 100 84 84 81 78 73 100 Ctr ATCC 20326 97 97 84 90 80 84 82 87 90 85 89 93 87 68 100 79 79 83 76 100 87 87 81 86 77 78 78 100 88 88 90 80 78 79 83 81 84 100 65 65 65 64 69 59 66 64 66 62 63 66 63 100 100 100 86 91 100 86 91 100 80 100 81 81 82 76 84 74 100 88 88 86 84 79 80 78 82 100 88 88 93 81 82 81 84 82 90 91 95 94 100 Ca AF038153 Ca ATCC 10231 Cb DSM 70034 Cc DSM 70136 Cd DSM 70042 Ce DSM 70858 Cg BCD 8932 Cglae CBS 5691 Ch DSM 70624 Cim BCD 1062 Cint BCD 685 Ck BCD 689 Cll DSM 70102 Cm DSM 70638 Cmal AB018532 Cmal BCD 806 Cmel AB018533 Cmu DSM 70862 Cp ATCC 20384 Cr BCD 814 Cs BCD 1054 Csan CBS 4261 Ct BCD 819 Ca ATCC 10231 Distanz-Matrix: Prozentuale Übereinstimmung der EF-3 Aminosäuresequenzen innerhalb der Unterabteilung der Ascomycota Cso BCD 818 Tab. 6.2: 93 93 87 87 80 84 82 85 92 88 92 94 89 67 94 84 96 87 91 81 100 93 93 87 87 79 85 80 84 90 88 92 93 89 65 92 84 96 89 89 79 98 100 6 Anhang Io CBS 5147 Kl AB018535 Km BCD 2563 Km BCD 5186 Km BCD 811 Km DSM 70106 Km DSM 70792 Ku BCD 877 Le DSM 70320 Lt CBS 6340 Mp DSM 70321 Pa DSM 70277 Pan BCD 1082 Pan DSM 70783 Pc CBS 601 Pc DSM 70392 Pf BCD 861 Pfe BCD 711 Pfe DSM 70090 Pg BCD 804 Pm DSM 70178 Po BCD 862 Pp AB018536 Ca AF038153 Ca ATCC 10231 Cb DSM 70034 Cc DSM 70136 Cd DSM 70042 Ce DSM 70858 Cg BCD 8932 Cglae CBS 5691 Ch DSM 70624 Cim BCD 1062 Cint BCD 685 Ck BCD 689 Cll DSM 70102 Cm DSM 70638 Cmal AB018532 Cmal BCD 806 Cmel AB018533 Cmu DSM 70862 Cp ATCC 20384 Cr BCD 814 Cs BCD 1054 Csan CBS 4261 87 87 96 80 84 80 84 80 86 90 90 91 94 68 86 93 87 85 85 84 87 87 84 84 93 78 83 78 84 81 84 89 91 89 94 62 84 98 85 81 81 83 84 84 84 84 93 78 83 78 82 81 85 88 91 89 92 63 84 98 85 81 81 83 85 85 84 84 92 77 84 78 84 82 84 86 89 90 91 64 84 97 84 80 82 84 86 84 85 85 94 79 84 80 84 82 85 89 91 90 94 64 84 98 86 82 82 84 86 86 83 83 91 76 81 76 80 79 84 86 89 87 90 62 82 96 84 79 79 81 84 84 84 84 93 78 83 78 82 81 85 88 91 89 92 63 84 98 85 81 81 83 85 85 83 83 91 76 82 80 85 81 82 88 87 85 89 65 81 92 84 79 80 82 84 84 95 95 86 90 77 85 78 88 88 86 89 91 87 65 95 83 90 89 93 77 91 91 85 85 90 79 84 79 86 83 82 89 89 88 90 64 84 94 86 82 83 84 85 85 85 85 90 78 81 77 80 79 86 88 93 89 91 62 84 88 86 82 84 80 85 86 87 87 92 82 83 78 84 84 84 91 89 89 90 66 86 92 87 82 86 83 87 87 87 87 88 83 81 84 87 81 83 86 90 89 89 64 86 86 88 80 86 80 88 88 87 87 88 83 81 84 87 81 83 86 90 89 89 64 86 86 88 80 86 80 88 88 89 89 94 80 82 80 82 78 86 90 93 90 92 64 87 90 89 82 85 83 89 89 92 92 84 87 75 84 76 83 86 86 88 90 87 63 91 83 90 90 86 74 91 93 91 91 88 83 80 81 81 82 84 88 89 93 89 64 90 86 89 83 87 81 88 88 86 86 94 80 85 80 83 81 85 90 91 91 92 67 85 93 87 83 83 85 87 87 84 84 93 78 80 76 81 78 83 86 86 87 90 66 83 89 84 86 82 81 84 84 92 92 90 84 82 83 83 85 90 89 94 100 94 66 93 88 94 86 90 83 94 93 84 84 93 78 83 79 81 80 84 90 89 88 89 66 83 90 86 81 82 83 86 86 91 91 81 85 75 81 76 87 84 83 84 88 83 64 91 78 86 83 92 75 87 86 86 86 95 80 84 82 84 81 84 88 90 91 92 68 85 94 87 84 84 84 87 87 Sb BCD 1392 Sb DSM 70412 Sc AB018539 Sp BCD 728 Sc DSM 1333 Scho DSM 70573 Schp AB018538 Schp BCD 773 Sd BCD 1257 Sd DSM 70487 Se MUCL 29838 Sp DSM 6580 Td DSM 70607 Yl AB018537 Yl BCD 2003 Yl BCD 2556 Zb BCD 1424 Zbi DSM 70415 Zf DSM 70506 Zm DSM 6959 Zr ATCC 48230 Fortsetzung Sb BCD 1256 Tab. 6.2: Ca AF038153 Ca ATCC 10231 Cb DSM 70034 Cc DSM 70136 Cd DSM 70042 Ce DSM 70858 Cg BCD 8932 Cglae CBS 5691 Ch DSM 70624 Cim BCD 1062 Cint BCD 685 Ck BCD 689 Cll DSM 70102 Cm DSM 70638 Cmal AB018532 Cmal BCD 806 Cmel AB018533 Cmu DSM 70862 Cp ATCC 20384 Cr BCD 814 Cs BCD 1054 Csan CBS 4261 87 87 94 80 82 78 84 81 87 91 92 89 94 64 84 94 87 85 84 83 86 86 83 83 89 76 83 76 87 81 81 88 87 85 90 64 82 93 84 77 80 83 83 83 87 87 94 80 82 78 84 81 87 91 92 89 94 64 84 94 87 85 84 83 86 86 84 84 95 78 85 79 84 81 86 88 90 89 94 66 84 95 85 83 83 85 85 85 86 86 94 79 81 77 83 80 86 90 91 88 94 64 84 93 86 84 84 82 85 85 84 84 95 78 85 79 84 81 86 88 90 89 94 66 84 95 85 83 83 85 85 85 76 76 82 70 70 72 73 73 73 77 78 78 77 57 74 78 76 74 75 71 75 75 75 75 78 71 71 71 71 73 72 74 76 78 77 57 74 76 75 74 74 70 74 74 75 75 78 71 71 71 71 73 72 74 76 78 77 57 74 76 75 74 74 70 74 74 84 84 95 78 85 79 84 81 86 88 90 89 94 66 84 95 85 83 83 85 85 85 84 84 94 77 84 78 84 80 85 87 89 88 93 66 83 94 84 82 82 84 84 84 84 84 94 77 84 78 84 80 85 87 89 88 93 66 83 94 84 82 82 84 84 84 84 84 91 80 83 74 82 78 87 85 89 84 88 64 82 90 84 79 82 83 84 84 83 83 89 76 83 76 87 81 81 88 87 85 90 64 82 94 84 77 80 83 83 83 77 77 80 74 87 70 83 76 78 77 82 84 81 67 78 80 81 73 76 87 79 77 78 78 82 75 99 72 84 76 78 77 82 81 81 68 79 83 79 72 77 92 79 78 78 78 80 76 86 69 82 76 79 77 83 84 81 64 79 80 82 74 77 87 80 78 84 84 93 80 81 76 84 80 86 88 90 90 93 64 84 93 86 83 83 82 84 84 85 85 93 80 81 76 84 80 86 88 90 90 93 65 84 93 86 84 84 82 84 84 86 86 94 80 85 79 84 81 86 88 92 89 93 64 85 97 87 81 83 85 87 87 87 87 94 80 84 77 85 82 86 90 91 89 94 66 86 94 85 84 85 84 84 84 85 85 90 78 81 75 83 80 84 89 91 88 91 64 84 92 84 83 84 82 84 84 Die verwendeten Abkürzungen entsprechen den Abkürzungen in der Abbildung 6.1. 120 6 Anhang 85 86 84 82 98 88 89 91 87 87 82 88 88 89 84 79 78 84 84 84 84 84 85 84 85 82 78 91 86 87 90 85 85 80 87 87 88 80 78 75 80 81 84 84 84 86 84 84 82 79 91 86 87 89 84 84 81 86 86 87 80 77 75 80 81 83 83 83 84 84 85 83 80 90 85 86 89 84 84 78 85 85 86 79 77 77 79 80 83 83 83 84 85 85 83 80 93 87 88 90 86 86 81 87 87 88 81 79 75 81 82 84 84 84 86 82 83 80 77 89 84 85 87 83 83 79 84 84 85 78 75 74 78 79 81 81 81 83 84 84 82 79 91 86 87 89 84 84 81 86 86 87 80 77 75 80 81 83 83 83 84 84 83 79 81 91 85 86 85 84 84 80 84 84 85 77 82 77 78 78 86 86 86 90 84 88 94 77 86 91 90 91 78 78 77 90 90 89 90 85 83 89 90 77 77 77 81 84 84 83 81 90 87 88 86 86 86 80 87 87 88 81 79 74 81 82 87 87 87 88 81 84 82 79 89 87 88 87 81 81 80 86 86 87 82 76 74 81 83 80 80 80 81 85 85 84 83 94 88 89 89 84 84 81 86 86 87 82 78 78 82 83 83 83 83 83 97 86 84 78 87 89 90 87 82 82 78 89 89 88 84 85 85 83 84 88 88 88 89 97 86 84 78 87 89 90 87 82 82 78 89 89 88 84 85 85 83 84 88 88 88 89 86 85 85 79 94 90 91 90 82 82 77 90 90 91 82 79 79 80 82 83 83 83 84 82 87 89 75 84 91 90 91 76 76 74 91 91 89 87 84 81 87 87 77 77 77 81 84 86 88 80 87 90 91 91 79 79 75 90 90 91 84 79 75 82 84 81 81 81 80 85 86 84 82 94 88 89 91 84 84 80 88 88 89 82 79 75 82 83 84 84 84 84 82 84 81 78 94 84 85 87 84 84 79 84 84 85 83 77 74 83 84 82 82 82 82 87 92 91 80 89 95 96 97 80 80 79 94 94 93 88 84 81 86 88 82 82 82 84 84 84 81 81 94 87 88 88 81 81 77 87 87 89 79 78 74 80 80 82 82 82 84 79 84 89 74 82 87 86 88 73 73 71 85 85 84 83 78 77 82 83 74 74 74 77 88 86 84 81 94 88 89 89 84 84 79 88 88 89 84 82 81 84 84 85 85 85 85 121 85 81 77 80 84 83 84 81 83 83 76 83 83 84 76 76 77 76 77 100 100 100 Hv DSM 70283 Pp AB018536 Hu BCD 3526 Po BCD 862 Hu ATCC 9774 Pm DSM 70178 Cso BCD 818 Ct BCD 819 Ctr ATCC 20326 Cv DSM 6956 Cvi DSM 70184 Cz AB018534 Cz BCD 690 De ATCC 20126 Dekb DSM 3429 Dekb DSM 70726 Dekc DSM 70736 Dh BCD 3512 Dh BCD 589 Dm ATCC 11627 Ef BCD 3514 Ef DSM 70554 Gs DSM 3431 Hb BCD 859 Hb DSM 3505 Hg DSM 70285 Hu ATCC 9774 Hu BCD 3526 Hv DSM 70283 Die verwendeten Abkürzungen entsprechen den Abkürzungen in der Abbildung 6.1. 83 84 86 74 83 87 86 88 77 77 74 86 86 86 98 84 80 95 100 Hg DSM 70285 Pg BCD 804 81 84 84 74 83 87 86 86 77 77 74 86 86 84 95 84 79 100 Hb DSM 3505 Pfe DSM 70090 Hb BCD 859 Pfe BCD 711 Gs DSM 3431 Pf BCD 861 Ef DSM 70554 Pc DSM 70392 Ef BCD 3514 Pc CBS 601 Dm ATCC 11627 Pan DSM 70783 Dh BCD 589 Pan BCD 1082 Dh BCD 3512 Pa DSM 70277 Dekc DSM 70736 Mp DSM 70321 Dekb DSM 70726 Lt CBS 6340 Dekb DSM 3429 Le DSM 70320 Cz BCD 690 Cz AB018534 Cvi DSM 70184 De ATCC 20126 83 84 86 73 82 87 86 88 76 76 74 86 86 85 100 85 81 77 80 84 83 84 81 83 83 76 83 83 84 76 76 77 76 77 100 100 Ku BCD 877 86 89 88 79 88 93 94 92 79 79 75 98 98 100 85 81 77 80 84 83 84 81 83 83 76 83 83 84 76 76 77 76 77 100 Km DSM 70792 87 90 89 78 87 94 95 93 78 78 76 100 100 84 79 83 71 78 82 81 81 72 72 68 80 80 79 80 88 100 Km DSM 70106 87 90 89 78 87 94 95 93 78 78 76 100 84 81 82 69 79 84 84 83 72 72 71 82 82 81 84 100 Km BCD 811 Cv DSM 6956 Ctr ATCC 20326 75 75 74 74 80 76 77 78 90 90 100 Km BCD 5186 88 89 89 81 90 99 100 79 78 75 79 85 77 78 80 100 100 Km BCD 2563 87 88 90 80 89 100 79 78 75 79 85 77 78 80 100 100 84 83 75 100 85 78 100 76 100 Kl AB018535 84 86 83 83 100 85 91 91 78 89 94 94 100 Cso BCD 818 Ct BCD 819 Ctr ATCC 20326 Cv DSM 6956 Cvi DSM 70184 Cz AB018534 Cz BCD 690 De ATCC 20126 Dekb DSM 3429 Dekb DSM 70726 Dekc DSM 70736 Dh BCD 3512 Dh BCD 589 Dm ATCC 11627 Ef BCD 3514 Ef DSM 70554 Gs DSM 3431 Hb BCD 859 Hb DSM 3505 Hg DSM 70285 Hu ATCC 9774 Hu BCD 3526 Hv DSM 70283 Io CBS 5147 Ct BCD 819 Fortsetzung Cso BCD 818 Tab. 6.2: 86 84 80 78 85 84 85 83 84 84 80 85 85 85 76 80 80 77 76 90 90 90 100 6 Anhang Zf DSM 70506 Zm DSM 6959 Zr ATCC 48230 84 84 82 80 92 87 88 89 86 86 81 86 86 87 82 77 77 82 83 84 84 84 84 84 84 83 80 93 87 88 89 87 87 82 86 86 87 82 77 78 82 83 84 84 84 85 86 84 84 81 92 88 89 89 84 84 79 88 88 89 80 78 78 80 81 85 85 85 87 83 85 84 82 94 86 87 90 87 87 83 87 87 88 82 77 75 82 83 84 84 84 87 81 84 83 80 90 85 86 87 84 84 82 87 87 88 81 75 75 81 82 83 83 83 85 Kl AB018535 Km BCD 2563 Km BCD 5186 Io CBS 5147 Kl AB018535 Km BCD 2563 Km BCD 5186 Km BCD 811 Km DSM 70106 Km DSM 70792 Ku BCD 877 Le DSM 70320 Lt CBS 6340 Mp DSM 70321 Pa DSM 70277 Pan BCD 1082 Pan DSM 70783 Pc CBS 601 Pc DSM 70392 Pf BCD 861 Pfe BCD 711 Pfe DSM 70090 Pg BCD 804 Pm DSM 70178 Po BCD 862 Pp AB018536 100 93 93 92 100 98 97 100 97 100 94 98 98 97 100 91 96 98 95 96 100 93 98 100 97 98 98 100 90 92 92 91 94 90 92 100 86 84 84 83 84 82 84 82 100 90 94 94 94 95 92 94 94 84 100 89 89 90 88 90 88 90 84 85 88 100 94 92 94 91 92 92 94 89 88 89 87 100 88 86 86 86 88 84 86 87 86 87 84 88 100 88 86 86 86 88 84 86 87 86 87 84 88 100 100 94 90 90 89 92 88 90 88 87 87 90 91 89 89 100 84 84 84 83 84 82 84 82 92 84 84 83 84 84 84 100 89 87 87 86 88 85 87 84 89 87 87 89 85 85 88 86 100 96 93 94 92 94 93 94 90 85 90 88 94 88 88 92 84 89 100 Die verwendeten Abkürzungen entsprechen den Abkürzungen in der Abbildung 6.1. 122 96 89 89 88 91 87 89 86 83 86 85 90 84 84 90 81 85 93 100 91 89 89 90 90 87 89 85 91 88 89 89 89 89 90 90 93 91 87 100 94 90 92 89 92 90 92 89 84 88 86 92 86 86 90 83 86 97 90 88 100 82 79 79 80 80 77 79 78 89 81 81 83 81 81 82 85 85 81 78 88 80 100 Pp AB018536 Zbi DSM 70415 75 80 77 84 80 81 82 81 76 76 74 80 80 81 73 70 69 73 74 81 81 81 78 Po BCD 862 Zb BCD 1424 77 78 77 88 81 78 79 79 78 78 73 78 78 79 71 70 71 71 72 81 81 81 79 Pm DSM 70178 Yl BCD 2556 76 80 76 84 80 80 81 81 76 76 75 79 79 80 73 71 69 73 74 82 82 82 79 Pg BCD 804 Yl BCD 2003 83 82 80 80 89 84 85 86 84 84 80 84 84 84 76 77 74 76 77 86 86 86 87 Pfe DSM 70090 Yl AB018537 83 81 80 82 89 84 85 84 83 83 78 84 84 86 77 74 74 78 78 82 82 82 85 Pfe BCD 711 Td DSM 70607 84 84 81 82 93 85 86 88 88 88 83 85 85 86 81 77 74 83 82 84 84 84 86 Pf BCD 861 Sp DSM 6580 84 84 81 82 93 85 86 88 87 87 82 85 85 86 81 77 74 81 82 84 84 84 86 Pc DSM 70392 Se MUCL 29838 84 84 82 83 94 86 87 89 88 88 83 86 86 87 82 78 75 82 83 85 85 85 87 Pc CBS 601 Sd DSM 70487 74 74 73 70 77 76 77 76 69 69 66 75 75 74 73 69 65 73 73 70 70 70 71 Pan DSM 70783 Sd BCD 1257 74 74 73 70 77 76 77 76 69 69 66 75 75 74 73 69 65 73 73 70 70 70 71 Pan BCD 1082 Schp BCD 773 74 76 73 71 81 77 78 76 70 70 66 76 76 77 73 69 65 74 74 72 72 72 72 Pa DSM 70277 Schp AB018538 84 84 82 83 94 86 87 89 88 88 83 86 86 87 82 78 75 82 83 85 85 85 87 Mp DSM 70321 Scho DSM 70573 82 85 82 80 94 87 88 89 86 86 81 88 88 88 81 77 75 83 82 84 84 84 87 Lt CBS 6340 Sc DSM 1333 84 84 82 83 94 86 87 89 88 88 83 86 86 87 82 78 75 82 83 85 85 85 87 Le DSM 70320 Sp BCD 728 83 86 83 81 94 88 89 90 87 87 82 89 89 89 82 78 76 84 83 84 84 84 88 Ku BCD 877 Sc AB018539 83 82 80 80 89 84 85 86 84 84 80 84 84 84 76 77 73 76 77 86 86 86 87 Km DSM 70792 Sb DSM 70412 83 86 83 81 94 88 89 90 87 87 82 89 89 89 82 78 76 84 83 84 84 84 88 Km DSM 70106 Sb BCD 1392 Cso BCD 818 Ct BCD 819 Ctr ATCC 20326 Cv DSM 6956 Cvi DSM 70184 Cz AB018534 Cz BCD 690 De ATCC 20126 Dekb DSM 3429 Dekb DSM 70726 Dekc DSM 70736 Dh BCD 3512 Dh BCD 589 Dm ATCC 11627 Ef BCD 3514 Ef DSM 70554 Gs DSM 3431 Hb BCD 859 Hb DSM 3505 Hg DSM 70285 Hu ATCC 9774 Hu BCD 3526 Hv DSM 70283 Km BCD 811 Sb BCD 1256 Fortsetzung Io CBS 5147 Tab. 6.2: 95 94 94 94 94 92 94 91 85 91 89 93 91 91 91 84 89 94 92 91 91 81 100 6 Anhang Sb BCD 1392 Sb DSM 70412 Sc AB018539 Sp BCD 728 Sc DSM 1333 Scho DSM 70573 Schp AB018538 Schp BCD 773 Sd BCD 1257 Sd DSM 70487 Se MUCL 29838 Sp DSM 6580 Td DSM 70607 Yl AB018537 Yl BCD 2003 Yl BCD 2556 Zb BCD 1424 Zbi DSM 70415 Zf DSM 70506 Zm DSM 6959 Zr ATCC 48230 95 95 94 93 95 92 94 92 85 92 90 91 85 85 92 86 87 92 92 89 90 81 93 89 94 93 92 94 91 93 94 82 94 86 90 85 85 86 81 85 89 85 85 87 79 90 95 95 94 93 95 92 94 92 85 92 90 91 85 85 92 86 87 92 92 89 90 81 93 95 95 95 94 97 94 95 94 84 94 89 91 87 87 91 84 87 94 92 89 91 79 94 94 94 93 92 94 91 93 91 84 91 89 90 84 84 91 85 86 91 91 88 89 80 92 95 95 95 94 97 94 95 94 84 94 89 91 87 87 91 84 87 94 92 89 91 79 94 80 79 79 78 80 77 79 75 77 79 80 79 76 76 77 73 78 79 76 78 78 72 81 78 77 77 76 78 75 77 73 75 77 76 77 76 76 74 73 76 77 74 78 75 72 79 78 77 77 76 78 75 77 73 75 77 76 77 76 76 74 73 76 77 74 78 75 72 79 95 95 95 94 97 94 95 94 84 94 89 91 87 87 91 84 87 94 92 89 91 79 94 94 94 94 94 96 93 94 94 83 94 88 90 86 86 90 83 86 93 91 88 90 78 94 94 94 94 94 96 93 94 94 83 94 88 90 86 86 90 83 86 93 91 88 90 78 94 90 90 92 89 92 90 92 88 81 87 87 88 85 85 88 80 84 90 86 84 89 76 89 89 95 94 93 94 92 94 94 82 94 86 91 85 85 86 81 85 89 85 85 87 78 91 82 81 81 82 82 79 81 81 76 82 78 80 79 79 79 74 79 84 78 84 81 74 83 83 83 83 84 84 81 83 81 76 83 80 83 80 80 81 74 79 84 79 81 82 74 84 82 81 81 82 82 79 81 79 76 82 78 80 78 78 80 74 79 83 79 84 80 74 81 94 94 94 92 93 92 94 88 84 89 89 92 86 86 89 83 87 92 90 90 89 79 94 94 94 94 92 93 92 94 88 84 89 89 93 86 86 90 83 87 92 91 90 89 80 94 94 97 97 96 97 95 97 93 84 93 87 93 89 89 93 84 87 94 90 89 91 79 94 95 95 94 93 95 92 94 91 86 92 90 93 85 85 91 84 89 92 92 89 89 82 93 92 94 94 92 92 92 94 87 84 90 91 92 84 84 87 84 87 90 88 88 89 80 93 Sb BCD 1392 Sb DSM 70412 Sc AB018539 Sp BCD 728 Sc DSM 1333 Scho DSM 70573 Schp AB018538 Schp BCD 773 Sd BCD 1257 Sd DSM 70487 Se MUCL 29838 Sp DSM 6580 Td DSM 70607 Yl AB018537 Yl BCD 2003 Yl BCD 2556 Zb BCD 1424 Zbi DSM 70415 Zf DSM 70506 Zm DSM 6959 Zr ATCC 48230 Io CBS 5147 Kl AB018535 Km BCD 2563 Km BCD 5186 Km BCD 811 Km DSM 70106 Km DSM 70792 Ku BCD 877 Le DSM 70320 Lt CBS 6340 Mp DSM 70321 Pa DSM 70277 Pan BCD 1082 Pan DSM 70783 Pc CBS 601 Pc DSM 70392 Pf BCD 861 Pfe BCD 711 Pfe DSM 70090 Pg BCD 804 Pm DSM 70178 Po BCD 862 Pp AB018536 Sb BCD 1256 Fortsetzung Sb BCD 1256 Tab. 6.2: Sb BCD 1256 100 92 100 96 99 96 79 76 76 96 95 95 92 92 81 81 81 94 94 94 98 94 Sb BCD 1392 100 92 94 91 94 78 76 76 94 93 93 87 98 81 82 79 88 88 92 94 89 Sb DSM 70412 100 96 99 96 79 76 76 96 95 95 92 92 81 81 81 94 94 94 98 94 Sc AB018539 100 95 100 79 77 77 100 99 99 93 94 83 84 83 94 94 96 96 93 Sp BCD 728 100 95 78 75 75 95 94 94 91 91 80 80 80 93 94 94 97 94 Sc DSM 1333 100 79 77 77 100 99 99 93 94 83 84 83 94 94 96 96 93 Scho DSM 70573 100 96 96 79 78 78 77 78 68 69 68 78 78 77 80 78 Schp AB018538 100 100 77 76 76 74 76 67 70 67 76 76 75 78 76 Schp BCD 773 100 77 76 76 74 76 67 70 67 76 76 75 78 76 Sd BCD 1257 100 99 99 93 94 83 84 83 94 94 96 96 93 Sd DSM 70487 100 98 92 93 83 84 83 93 93 95 95 92 Se MUCL 29838 100 92 93 82 84 82 93 93 95 95 92 Sp DSM 6580 100 87 79 82 80 91 91 93 92 90 Td DSM 70607 100 81 84 79 89 89 93 94 90 Yl AB018537 100 86 95 82 82 82 81 80 Yl BCD 2003 100 85 81 81 85 83 81 Yl BCD 2556 100 82 82 83 81 80 Zb BCD 1424 100 99 94 94 93 Zbi DSM 70415 100 94 94 94 Zf DSM 70506 100 94 93 Zm DSM 6959 100 95 Zr ATCC 48230 100 Die verwendeten Abkürzungen entsprechen den Abkürzungen in der Abbildung 6.1. 123 6 Anhang 73 73 76 74 73 73 77 71 82 69 100 75 71 78 74 74 74 78 71 88 69 87 100 75 71 78 74 74 74 78 71 88 69 88 99 100 87 82 88 90 83 88 80 81 74 76 76 76 76 100 Sc AB018539 Trc DSM 70684 74 75 71 74 70 73 73 71 67 100 Spj DSM 70847 75 70 77 73 69 69 74 69 100 Spj BCD 778 86 78 81 86 86 83 82 100 Spj BCD 4982 81 81 80 87 80 77 100 Rm DSM 70408 Rg BCD 3530 88 75 82 86 89 100 Fn AF316889 82 75 82 86 100 Crh DSM 70067 Crf BCD 823 Crc DSM 70022 Crc BCD 2578 100 77 81 83 100 77 81 100 89 100 Crl BCD 824 Bd DSM 70745 Cra DSM 70197 Crc BCD 2578 Crc DSM 70022 Crf BCD 823 Crh DSM 70067 Crl BCD 824 Fn AF316889 Rg BCD 3530 Rm DSM 70408 Spj BCD 4982 Spj BCD 778 Spj DSM 70847 Trc DSM 70684 Sc AB018539 Cra DSM 70197 Distanz-Matrix: Prozentuale Übereinstimmung der EF-3 Aminosäuresequenzen innerhalb der Unterabteilung der Basidiomycota Bd DSM 70745 Tab. 6.3: 31 33 32 28 34 31 28 33 31 31 31 31 30 30 100 Die verwendeten Abkürzungen entsprechen den Abkürzungen in der Abbildung 6.1. 6.3 Real-Time RT-PCR 6.3.1 RNA-Extraktion RNA wurde wie im Kap. 2.6.1 beschrieben extrahiert und die Eluate anschließend mit DNase I [Sigma-Aldrich] behandelt. Hierzu wurden 35 µl des Eluats mit 4 µl 10 x Reaktionspuffer [Sigma-Aldrich] und 1 µl Amplification Grade DNase I [Sigma-Aldrich] versetzt und 30 min bei 37 °C inkubiert. Die Deaktivierung der DNase I erfolgte durch Zugabe von 4 µl Stop Solution [Sigma-Aldrich] und Inkubation bei 70 °C für 20 min. Die Proben wurden direkt in der RTPCR eingesetzt oder bei -20 °C gelagert. 6.3.2 Real-Time One-Step RT-PCR Alle Real-Time One-Step RT-PCR Versuche wurden mit einem LightCycler® 2.0 Instrument in 20 µl LightCycler® Kapillaren durchgeführt und mit der LightCycler® Software 4.0 ausgewertet [Roche Diagnostics]. Die spezifische Amplifikation der Target-cDNA wurde bei dem Einsatz von Hybridisierungssonden im Fluoreszenzkanal 640/Back 530 analysiert. Real-Time PCR-Reaktionen zur Kontrolle des DNase-Verdaus wurden mit SYBR®-Green I [Molecular Probes] durchgeführt und im Fluoreszenzkanal 530 ausgewertet. Die Real-Time RT-PCR Versuche wurden mit dem LightCycler® RNA Master HybProbe Kit [Roche Diagnostics] durchgeführt. Die Real-Time PCR-Reaktionen zur Kontrolle des DNase-Verdaus wurden mit den gleichen Reagenzien, wie im Kap. 2.13 beschrieben, durchgeführt. 124 6 Anhang 6.3.3 Real-Time One-Step RT-PCR-Programm Das One-Step RT-PCR-Programm mit Hybridisierungssonden bestand aus folgenden fünf Teilprogrammen: Teilprogramm RT Reaktion Denaturierung der cDNA Amplifikation Schmelzkurven-Analyse Kühlen Anzahl Zyklen 1 1 45 1 1 Analysis Mode None None Quantification Melting Curves None Die Teilprogramme hatten folgende Temperaturprofile: RT Reaktion Target Hold [°C] [hh:mm:ss] 61 00:20:00 Ramp Rate [°C/s] 20 Sec. Target [°C] 0 Denaturierung der cDNA Target Hold [°C] [hh:mm:ss] 95 00:00:30 Ramp Rate [°C/s] 20 Sec. Target [°C] 0 Amplifikation Target [°C] 95 55 72 Hold [hh:mm:ss] 00:00:01 00:00:30 00:00:15 Ramp Rate [°C/s] 20 20 20 Sec. Target [°C] 0 45 0 Schmelzkurven-Analyse Target Hold [°C] [hh:mm:ss] 95 00:00:00 40 00:01:00 70 00:00:00 Ramp Rate [°C/s] 20 20 0.1 Sec. Target [°C] 0 0 0 Kühlung Target [°C] 40 Ramp Rate [°C/s] 20 Sec. Target [°C] 0 Hold [hh:mm:ss] 00:00:30 Step Size [°C] 0 Step Size [°C] 0 Step Size [°C] 0 0.5 0 Step Size [°C] 0 0 0 Step Size [°C] 0 Step Delay [cycles] 0 Acquisition Mode None Step Delay [cycles] 0 Acquisition Mode None Step Delay [cycles] 0 10 0 Acquisition Mode None Single None Step Delay [cycles] 0 0 0 Acquisition Mode None None Continuous Step Delay [cycles] 0 Acquisition Mode None Das PCR-Programm mit SYBR®-Green I [Molecular Probes] zur Kontrolle des DNaseVerdaus bestand aus den folgenden vier Teilprogrammen: Teilprogramm Initiale Denaturierung Amplifikation Schmelzkurven-Analyse Kühlen Anzahl Zyklen 1 45 1 1 125 Analysis Mode None Quantification Melting Curves None 6 Anhang Die Teilprogramme hatten folgende Temperaturprofile: Initiale Denaturierung der cDNA Target Hold Ramp Rate [°C] [hh:mm:ss] [°C/s] 95 00:15:00 20 Sec. Target [°C] 0 Amplifikation Target [°C] 95 55 72 Hold [hh:mm:ss] 00:00:01 00:00:30 00:00:15 Ramp Rate [°C/s] 20 20 20 Sec. Target [°C] 0 45 0 Schmelzkurven-Analyse Target Hold [°C] [hh:mm:ss] 95 00:00:00 50 00:01:00 95 00:00:00 Ramp Rate [°C/s] 20 20 0.1 Sec. Target [°C] 0 0 0 Kühlung Target [°C] 40 Ramp Rate [°C/s] 20 Sec. Target [°C] 0 6.3.4 Hold [hh:mm:ss] 00:00:30 Step Size [°C] 0 Step Size [°C] 0 0.5 0 Step Size [°C] 0 0 0 Step Size [°C] 0 Step Delay [cycles] 0 Acquisition Mode None Step Delay [cycles] 0 10 0 Acquisition Mode None None Single Step Delay [cycles] 0 0 0 Acquisition Mode None None Continuous Step Delay [cycles] 0 Acquisition Mode None Real-Time One-Step RT-PCR-Ansätze Die One-Step RT-PCR wurde mit den Hybridisierungssonden und Primern für den Hefegesamtnachweis durchgeführt. Die Versuche wurden mit allen Sonden und Primern oder nur mit den in der folgenden Tabelle aufgeführten Sonden und Primern durchgeführt. Komponente LightCycler RNA Master HybProbe (2,7-fach) Mn(OAc)2 (50 mM) 3´-Primer-Mix HS11/I-IV (je 10 µM) 5´-Primer-Mix HT1r-3r (10 µM) LC-Fluorecein Sonde Yff1 (10 µM) LC-Red-640 Sonde Yfr4 (10 µM) Probe H2O Volumen 7,5 µl 1,3 µl 0,4 µl 0,8 µl 0,1 µl 0,4 µl 5,0 µl ad. 20 µl Endkonzentration 1x 3,25 mM 0,2 µM (je Primer) 0,4 µM (je Primer) 0,05 µM 0,2 µM Der Kontrollansatz mit SYBR®-Green I setzte sich wie folgt zusammen: Komponente 10 x PCR-Puffer MgCl2 (100 mM) dNTP-Mix (je 10 mM) BSA (30 µg/µl) 3´-Primer-Mix HS11/I-IV (je 10 µM) 5´-Primer-Mix HT1r-3r (10 µM) SYBR®-Green I (100-fach) Taq DNA Polymerase (5 U/µl) Probe H2O Volumen 2,0 µl 0,6 µl 0,4 µl 1,0 µl 0,4 µl 0,8 µl 0,1 µl 0,4 µl 5,0 µl ad. 20 µl 126 Endkonzentration 1x 3,0 mM 0,2 mM (je Nucleotid) 1,5 µg/µl 0,2 µM (je Primer) 0,4 µM (je Primer) 0,5-fach 2,0 U/Reaktion 6 Anhang 6.3.5 Ergebnisse der Real-Time One-Step RT-PCR Die Eignung der Primer und Hybridisierungssonden des Real-Time PCR Hefegesamtnachweissystems in der Real-Time One-Step RT-PCR wurde mit aufgearbeitetem YM-Medium (Kap. 6.3.1), das mit S. cerevisiae var. diastaticus (DSM 70487) dotiert wurde getestet. Bei diesen Experimenten zeigte sich, dass beim Einsatz aller Komponenten (Primer und Sonden) keine One-Step RT-PCR möglich war. In den Reaktionsansätzen wurden ausschließlich Primerdimere gebildet. Nach Reduktion der verwendeten Primer- und Sondenanzahl (siehe Kap. 6.3.4) konnten bis zu 102 Zellen/ml S. cerevisiae var. diastaticus mit der Real-Time One-Step RT-PCR nachgewiesen werden (Abb. 6.2). Nach Agarosegelelektrophorese wurden Amplifikate der gewünschten Länge detektiert (Abb. 6.3). Die Real-Time PCR mit SYBR®-Green zur Kontrolle der DNase Behandlung zeigte, dass keine DNA in den Proben vorhanden war (Abb. 6.4). Die mRNA des EF-3 Gens war demnach mit einem reduzierten System über Real-Time OneStep RT-PCR nachweisbar. Abb. 6.2: Real-Time One-Step RT-PCR Die Real-Time One-Step RT-PCR mit dem reduzierten Hefegesamtnachweissystem wurde mit aufgearbeitetem YM-Medium (Kap. 6.3.1) durchgeführt, das mit 106 Zellen/ml (grüne Linie), 105 Zellen/ml (rote Linie), 104 Zellen/ml (schwarze Linie), 103 Zellen/ml (blaue Linie) oder 102 Zellen/ml (rote Punkte) S. cerevisiae var. diastaticus (DSM 70487) dotiert war. Als Negativkontrolle (blaue Punkte) wurde undotiertes YM-Medium verwendet. 127 6 Anhang Abb. 6.3: Agarosegelelektrophorese nach Real-Time One-Step RT-PCR Die Real-Time One-Step RT-PCR mit dem reduzierten Hefegesamtnachweissystem wurde mit aufgearbeitetem YM-Medium (Kap. 6.3.1) durchgeführt, das mit S. cerevisiae var. diastaticus (DSM 70487) dotiert war. Die Agarosegelelektrophorese wurde anschließend mit 5 µl der Reaktionsansätze in einem 2-%igen Gel durchgeführt (Kap. 2.8). 1: Molekulargewichtsmarker VI 2: undotiertes YM-Medium 3: 106 Zellen/ml S. c. var. diastaticus 4: 105 Zellen/ml S. c. var. diastaticus 5: 104 Zellen/ml S. c. var. diastaticus 6: 103 Zellen/ml S. c. var. diastaticus 7: 102 Zellen/ml S. c. var. diastaticus Abb. 6.4: Schmelzkurven-Analyse zur Kontrolle des DNA Abbaus Der vollständige Abbau der DNA in den Proben für die Real-Time One-Step RT-PCR mit dem reduzierten Hefegesamtnachweissystem wurde mit einer Real-Time PCR mit SYBR®-Geen I überprüft. Mit S. cerevisiae var. diastaticus (DSM 70487) dotierte Proben: 106 Zellen/ml (grüne Linie), 105 Zellen/ml (rote Linie), 104 Zellen/ml (schwarze Linie), 103 Zellen/ml (blaue Linie) oder 102 Zellen/ml (rote Punkte); Negativkontrolle: undotierte Probe (blaue Punkte); Positivkontrolle: 250 pg S. cerevisiae var. diastaticus (DSM 70487) DNA (schwarze Punkte). 128