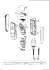Komplexe von Silber (l)-Salzen mit Naphthalino (cycIo) phanen
Transcrição
Komplexe von Silber (l)-Salzen mit Naphthalino (cycIo) phanen
Komplexe von Silber(l)-Salzen mit Naphthalino(cycIo)phanen, Strukturbestimmung von (rac-[2](l,5)Naphtha!ino[2]paracyclophan)-silber(I)-perchlorat Complexes of Silver(I) Salts with Naphthalino(cyclo)phanes, Structure Determination of (rac-[2](l,5)Naphthalino[2]paracyclophane)silver(I) Perchlorate H. Schmidbaur*, W. Bublak, M. W. Haenel + , B. Huber + + und G. Müller + + Anorganisch-Chemisches Institut der Technischen Universität München, Lichtenbergstraße 4. D-8046 Garching Herrn Prof. Dr. H. Nöth zum 60. Geburtstag gewidmet Z. Naturforsch. 43b, 7 0 2 - 7 0 6 (1988); eingegangen am 29. Januar 1988 Silver(I) A r e n e Complexes, Crystal Structure. Naphthalinocyclophane Complexes The 1:1 complexes of Ag[GaCl 4 ] with anti-[2.2\(\ ,4)naphthalinophane and of Ag[C10 4 ] with [2](1.4)naphthalino[2]paracyclophane and rac-[2](l,5)naphthalino[2]paracyclophane have been prepared and characterized by elemental analyses and IR spectra. The crystal structure of the last compound, ([2](l,5)naphthalino[2]paracyclophane)silver(I) Perchlorate, has been determined by X-ray methods. It crystallizes in the centrosymmetrical space group P2 Jn with cell dimensions a = 12.495(2), b = 8.546(1), c - 16.196(2) Ä , ß = 101.27(1)°. Both enantiomers of the ligands are present in the unit cell and related by centrosymmetry. Each silver atom is connected with the naphthalin systems of two ligands and with two Perchlorate anions, one of which is chelating, while the other is only monodentate. The cation/anion chains are linked through the organic ligands in such a way that a sheet structure is formed. The benzene rings of the cyclophanes are not involved in the metal coordination, the naphthaline rings are ty3-bonded to the silver atoms, which are not ringcentered. Einführung Die gute Löslichkeit einer Reihe von Salzen des einwertigen Silbers in aromatischen Kohlenwasserstoffen ist ein seit langem bekanntes Phänomen [1], So löst sich Silberperchlorat, wie auch andere Salze mit komplexen Anionen, gut in Benzol oder Toluol. Aus solchen Lösungen konnten kristalline Arenkomplexe, wie z.B. (C 6 H 6 )Ag[AlCl 4 ] [2], isoliert werden. Die Aromaten werden bei diesen Addukten, ähnlich wie Alkene, nur ^ ( j ^ - g e b u n d e n ; mit einem sehr schwach koordinierenden Carbaboranat-Anion konnte sogar erstmals ein ^'-Silber(I)-Arenkomplex dargestellt werden [3]. Der Grund für die geringe Haptizität der Ag(I)-Verbindungen mit der Elektronenkonfiguration d10s° liegt darin, daß das niedrigste Akzeptororbital des Metalls ein s-Orbital darstellt. Im Gegensatz dazu stehen die d I0 s 2 -konfigurierten Hauptgruppenmetall-Kationen, in denen die /^Orbitale die Rolle der LUMOs übernehmen (Ga 1 , In1, Tl1, Sn11, Pb"), und die entsprechend allesamt gegen Arene ^-Koordination aufweisen [4], Mit einfachen Aromaten ist inzwischen eine große Anzahl von Ag + -Komplexen charakterisiert worden. Aber auch kondensierte Systeme, wie z. B. Naphthalin, bilden Komplexe mit diversen Silber/AromatVerhältnissen (2:3, 1:1, 2:1, 4:1) [1]. Cyclophane mit kurzen Brücken zwischen den Arenringen und mit der daraus folgenden Anomalität der 7r-Systeme wurden als Arenliganden für Ag(I) erst kürzlich erprobt [5]. Eine Röntgenstrukturbestimmung wurde am Beispiel des ([3.3]Paracyclophan)silber(I)-tetrachlorogallat(III)-Komplexes durchgeführt. In diesem Komplex liegt ein metallorganisches Koordinationspolymeres mit Cyclophan-Silber-Ketten vor. Die Anionen ergänzen die Koordinationssphären der Metallzentren. In der hier vorgelegten Arbeit wird das Strukturprinzip polymerer Silber(I)-„Naphthalinophan"-Komplexe vorgestellt. * Sonderdruckanforderungen an Prof. Dr. H. Schmid- baur. ++ MPI für Kohlenforschung, 4330 Mülheim a . d . R u h r . Röntgenstrukturanalyse. Verlag der Zeitschrift für Naturforschung. D-7400 Tübingen 0932-0776/88/0600-0702/$ 01.00/0 Ergebnisse und Diskussion N a p h t h a l i n o ( c y c l o ) p h a n e b i l d e n leicht K o m p l e x e mit d i v e r s e n S i l b e r s a l z e n , d i e in g ä n g i g e n S o l v e n t i e n s t e t s s c h w e r löslich s i n d u n d d u r c h g e h e n d d i e g l e i c h e Dieses Werk wurde im Jahr 2013 vom Verlag Zeitschrift für Naturforschung in Zusammenarbeit mit der Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. digitalisiert und unter folgender Lizenz veröffentlicht: Creative Commons Namensnennung-Keine Bearbeitung 3.0 Deutschland Lizenz. This work has been digitalized and published in 2013 by Verlag Zeitschrift für Naturforschung in cooperation with the Max Planck Society for the Advancement of Science under a Creative Commons Attribution-NoDerivs 3.0 Germany License. Zum 01.01.2015 ist eine Anpassung der Lizenzbedingungen (Entfall der Creative Commons Lizenzbedingung „Keine Bearbeitung“) beabsichtigt, um eine Nachnutzung auch im Rahmen zukünftiger wissenschaftlicher Nutzungsformen zu ermöglichen. On 01.01.2015 it is planned to change the License Conditions (the removal of the Creative Commons License condition “no derivative works”). This is to allow reuse in the area of future scientific usage. H. Schmidbaur et al. • Komplexe von Silber(I)-Salzen mit Naphthalino(cyclo)phanen l:l-Stöchiometrie wie die bekannten CyclophanKomplexe aufweisen. So liefert a/?r/-[2.2](l,4)Naphthalinophan (1) [6] mit Ag[GaCl 4 ] den l:l-Komplex 2. Silberperchlorat wurde mit den zwei Isomeren Ag(GaClJ 1 [2](l,4)Naphthalino[2]paraeyclophan (3) und (racemischem) [2](l,5)Naphthalino[2]paraeyclophan (5) [7] zu den Komplexen 4 bzw. 6 umgesetzt. Die Versuche erfolgten vorsichtshalber unter Kühlung in Toluol, da solche Arenkomplexe häufig wenig stabil sind [8]. AgtCIOJ • Toluol (C 2 0 H 1 8 )Ag [ C 1 0 J K Ag [C104 ] (C 2 0 H, 8 )Ag[ClO 4 ] 6 Die Komplexe 2 und 4 sind bisher nur durch Elementaranalysen und IR-Spektren belegt. Von 6 wurden jedoch auch für die Röntgenstrukturanalyse geeignete Einkristalle erhalten. Das Produkt ([2](l,5)Naphthalino[2]paracyclophan)silber(I)-perchlorat (6) kristallisiert in der zentrosymmetrischen Raumgruppe P2 x ln. Daraus folgt unmittelbar, daß beide Enantiomere von 5 zusammen in den Kristall des Komplexes 6 eingebaut werden. Die Strukturbestimmung ergab wiederum die Konstitution eines Koordinationspolymeren. Es liegen Kation-Anion-Ketten vor, die mit denen im (Cyclohexylbenzol) 2 Ag[C10 4 ] vergleichbar sind [9]. Die Stränge werden an den Silberatomen über Naphthalinocyclophan-Moleküle miteinander vernetzt 703 (Abb. 1). Jede Kette ist abwechselnd zur einen und zur anderen Seite hin koordiniert, so daß ein Schichtengitter entsteht. Als Aren-Donor für die Silberatome wirkt jeweils nur die Naphthalineinheit, während die Benzolringe der Cyclophane keinerlei Wechselwirkung mit den Silberatomen eingehen (Abb. 1). Die erste Koordinationssphäre der Silberatome wird aus drei Sauerstoffatomen ( O l ' , 0 2 , 0 3 ) , von denen zwei chelatisierend wirken ( 0 2 , 0 3 ) , sowie zwei jr-Systemen von verschiedenen Naphthalineinheiten gebildet. Zu letzteren existieren je zwei kurze (Ag-C9/C 10: 2,406(4)/2,552(4) Ä; Ag"-C17/C18: 2,365(4)/2,608(4) Ä) und je eine längere Bindung (Ag-C 14/Ag"-C 16: 2,979(4)/2,950(4) Ä). Die Koordination kann demnach näherungsweise als r]Vif beschrieben werden. Es fällt allerdings auf (Abb. 1), daß die Verbindungslinien zwischen den Ag-Atomen und den Mittelpunkten der an sie koordinierten Doppelbindungen einen Winkel von 144,5° bilden, der von der Ebene der drei koordinierten O-Atome in etwa halbiert wird. Vergleichbare Geometrien, wenn auch mit kleineren Interaren-Winkeln werden u. a. bei einer Vielzahl von Aren-Komplexen der niedervalenten Metalle der 13. Gruppe gefunden. Beim ([3.3]Paracyclophan)silber-tetrachlorogallat wird dagegen eine wesentlich symmetrischere ^/^'-Koordination zweier Doppelbindungssysteme an ein Ag + Ion beobachtet [5]. Die Koordinationsgeometrie am Silber ist irregulär, und die Beschreibung kann sich nur sehr schwer an idealen Polyedern orientieren, wobei allerdings die drastischen Unterschiede in den Ag—C-Bindungslängen nicht übersehen werden sollten. Die C—C-Bindungslängen des [2](l,5)Naphthalino[2]paracyclophans im Komplex 6 entsprechen weitgehend denen des freien Naphthalins bzw. Benzols (Abb. 2). Die Silberatome koordinieren dabei bezeichnenderweise nur an die kürzeren C—C-Struktureinheiten des Naphthalins. Der Benzolteil des Cyclophans bleibt, wie erwähnt, von einer SilberWechselwirkung ausgespart. Hier zeigen sich erhebliche Unterschiede zu dem ([2](l,4)Naphthalino[2]paracyclophan)gallium(I)-Komplex [10], Das niederwertige Hauptgruppenmetall bildet zum ideal aromatischen Benzolring eine stärkere Bindung aus als zum mehr alkenartigen Naphthalinsystem. Silber(I) (und Kupfer(I)) koordinieren demnach bevorzugt an die C—C-Einheiten mit dem größten Doppelbindungscharakter. 704 H. Schmidbaur et al. • Komplexe von Silber(I)-Salzen mit Naphthalino(cyclo)phanen 704 Abb. 1. Kristallstruktur von 6: Projektion auf die a,c-Ebene. Die [AgC10 4 ]-Baueinheiten bilden Stränge mit kristallographischer 2 r S y m m e t r i e , die sich parallel zur fr-Achse durch den Kristall ziehen (senkrecht zur Papierebene). Sie sind über zwei Naphthalinophane pro Silberatom untereinander verknüpft, die um ein Symmetriezentrum angeordnet sind. Das daraus resultierende Schichtengitter wird senkrecht zur 2 r A c h s e durch die Gleitebene n aufgebaut. OW Abb. 2. Molekülstruktur des Naphthalinophans in 6 mit den beiden daran koordinierten [AgC10 4 ]-Einheiten ( O R T E P . Schwingungsellipsoide 50%, ohne HAtome). Es sind jeweils nur die Linien von den Ag-Atomen auf die Mittelpunkte der Bindungen zwischen den beiden nächsten C-Atomen eingezeichnet. 705 H. Schmidbaur et al. • Komplexe von Silber(I)-Salzen mit Naphthalino(cyclo)phanen Die Perehlorat-Anionen besitzen in 6 nahezu ideale Tetraedergeometrie (Tab. I). Auffallend ist der etwas kleinere Winkel 0 2 - C 1 - 0 3 (107,1(2)°), der aber unmittelbar auf die Chelatbildung zurückzuführen ist. Die Abstände C 1 - 0 1 / 0 2 / 0 3 sind innerhalb der Standardabweichung gleich (1,445(3); 1,440(3); 1,446(3) Ä); nur 0 4 ist stärker an Chlor gebunden (1,406(3) Ä), da es keine zusätzliche Kontaktfunktion zu Silber ausübt. Diese deutlichen strukturellen Konsequenzen des unterschiedlichen Donor-Verhaltens der O-Atome sind um so bemerkenswerter, als das Perchlorat-Ion in der Regel nur äußerst schwach koordinierend auftritt. führt. Ag[GaCl 4 ] wurde aus GaCl 3 und AgCl in Benzol dargestellt, AgC10 4 wurde von der Riedel-deHaen A G bezogen und ohne weitere Reinigung eingesetzt. Experimenteller Teil Analyse für C24H20AgCl4Ga (627,82) ' Ber. C 45,91 H 3,21 Ag 17,18, Gef. C 44,82 H 3,08 Ag 17,2. Die Umsetzungen wurden unter Ausschluß von Luft, Licht und Feuchtigkeit mit entsprechend vorbehandelten Geräten und Lösungsmitteln durchge- Tab. I. Wichtige Abstände (Ä) und Winkel (°) in der Struktur von 6. (Siehe Abb. 2 für die verwendete Atomnumerierung.) Ag-C9 Ag—C10 Ag—C14 Ag-02 Ag—03 Ag—Ol' C1-C2 C2-C3 C3-C4 C1-C7 C7-C8 C8-C9 C9-C10 C10-C11 C11-C12 C14-C15 C13-C18 C16-C17 Cl-Ol C1-03 2,406(4) 2,552(4) 2,979(4) 2,776(3) 2,653(4) 2,567(3) 1,391(6) 1,389(6) 1,395(6) 1,512(5) 1,566(6) 1,530(5) 1,367(6) 1,425(6) 1,363(6) 1,425(5) 1,454(5) 1,421(5) 1,445(3) 1,446(3) D 1 —Ag—D2" Dl-Ag-Ol' D 1—Ag—03 D 1—Ag—02 D2—Ag—Ol' D2—Ag—03 D2—Ag—02 0 1 ' —Ag—03 03—Ag—02 144,8 90,5 113,0 106,6 109,4 101,7 90,5 66,4 50,6(1) C17 —Ag" C18—Ag" C16—Ag" Ag—D l a D2-Ag" 2,365(4) 2,608(4) 2,950(4) 2,38 2,39 C1-C6 C5-C6 C4-C5 C4-C20 C19-C20 C18—C19 C9-C14 C13-C14 C12-C13 C15-C16 C17-C18 1.407(6) 1,390(6) 1,387(6) 1,526(6) 1,564(6) 1,512(5) 1,449(5) 1,427(5) 1,413(5) 1,350(5) 1,381(5) Cl-02 C1-04 1,440(3) 1,406(3) Ol—Cl—02 Ol—Cl —03 O l —Cl—04 02-C1-03 02-C1-04 03-C1-04 109,0(2) 109,3(2) 110,2(2) 107,1(2) 110,7(2) 110,3(2) a D 1 / D 2 = Mittelpunkte der Bindungen C 9 - C 1 0 / C17—C18. Symmetrieoperationen: O l ' : 0,5—x, 0,5+_y, 0,5—z; Ag", D2": -y, -z. (anti-[2.2](l ,4)Naphthalinophan)silber(I)tetrachlorogallat(III) (2) 15,6 mg anti-[2.2](l,4)Naphthalinophan (1) (50,6 ^mol) werden zusammen mit 16,3 mg Ag[GaCl 4 ] (51,0 ^mol) in 15 ml Toluol zum Sieden erhitzt. Beim Abkühlen bildet sich ein farbloser, mikrokristalliner Niederschlag, der mit 2 x 2 ml Benzol gewaschen und im Vakuum getrocknet wird. Ausbeute 90%, Fp. 232 °C. ([2](l,4)Naphthalino[2]paracyclophan)silber(I)perchlorat (4) Zu 11,7 mg Ag[C10 4 ] (56,4 pmo\) in 1,5 ml Toluol werden 14,7 mg [2](l,4)Naphthalino[2]paracyclophan (3) (56,9 //mol), gelöst in 2 ml Toluol, zugetropft. Die Mischung wird sofort trüb. Nach einiger Zeit setzt sich ein Niederschlag ab, der abgetrennt und getrocknet wird. Ausbeute > 9 5 % , Fp. 132 °C (Zers.). IR (Nujol, Csl): 620 s, 690 sh, 770 s, br, 800 s, 890 s, br, 1010 vs, br, 1120 vs, br. Analyse für CwH18AgCl04 (465,68) Ber. C 51,58 H 3,89 Cl 7,61, Gef. C 49,59 H 3,93 Cl 7,6. ([2](1,5)Naphthalino[2 Perchlorat (6) Jparacyclophan ) silber (I) - 17,3 mg (67,0 //mol) des racemischen Gemisches von [2](l,5)Naphthalino[2]paracyclophan (5) werden in 2 ml Toluol gelöst und mit einer Lösung von 13,9 mg Ag[C10 4 ] (67,0 //mol) in 0,5 ml Toluol vereinigt. Die Mischung bleibt zunächst klar, bis sich nach 1 d ein mikrokristalliner Niederschlag bildet, aus dem sich beim Stehen für die Strukturanalyse geeignete Kristalle bilden. Ausbeute 80%, Fp. 139-142 °C (Zers.). IR (Nujol/Csl): 565 m, 582 w, 615 s, 725 sh, 735 s, 890 s, 843 m, 900 s, br, 1010 vs, br, 1120 vs, br. Analyse für C20Hl8AgClO4 (465,87) Ber. C 51,58 H 3,89 Ag 23,16, Gef. C 49,22 H 3,74 Ag 23,17. 706 Röntgenstrukturanalyse H. Schmidbaur et al. • Komplexe von Silber(I)-Salzen mit Naphthalino(cyclo)phanen 706 von Verbindung 6 Kristallstrukturdaten: Syntex-P2rDiffraktometer, M o K a - S t r a h l u n g , X = 0,71069 Ä , G r a p h i t - M o n o chromator, T = - 3 5 ° C C:0H18AgClO4, Mr = 4 6 5 , 6 7 , m o n o k l i n , R a u m g r u p p e P 2 x / n , N r . 14, a = 1 2 , 4 9 5 ( 2 ) , b = 8 , 5 4 6 ( 1 ) , c = 16,196(2) Ä , ß = 101,27(1)°, V = 1696,1 Ä 3 , Z = 4, D b e r = 1,823 g e r n - 3 , ^ ( M o K a ) = 13,6 c m " 1 , F ( 0 0 0 ) = 9 3 6 e . Die gemessenen integrierten Intensitäten von 2998 Reflexen wurden für Lp-Effekte und empirisch für A b s o r p t i o n k o r r i g i e r t (rel. T r a n s m i s s i o n : 0,79— 1,00). N a c h Mittelung äquivalenter D a t e n verblieben 2663 u n a b h ä n g i g e S t r u k t u r f a k t o r e n (Rml = 0 , 0 2 ) , v o n d e n e n 2 1 8 1 m i t F 0 > 4,0ct(F o ) als „ b e o b a c h t e t " e i n g e s t u f t u n d f ü r alle w e i t e r e n R e c h n u n g e n v e r w e n d e t w u r d e n . D i e S t r u k t u r w u r d e mit a u t o m a t i s i e r t e n P a t t e r s o n - M e t h o d e n gelöst ( S H E L X S - 8 6 [11]) u n d m i t F o u r i e r - S y n t h e s e n v e r v o l l s t ä n d i g t . A l l e 18 H A t o m e konnten nach anisotroper Verfeinerung der N i c h t - H - A t o m e in D i f f e r e n z - S y n t h e s e n l o k a l i s i e r t werden. Die anisotrope Verfeinerung konvergierte b e i R(RW) = 0 , 0 3 3 ( 0 , 0 3 2 ) , w = l / c r ( F 0 ) (235 v e r f e i n e r t e P a r a m e t e r , H - A t o m e k o n s t a n t mit U , i 0 = 0 , 0 5 Ä 2 , R e f l e x 101 u n t e r d r ü c k t , S H E L X - 7 6 [12]). D a s m a x i m a l e V e r h ä l t n i s s h i f t / e r r o r im l e t z t e n Z y k l u s w a r 0 , 0 0 1 , die m i n i m i e r t e F u n k t i o n Z w ( | F 0 | — |F C |) 2 . D i e R e s t e l e k t r o n e n d i c h t e z e i g t e k e i n e A n o m a lien: Ag Xm ( m a x . / m i n . ) = 0 , 6 5 / - 0 , 5 9 e / Ä 3 , mit d e n M a x i m a an A g . T a b . I enthält wichtige A b s t ä n d e u n d W i n k e l , T a b . II die A t o m k o o r d i n a t e n . A b b . 1 u n d 2 z e i g e n A u s s c h n i t t e a u s d e r Kristall- u n d M o l e - [1] Gmelin, Handbuch der Anorganischen Chemie, Silberorganische Verbindungen, 8. Aufl., Silber, Teil B 5 , Springer-Verlag, Berlin (1975). [2] R. W. Turner und E. L. A m m a , J. A m . Chem. Soc. 88, 3243 (1966). [3] K. Shelly, D. C. Finster, Y. J. Lee, R. Scheidt und C. A. Reed, J. Am. Chem. Soc. 107, 5955 (1985). [4] H. Schmidbaur, Angew. Chem. 97, 893 (1985); Angew. C h e m . , Int. Ed. Engl. 24, 893 (1985). [5] H. Schmidbaur, W. Bublak, B. H u b e r . G. Reber und G. Müller, Angew. Chem. 98, 1108 (1986); Angew. Chem., Int. Ed. Engl. 25, 1089 (1986). [6] M. W. Haenel. Chem. Ber. 115, 1425 (1982). [7] P. M. Keehn und S. M. Rosenfeld (Herausg.): Cyclophanes. Vol. I und II, Acad. Press, New York, London (1983). [8] A. E. Hill und F. W. Miller, J. A m . Chem. Soc. 47, 2702 (1925). külstruktur. Weitere h i n t e r l e g t [13]. Kristallstrukturdaten wurden Tab. II. Fraktionelle Atomkoordinaten und äquivalente, isotrope Temperaturfaktoren für 6 (U e q = ( U I U 2 U 3 ) ' \ wobei Uj die Eigenwerte der Ujj-Matrix sind). Atom Ag Cl Ol 02 03 04 Cl C2 C3 C4 C5 C6 C7 C8 C9 C10 Cll C12 C13 C14 C15 C16 C17 C18 C19 C20 x/a 0.1539(1) 0,1108(1) 0,1649(3) 0,0376(3) 0.1910(3) 0,0538(3) 0.2926(3) 0,3362(3) 0.2808(3) 0,1802(3) 0.1440(3) 0,1989(3) 0,3331(4) 0,2590(3) 0,2161(3) 0,2838(3) 0.2631(3) 0,1800(3) 0,1065(3) 0.1156(3) 0,0280(3) -0.0587(3) -0,0568(3) 0,0253(3) 0.0477(3) 0,1017(4) y/b -0,0079(1) -0,2898(1) -0,4367(3) -0,2547(4) -0,1658(4) -0,2980(4) -0.4057(5) -0,2938(5) -0,2464(5) -0,3125(5) -0,4386(5) -0,4865(5) -0,4171(5) -0,3230(5) -0,1741(5) -0,0486(5) 0,0674(5) 0,0453(4) -0,0807(5) -0,1802(4) -0,2834(5) -0,2965(5) -0,2234(5) -0.1209(4) -0,0849(5) -0,2307(5) z/c 0,1410(1) 0,2700(1) 0,2615(2) 0,1919(2) 0.2848(2) 0.3366(2) -0.0564(2) -0,1027(2) -0,1816(2) -0,2169(2) -0,1760(3) -0.0970(2) 0,0377(3) 0,0877(2) 0,0402(2) 0,0393(2) -0.0251(3) -0,0923(2) -0,0937(2) -0,0219(2) -0,0159(2) -0,0799(2) -0,1584(2) -0,1679(2) -0,2544(2) -0,2878(2) ueq 0,028 0,022 0,031 0,035 0,041 0,043 0,023 0,026 0,026 0,022 0,025 0,026 0,030 0,025 0.020 0,023 0,026 0,022 0.018 0,018 0,023 0,023 0.021 0.021 0.025 0.030 [9] E. L. A m m a und E. A. Griffith, J. Am. Chem. Soc. 93, 3167 (1971). [10] H. Schmidbaur. W. Bublak, B. H u b e r und G. Müller. Z . Naturforsch. 42b, 147 (1987). [11] G. M. Sheldrick. in G. M. Sheldrick, C. Krüger und R. G o d d a r d (Herausg.): Crystallographic Computing 3, S. 175, Oxford University Press, Oxford (1985). [12] G. M. Sheldrick, SHELX-76, Program for Crystal Structure Determination. Univ. Cambridge, England (1976). [13] Fachinformationszentrum Energie, Physik, Mathematik G m b H , D-7514 Eggenstein-Leopoldshafen 2. Anforderungen sollten unter Angabe der Hinterlegungsnummer CSD 52896. der Autoren und des Zeitschriftenzitats erfolgen.