Baixe o caderno
Transcrição
Baixe o caderno
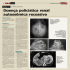
Caderno2 Este encarte é parte integrante da edição 426 do Jornal da Imagem | Fevereiro de 2014 Apoio HOSPITAIS SÃO FRANCISCO E BENEFICÊNCIA PORTUGUESA CASO 1 HOSPITAL BENEFICÊNCIA PORTUGUESA Caso recebido em 23 de janeiro de 2014 A História clínica Paciente masculino, 45 anos, com história pregressa de insuficiência renal crônica (IRC), com transplante renal há cerca de 9 anos, apresentando tosse e dispneia. Figura 2 Reconstrução coronal MIP com janela de pulmão demonstrando os mesmos achados da Figura 1 B Figura 1 TC de tórax: cortes axiais (A e B) demonstrando opacidades nodulares centrolobulares nos lobos superiores, com calcificações associadas, predominando à direita Figura 4 A B Figura 3 Imagens de cintilografia com MDC99Tc demonstrando captação do radiofármaco no lobo superior direito (setas) Imagens de TC sem contraste no plano axial (A) e coronal (B) com janela de partes moles evidenciando calcificações vasculares na parede torácica anterior (setas) CASO 2 HOSPITAL SÃO FRANCISCO Caso recebido em 23 de janeiro de 2014 História clínica Feminino, 43 anos, se apresentou a emergência do hospital com hemicoreia à direita, sem antecedentes patológicos. Hemograma: normal, Glicemia: 831 mg/dl. Figura 1 Imagem de RM ponderada em T2 demonstrando baixo sinal nos núcleos estriados, mais evidente à esquerda Figura 4 Imagem de RM ponderada em T1, com contraste, demonstrando o alto sinal mais evidente no núcleo estriado esquerdo, sem realce pelo agente paramagnético Figuras 2 e 3 Imagens de RM ponderadas em T1, demonstrando alto sinal nos núcleos estriados CASO 1 Autores: Drs. Eduardo Marques da Rocha Trevisan, Pablo Rydz Pinheiro Santana, Ana Paula Santos Lima, Antônio Carlos Portugal Gomes – Med Imagem – H. Beneficência Portuguesa Calcificação Pulmonar Metastática Calcificação pulmonar metastática (CPM) é uma doença incomum caracterizada por depósito de sais de cálcio em tecidos normais, sendo o pulmão o órgão mais suscetível. Está relacionada a alterações no metabolismo do cálcio e do fósforo, que podem ser decorrentes de causas benignas como hiperparatireoidismo primário, hipervitaminose D, doença de Paget e osteopetrose; ou malignas, como mieloma múltiplo, linfomas e leucemia. Entretanto, a maioria dos casos ocorre em pacientes com insuficiência renal crônica, especialmente aqueles em hemodiálise. A CPM é usualmente assintomática. Entretanto, alterações da função pulmonar podem ser vistas, como pneumopatia restritiva e mais raramente insuficiência respiratória. Em geral, as manifestações clínicas não apresentam CASO 2 correlação com a extensão do acometimento pulmonar. A radiografia convencional de tórax normalmente não evidencia alterações, e quando presentes, são inespecíficas, sendo a tomografia computadorizada de alta resolução (TCAR) o melhor método de imagem para avaliação da CPM. Os achados mais comuns na TCAR são formações nodulares mal definidas com atenuação em vidro fosco de distribuição predominantemente centrolobular, medindo entre 3 e 10 mm, que tendem a ser mais numerosas nos lobos superiores, e exibem calcificações em cerca de 60% dos casos. Menos comumente, essas opacidades podem exibir um padrão difuso ou envolver os lobos inferiores. Calcificações vasculares na parede torácica são frequentes, tipicamente entre os músculos peitorais maior e menor. A Cintilo- grafia com MDC99Tc auxilia no diagnóstico, pois pode confirmar a natureza cálcica das lesões. O paciente apresentava alterações dos níveis séricos de cálcio e fosfato (Cálcio ionizado 1,48 mMol/L e Fósforo 9,7 mg/dL). Os achados de imagem demonstravam opacidades centrolobulares comprometendo os lobos superiores, algumas exibindo pequenos componentes cálcicos, além de calcificações vasculares na parede torácica anterior. Estes achados não apresentaram alterações significativas em exames de controle subsequentes. Foi realizada também cintilografia pulmonar com MDC99Tc, que apresentou captação do radiofármaco nas lesões, notadamente à direita. O tratamento se baseia na correção das causas de hipercalcemia e hiperfosfatemia, normalmente decorrentes de IRC. Eventual- mente, a CPM pode resolver sem tratamento. Concluindo, CPM deve ser considerada no diagnóstico diferencial de opacidades centrolobulares difusas em pacientes com distúrbio do metabolismo do cálcico e fósforo, principalmente relacionado à IRC. Referências Bibliográficas: 1.Marchiori E., Souza Jr A.S., Franquet, T., Müller, N.L. Diffuse High-Atenuation Pulmonary Abnormalities: A Pattern-Orientede Diagnostic Aproach on High Resolution CT – AJR 2005;184;273-282. 2.Bozi, L.C.F.; de Melo, A.S.A., Marchiori E. Calcificação pulmonar metastática: relato de caso - Radiol Bras. 2012 Set/ Out;45(5):297-299. 3.Hartman, T.E., Müller, N.L., Primack, S.L., et al. Metastatic Pulmonary Calcification in Patients with Hypercalcemia: Findings on Chest Radiographs and CT Scans - AJR 1994;162:799-802. Autores: Drs. Gabriel P. Coelho, Lenara R. A. Coelho, Fernanda F. Brusasco, Paula P. Costa. Orientador: Lucas G. Abud Serviço: Documenta – Hospital São Francisco Síndrome hemibalismo-hemicoreia associada à hiperglicemia “Diabetic Striatal Disease” Síndrome caracterizada pela presença de alto sinal confinado ao núcleo estriado, nas sequências ponderadas em T1 da Ressonância Magnética e distúrbios do movimento hipercinéticos contralaterais em pacientes diabéticos. A tomografia computadorizada pode demonstrar hiperdensidade nesta região. Uma variedade de anomalias neurológicas está associada com hiperglicemia não cetótica em pacientes diabéticos, incluindo função mental prejudicada, crises convulsivas parciais e generalizadas e déficits neurológicos focais. 2 | Caderno 2 Coreia e balismo podem resultar de uma variedade de condições, incluindo doenças cerebrovasculares, infecções, drogas, alterações metabólicas, doenças neurodegenerativas, desordens imunológicas e tumores, bem como hiperglicemia não cetótica em diabetes mellitus primária. Hiperglicemia não cetótica é uma causa incomum de coreia-balismo, e coreia-balismo também é uma rara manifestação de diabetes mellitus primária. Notavelmente, dormência e fraqueza podem aparecer antes do desenvolvimento da coreia, su- gerindo que a coreia é, por vezes, uma manifestação clínica tardia da lesão do núcleo estriado. O reconhecimento desta doença é importante porque é uma doença tratável e com um bom prognóstico. Apenas alguns pacientes com esta síndrome foram submetidos a estudos patológicos post-mortem ou biópsias e os resultados demonstraram perda seletiva neuronal, gliose, astrocitose reativa e hemorragia. O núcleo estriado é conhecido por ser um alvo seletivo de diversas doenças neurológicas, por exemplo, Doença de Huntington, doença de Hallervorden-Spatz e cirrose. Outros diagnósticos diferenciais incluem toxicidade pelo manganês na nutrição parenteral em longo prazo, problemas do metabolismo do cálcio, doença de Wilson, neurofibromatose e hipóxia. Referências bibliográficas 1.Abe, Y., et al. Diabetic Striatal Disease: Clinical Presentation, Inter Med 48: 1135-1141, 2009. 2.Lai, PH, et al. Chorea-Ballismus with Nonketotic Hyperglycemia in Primary Diabetes Mellitus, AJNR Am J Neuroradiol 17:1057–1064, June 1996. CASO 3 HOSPITAL SÃO FRANCISCO Caso recebido em 23 de janeiro de 2014 História clínica Masculino, 53 anos, assintomático, realizou Raio-X de tórax para liberação de atividade física. Sem antecedentes patológicos, nega tabagismo. Hemograma: normal, Proteinúria de Bence-Jones: Negativa, Eletroforese de Proteínas: normal, Aspirado de Medula Óssea: ausência de plasmocitose. Figura 1 Raios X de tórax em PA demonstrando massa perihilar à direita Figura 2 Figura 3 Figura 4 Imagem de TC em corte axial, janela pulmonar, demonstrando massa perihilar à direita, sem alterações nos campos pulmonares Imagem de TC em corte axial, sem contraste, demonstra formação expansiva arredondada com densidade de partes moles em região hilar direita Imagem de TC em corte axial, com contraste, mostrando o importante realce após administração do contraste EV e o íntimo contato com a artéria pulmonar direita CASO 4 HOSPITAL BENEFICÊNCIA PORTUGUESA Caso recebido em 23 de janeiro de 2014 História clínica A B C D Feminino, 7 meses de idade, com quadro de massa abdominal palpável. Figura 1 Tomografia computadorizada sem contraste endovenoso (cortes axiais), demonstrando aumento do volume renal bilateral A B C D Figura 2 Tomografia computadorizada após a injeção intravenosa do contraste, evidenciou lesões hipoatenuantes, com discreta impregnação e determinam compressão do parênquima renal adjacente Edição 426 – Fevereiro de 2014 | 3 CASO 3 Autores: Drs. Lenara R. A. Coelho, Gabriel P. Coelho, Fernanda F. Brusasco, Lara Z. Lauar. Orientador: Marcus Vinicius Valentin. Serviço: Documenta – Hospital São Francisco Plasmocitoma Extramedular Plasmocitoma extramedular é uma doença rara (3% dos tumores de células plasmáticas), caracterizada histopatologicamente por infiltrado de células plasmáticas de maturidades diversas e produtoras de imunoglobulina monoclonal fora da medula óssea. Sua incidência aumenta com a idade, sendo mais comum em homens do que em mulheres, em uma proporção 4:1. Acomete com maior frequência a região da cabeça e pescoço, sendo o trato respiratório superior representado por 78 a 85% dos casos. Outros locais incluem: trato gastrointestinal, bexiga, sistema nervoso central, tireoide, mama, testículos, parótida, linfonodos e pele. Plasmocitoma primário dos linfonodos é muito raro (2% dos Plasmocitomas Extramedulares) e o prognóstico é melhor que em outros sítios. O comprometimendo de linfonodos hilares é ainda mais infrequente, com poucos casos relatados na literatura. A recorrência é rara e não costuma progredir para mieloma múltiplo após o tratamento. O diagnóstico baseia-se na biópsia da lesão e no encontro de CASO 4 tumor monoclonal de plasmócitos extramedular excluindo-se mieloma múltiplo. Os achados anatomopatológicos incluem: massas hipercelulares de células plasmocitoides monótonas bem diferenciadas, com núcleos pequenos, excêntricos e hipercromáticos e a imunohistoquímica demonstra anticorpos positivos CD138 e Lambda. Devido à radiosensibilidade do tumor, a radioterapia é peça central na terapêutica, porém, ainda se discute dose e necessidade de irradiação de linfonodos regionais. Cirurgia é tratamento de primeira escolha e quimioterapia continua sendo controversa. Referências bibliográficas 1.Henriques, A. C, et al. Plasmocitoma extramedular. Arq. Med. ABC, v. 30, n. 1, jun 2005. 2.Iwata, H., et al. Extramedullary Plasmacytoma from The Hilar Lymphnode-One Case Report. Journal of the Japanese Association for Chest Surgery, Vol.18; n° 2; pg.136-140(2004). 3.Keisuke, N., et al. Excision of Extramedullary Plasmacytoma in a Hilar Lymph Node. Japanese Journal of Lung Cancer, Vol. 46; n° 6; pg. 723-726(2006.) Autores: Igor Austin Fernandes Martins, Rafael Ruiz Machado e Douglas Jorge Racy, da Med Imagem – Beneficência Portuguesa de São Paulo. Nefroblastomatose Os termos nefroblastomatose e restos nefrogênicos (RN) descrevem persistência de focos do parênquima renal embrionário (blastema metanéfrico) além de 36 semanas de gestação, quando a nefrogênese é normalmente completa. RN são incidentalmente encontrados em aproximadamente 1% das autópsias de rins infantis e podem sofrer transformação maligna em nefroblastoma (tumor de Wilms) em 1% dos casos. Atualmente estima-se que 3044% dos tumores de Wilms têm como lesão precursora os restos nefrogênicos, e estes são encontrados em até 99% dos tumores de Wilms bilaterais. Restos nefrogênicos podem ser únicos, múltiplos ou difusos. São divididos em perilobar e intralobar com base na localização e nas síndromes com o qual estão associados. Restos perilobares são encontrados no córtex periférico ou colunas de Bertin. Estão associados 4 | Caderno 2 com a síndrome de Beckwith-Wiedemann, hemi-hipertrofia, síndrome de Perlman e trissomia do 18. Os intralobares são consideravelmente menos comuns que o tipo perilobar, mas têm uma maior associação com o desenvolvimento do tumor de Wilms. Clinicamente os pacientes portadores de RN são assintomáticos, e geralmente seu diagnóstico é incidental (em exames de imagem ou no intra-operatório) em conjunto com um tumor de Wilms. A nefroblastomatose difusa, pode ser sintomática, se manifestando como massa abdominal uni ou bilateral e pode ser palpável ao nascimento. Geralmente é descoberta dentro dos primeiros 12 meses de vida. O estudo ultrassonográfico revela nódulos hipoecóicos, embora as lesões possam ser iso ou hiperecogênicas em comparação com o parênquima renal normal. É um método menos sensível do que a RM e a TC. No entanto, o seu baixo custo e a ausência de radiação o torna atrativo para o rastreamento. Na tomografia computadorizada do paciente com RN, podemos observar nódulos periféricos com baixa atenuação e discreto realce em relação ao parênquima renal adjacente. É um importante método de avaliação tanto nos estudos iniciais de crianças com tumor de Wilms quanto no acompanhamento de crianças com nefroblastomatose. Na ressonância magnética, apresenta-se com hipossinal em T1 e sinal variável em T2. É importante ressaltar que tanto na TC quanto na RM os restos nefrogênicos tendem a ser homogêneos enquanto que o tumor de Wilms heterogêneo. Crianças com síndromes associadas a RN, devem ser submetidas a uma TC de base, para rastreamento de tumor de Wilms. O seguimento renal com USG deve ser realizado a cada 3 meses até os 7 anos de idade, quando o risco de desenvolvimento em Tumor de Wilms diminui substancialmente. O rastreamento deve ser realizado até os 10 anos de idade, quando o risco de degeneração em tumor de Wilms se torna mínimo. A escolha do tratamento permanence controvérsa. Alguns autores sugerem a quimioterapia, enquanto outros sustentam que um seguimento já é suficiente, já que a quimioterapia adjuvante não impede a transformação maligna dos restos nefrogênicos. Referências Bibliográficas 1.Lisa H.Lowe, MD. Pediatric Renal Masses: Wilms Tumor and Beyond Radiographics November 2000 20:6 15851603. 2.Gael J. Lonergan, Lt Col, USAF, MC. Nephrogenic rests, nephroblastomatosis, and associated lesions of the kidney. Radiographics July 1998 18:4 947968. 3.Keith S. White, MD. Imaging of nephroblastomatosis: an overview. Radiology January 1992 182:1 1-5
Documentos relacionados
Newsletter: Vol. 06 – # 16 – Genética dos Tumores de Wilms
 diferenças de emenda do RNA. A isoforma II está relacionada à presença de três
aminoácidos entre o terceiro e o quarto dedos de zinco, lisina (K), treonina (T) e serina
(S) e a proteína pode ser fo...
diferenças de emenda do RNA. A isoforma II está relacionada à presença de três
aminoácidos entre o terceiro e o quarto dedos de zinco, lisina (K), treonina (T) e serina
(S) e a proteína pode ser fo...